Introducción
La nefritis lúpica (NL) es un tipo de glomerulonefritis que se desarrolla como consecuencia del lupus eritematoso sistémico (LES)1,2. La NL se clasifica histológicamente en seis clases (I-VI)3, siendo las más frecuentes las tipo III y IV (proliferativas), por lo que la evidencia para las otras es menos sólida1.
La NL se presenta aproximadamente en el 50 a 60% de las personas con LES, en quienes es una de las principales causas de morbimortalidad puesto que se asocia a falla renal o muerte1,2. En suma, la prevalencia, severidad y mortalidad de la NL son mayores en hispanos, afroamericanos, y asiáticos4.
El tratamiento farmacológico de la NL consta de las fases de inducción y mantenimiento1. Entre los fármacos principalmente utilizados durante estas fases, se encuentran los antimaláricos, glucocorticoides (GC), inmunosupresores como micofenolato mofetilo (MMF) y ciclofosfamida (CYC) endovenosa, entre otros1,2. Sin embargo, la incidencia de respuesta renal completa suele ser baja (~20 a 30%)1,5,6, y tanto las recaídas como los eventos adversos pueden ser frecuentes con estas terapias1. Por ello, actualmente se ha propuesto el uso de diferentes dosis de dichos fármacos y otros inmunosupresores ya sea solos o en combinación.
La evaluación de los beneficios y daños de estos fármacos permitirá conocer cuáles son las opciones más eficaces y seguras que logren inducir la remisión de la enfermedad, prevenir las recaídas, prevenir la progresión a falla renal y disminuir la mortalidad de los adultos con diagnóstico reciente de NL.
En base a lo anterior, la Dirección de Guías de Práctica Clínica, Farmacovigilancia y Tecnovigilancia del Instituto de Evaluación de Tecnologías en Salud e Investigación (IETSI) de EsSalud elaboró la guía de práctica clínica (GPC) basada en evidencias para tratamiento farmacológico inicial de nefritis lúpica, cuyas recomendaciones serán aplicadas por profesionales de la salud en EsSalud. El presente artículo es un resumen de dicha GPC.
Metodología
El procedimiento seguido para la elaboración de la presente GPC está detallado en su versión “in extenso”, la cual puede descargarse de la página web del IETSI de EsSalud (http://www.essalud.gob.pe/ietsi/guias_pract_clini.html).
En resumen, se aplicó la siguiente metodología:
Conformación del grupo elaborador de la guía (GEG):
Se conformó un GEG, que incluyó metodólogos y médicos reumatólogos, nefrólogos e internistas.
Formulación de preguntas:
En concordancia con los objetivos y alcances de esta GPC, el GEG formuló 6 preguntas clínicas (Tabla 1), cada una de las cuales pudo tener una o más preguntas PICO (Population, Intervention, Comparator, Outcome). A su vez, cada pregunta PICO pudo tener uno o más desenlaces (o outcomes) de interés.
Búsqueda y selección de la evidencia:
Para cada pregunta PICO, durante junio a agosto del 2021, se buscaron revisiones sistemáticas (RS) publicadas como artículos científicos (mediante búsquedas sistemáticas en PubMed) o realizadas como parte de una GPC previa (mediante una búsqueda sistemática de GPC). Cuando se encontraron RS de calidad aceptable según el instrumento A Measurement Tool to Assess Systematic Reviews-II (AMSTAR II)7, se escogió una para cada desenlace de interés, la cual fue actualizada cuando el GEG lo consideró necesario. Cuando no se encontró ninguna RS de calidad aceptable, se realizó una búsqueda de novo de estudios primarios (Material suplementario 1).
Evaluación de la certeza de la evidencia:
Para cada desenlace de cada pregunta PICO, se evaluó la certeza de la evidencia siguiendo la metodología de Grading of Recommendations Assessment, Development, and Evaluation (GRADE)8 (Material suplementario 2).
Formulación de las recomendaciones:
El GEG revisó la evidencia seleccionada para cada pregunta clínica en reuniones periódicas, usando los marcos Evidence to Decision (EtD) de la metodología GRADE (9, 10) (Material suplementario 2). Para ello, tuvo en consideración: 1) Beneficios y daños de las opciones, 2) Valores y preferencias de los pacientes, 3) Aceptabilidad por parte de los profesionales de salud y pacientes, 4) Equidad, 5) Factibilidad de las opciones en EsSalud, y 6) Uso de recursos. Luego de discutir estos criterios para cada pregunta, el GEG, por consenso o por mayoría simple, formuló cada recomendación, asignándole una fuerza (fuerte o condicional) y una certeza de la evidencia (alta, moderada, baja, o muy baja) (Tabla 2).
Formulación de buenas prácticas clínicas:
El GEG formuló buenas prácticas clínicas (BPC), usualmente en base a su experiencia clínica o a adopciones de otras guías o protocolos (Tabla 1).
Revisión por expertos externos:
La presente GPC fue revisada en reuniones con especialistas representantes de otras instituciones, tomadores de decisiones de EsSalud, y pacientes. Asimismo, su versión extensa fue enviada por vía electrónica a expertos externos para su revisión (mencionados en la sección de agradecimientos). Cuando fue pertinente, el GEG tuvo en cuenta los resultados de estas revisiones para modificar las recomendaciones finales.
Actualización de la GPC:
La presente GPC tiene una vigencia de tres años. Al acercarse al fin de este período, se procederá a realizar una RS de la literatura para su actualización, luego de la cual se decidirá si se actualiza la presente GPC o se procede a realizar una nueva versión.
Desarrollo de recomendaciones
La presente GPC abordó 6 preguntas clínicas, en base a las cuales se formularon 11 recomendaciones (todas condicionales), 22 BPC, y 2 flujogramas (Tabla 1, Figura 1 y Figura 2).
Tabla 1 Lista de recomendaciones y buenas prácticas clínicas (BPC).
| Enunciado | Tipo * | Certeza ** | |
| Consideraciones generales sobre el tratamiento farmacológico de la nefritis lúpica (NL) | |||
| En adultos con NL clase I a V no refractarios, se debe coadministrar antimaláricos (ej. hidroxicloroquina a dosis que no exceda los 5 mg/kg/día vía oral y disminuirla gradualmente) como parte del cuidado estándar durante las fases de inducción y mantenimiento, a menos que hubiera alguna contraindicación. | BPC | ||
| En adultos con NL clase I a V no refractarios que presenten proteinuria > 500 mg/día o hipertensión arterial, brindar inhibidores de la enzima convertidora de angiotensina (IECA) o antagonistas del receptor de angiotensina II (ARA-II) a dosis recomendadas por guías de práctica clínica basadas en evidencia. | BPC | ||
| En adultos con NL clase I a V no refractarios, considere brindar estatinas en base a los niveles lipídicos y riesgo cardiovascular a 10 años. Brindar las estatinas a dosis recomendadas por guías de práctica clínica basadas en evidencia. | BPC | ||
| Considerar definir respuesta renal completa cuando se obtenga: Proteinuria ≤ 0.8 g/día y Empeoramiento de la tasa de filtración glomerular estimada (TFGe) no mayor a 20% del valor basal o una TFGe ≥ 60 mL/min/1.73 m2. | BPC | ||
| Considerar definir respuesta renal parcial cuando se obtenga: Reducción de la proteinuria ≥ 50% del valor basal y ≤ 3 g/día y Empeoramiento de la TFGe basal no mayor a 20% del valor basal. | BPC | ||
| Tratamiento farmacológico en la fase de inducción | |||
| Pregunta 1: En adultos con nefritis lúpica (NL) clase I a V no refractarios, ¿se debería iniciar la fase de inducción brindando glucocorticoides (GC) orales a dosis medias en lugar de dosis altas? | |||
| Considerar las siguientes dosis de inicio de GC orales: Dosis medias: prednisona a 0.3-0.5 mg/kg/día o equivalentes. Dosis altas: prednisona a 1 mg/kg/día o equivalentes. Luego, disminuirla progresivamente hasta ≤ 5 mg/día o equivalentes, excepto cuando otras manifestaciones lúpicas requieran administrar dosis mayores. | BPC | ||
| En adultos con NL clase I a II no refractarios en fase de inducción: Cuando se presente proteinuria en rango nefrótico (> 3 g/día), considere brindar GC orales a dosis medias con descenso progresivo más inmunosupresores durante seis meses. Cuando no se presente proteinuria en rango nefrótico, la decisión sobre brindar estas terapias debe ser individualizada y tomando en cuenta la presencia de otras manifestaciones lúpicas. Considere brindar pulsos de GC endovenosos teniendo en cuenta otras manifestaciones de la enfermedad. | BPC | ||
| En adultos con NL clase III a V no refractarios en fase de inducción, primero brindar pulsos de GC endovenosos (metilprednisolona a 0.25-0.50 g/día o equivalentes durante uno a tres días) y luego brindar GC orales en combinación con algún inmunosupresor para disminuir las dosis acumuladas de GC. | BPC | ||
| En adultos con NL clase III a V no refractarios, sugerimos considerar iniciar la fase de inducción brindando GC orales a dosis medias en lugar dosis altas en combinación con algún inmunosupresor. | Recomendación condicional a favor de la intervención | Muy baja (⊕⊝⊝⊝) | |
| En adultos con NL clase I a V se podría considerar el uso de GC orales a dosis altas en casos especiales: en los que la gravedad de la enfermedad y/o la presencia de otras manifestaciones lúpicas hagan revalorar la decisión. | BPC | ||
| Pregunta 2: En adultos con nefritis lúpica (NL) clase III a V no refractarios, ¿se debería brindar micofenolato mofetilo (MMF) en lugar de ciclofosfamida (CYC) endovenosa como terapia inicial de la fase de inducción? | |||
| En adultos con NL clase III a IV no refractarios, sugerimos brindar -en combinación con glucocorticoides- MMF en lugar de CYC endovenosa, como terapia inicial de la fase de inducción. | Recomendación condicional a favor de la intervención | Baja (⊕⊕⊝⊝) | |
| En adultos con NL clase V no refractarios, sugerimos brindar -en combinación con glucocorticoides- MMF en lugar de CYC endovenosa, como terapia inicial de la fase de inducción. | Recomendación condicional a favor de la intervención | Muy baja (⊕⊝⊝⊝) | |
| Considerar la siguiente dosis de MMF: 2-3 g/día por vía oral durante seis meses. | BPC | ||
| En adultos con NL clase III a V se podría considerar optar por el uso de CYC endovenosa como terapia inicial en casos especiales: cuando no se contemple el embarazo y/o cuando las comorbilidades, presencia de otras manifestaciones lúpicas o contraindicaciones a otros fármacos para inducción hagan revalorar esta decisión. | BPC | ||
| Pregunta 3: En adultos con nefritis lúpica (NL) clase III a V no refractarios, en quienes se decida iniciar la fase de inducción con ciclofosfamida (CYC) endovenosa, ¿se debería brindar CYC a dosis bajas en lugar de dosis altas? | |||
| En adultos con NL clase III a IV no refractarios, en quienes se decida iniciar la fase de inducción con CYC endovenosa en combinación con glucocorticoides, sugerimos brindar dosis bajas en lugar de dosis altas. | Recomendación condicional a favor de la intervención | Baja (⊕⊕⊝⊝) | |
| En adultos con NL clase V no refractarios, en quienes se decida iniciar la fase de inducción con CYC endovenosa en combinación con glucocorticoides, sugerimos brindar CYC a dosis bajas o dosis altas. | Recomendación condicional a favor de ambas opciones | Muy baja (⊕⊝⊝⊝) | |
| Considerar las siguientes dosis de CYC endovenosa: Dosis bajas: 0.5 g cada 15 días por vía endovenosa hasta completar seis dosis. Dosis altas: 0.5-1 g/m2/mes por vía endovenosa durante seis meses. | BPC | ||
| En adultos con NL clase III a V se podría considerar el uso de CYC endovenosa a dosis altas en casos especiales: en los que la gravedad de la enfermedad y/o presencia de otras manifestaciones lúpicas hagan revalorar esta decisión. | BPC | ||
| Cuando se brinde CYC endovenosa, ajustar la dosis en curso en caso se presente deterioro de la función renal y/o daño hepático severo. | BPC | ||
| Pregunta 4: En adultos con nefritis lúpica (NL) clase III a V no refractarios, ¿se debería brindar tacrolimus (TAC) en lugar de los inmunosupresores convencionales (micofenolato mofetilo (MMF) o ciclofosfamida (CYC) endovenosa) como terapia inicial de la fase de inducción? | |||
| En adultos con NL clase III a IV no refractarios, sugerimos brindar -en combinación con glucocorticoides- MMF en lugar de TAC, como terapia inicial de la fase de inducción. | Recomendación condicional a favor del control | Muy baja (⊕⊝⊝⊝) | |
| En adultos con NL clase III a IV no refractarios, sugerimos brindar -en combinación con glucocorticoides- TAC o CYC endovenosa, como terapia inicial de la fase de inducción. | Recomendación condicional a favor de ambas opciones | Muy baja (⊕⊝⊝⊝) | |
| En adultos con NL clase III a IV , para elegir iniciar con TAC o CYC endovenosa considerar: contraindicaciones para el uso de alguno de estos fármacos, deseo de embarazo (preferir TAC), presencia de deterioro de la función renal (preferir CYC endovenosa), y otras manifestaciones lúpicas que orienten la decisión. | BPC | ||
| Considerar lo siguiente respecto a la dosis de TAC: TAC: 0.05-0.15 mg/kg/día vía oral divido en dos dosis durante seis meses. Si es posible, dosar los niveles séricos de TAC para alcanzar una concentración de 6-10 ng/mL en el primer y segundo mes, y de 4-8 ng/mL en los meses restantes. | BPC | ||
| En adultos con NL clase V no refractarios, sugerimos brindar -en combinación con glucocorticoides- MMF en lugar de TAC, como terapia inicial de la fase de inducción. | Recomendación condicional a favor del control | Muy baja (⊕⊝⊝⊝) | |
| En adultos con NL clase III a V se podría considerar el uso de TAC en lugar de MMF en casos especiales: cuando MMF este contraindicado, cuando el riesgo de herpes zoster implique consecuencias importantes para el paciente o para la continuidad del tratamiento, y/o cuando presencia de otras manifestaciones lúpicas hagan revalorar esta decisión. | BPC | ||
| Pregunta 5: En adultos con nefritis lúpica (NL) clase III a V no refractarios, ¿se debería brindar terapia combinada de tacrolimus (TAC) más micofenolato mofetilo (MMF) (terapia multitarget) en lugar de monoterapia con ciclofosfamida (CYC) endovenosa como terapia inicial de la fase de inducción? | |||
| En adultos con NL clase III a IV no refractarios, sugerimos brindar -en combinación con glucocorticoides- TAC más MMF (terapia multitarget) en lugar de CYC endovenosa, como terapia inicial de la fase de inducción. | Recomendación condicional a favor de la intervención | Baja (⊕⊕⊝⊝) | |
| En adultos con NL clase V no refractarios, sugerimos brindar -en combinación con glucocorticoides- TAC más MMF (terapia multitarget) en lugar de CYC endovenosa, como terapia inicial de la fase de inducción. | Recomendación condicional a favor de la intervención | Baja (⊕⊕⊝⊝) | |
| Considerar las siguientes dosis de la terapia multitarget: TAC: 2-4 mg/día vía oral durante seis meses. MMF: 0.5-1 g/día vía oral durante seis meses. | BPC | ||
| En adultos con NL clase III a V se podría considerar el uso de CYC endovenosa en casos especiales: cuando TAC o MMF estén contraindicados, ante deterioro de la función renal, y/o presencia de otras manifestaciones lúpicas que hagan revalorar esta decisión. | BPC | ||
| Tratamiento farmacológico en la fase de mantenimiento | |||
| Pregunta 6: En adultos con nefritis lúpica (NL) clase I a V no refractarios, ¿se debería brindar micofenolato mofetilo (MMF) en lugar azatioprina (AZA) como terapia inicial de la fase de mantenimiento? | |||
| En adultos con NL clase I a V no refractarios, sugerimos brindar -en combinación con glucocorticoides- MMF en lugar de AZA, como terapia inicial de la fase de mantenimiento. | Recomendación condicional a favor de la intervención | Muy baja (⊕⊝⊝⊝) | |
| Considerar las siguientes dosis: MMF: 1-2 g/día por vía oral durante tres a cinco años. AZA: 1.5-2 mg/kg/día por vía oral durante tres a cinco años. | BPC | ||
| En adultos con NL clase I a V se podría considerar el uso de AZA en casos especiales: cuando se contemple el embarazo y/o el MMF esté contraindicado. | BPC | ||
| Durante la fase de mantenimiento continuar disminuyendo gradualmente la dosis de glucocorticoides (GC) a la mínima posible (prednisona ≤ 5 mg/día o equivalentes), excepto cuando otras manifestaciones lúpicas requieran administrar dosis mayores. Podría considerarse la descontinuación de los GC cuando la respuesta renal completa se mantenga por 12 meses o más pero esta decisión debe ser individualizada teniendo en cuenta la actividad de la enfermedad, y presencia de comorbilidades. | BPC | ||
* Recomendación basada en evidencias, ® o buenas prácticas clínicas (BPC) basadas en consenso.
** La certeza de la evidencia solo se establece para las recomendaciones, mas no para las BPC.
Tabla 2 Significado de los niveles de certeza de la evidencia y de la fuerza de la recomendación.
| Significado de los niveles de certeza de la evidencia y de la fuerza de la recomendación | ||
| Enunciado | Significado | |
| Certeza de la evidencia | Alta (⨁⨁⨁⨁) | Cuando se usa para describir la certeza para cierto desenlace: significa que es muy probable que el verdadero efecto sea similar al efecto estimado. Para expresar esta certeza en los efectos de los desenlaces se utilizó el fraseo “se evitarán/causarán, incrementará/disminuirá, no modificará …”. Cuando se usa para describir la certeza para cierta recomendación: significa que nuestra confianza en la evidencia usada para tomar la decisión es alta. |
| Moderada (⨁⨁⨁◯) | Cuando se usa para describir la certeza para cierto desenlace: significa que es probable que el verdadero efecto sea similar al efecto estimado. Para expresar esta certeza en los efectos de los desenlaces se utilizó el fraseo “probablemente se evitarán/causarán, incrementará/disminuirá, no modificará …”. Cuando se usa para describir la certeza para cierta recomendación: significa que nuestra confianza en la evidencia usada para tomar la decisión es moderada. | |
| Baja (⨁⨁◯◯) | Cuando se usa para describir la certeza para cierto desenlace: significa que el verdadero efecto podría ser sustancialmente diferente al efecto estimado. Para expresar esta certeza en los efectos de los desenlaces se utilizó el fraseo “posiblemente se evitarán/causarán, incrementará/disminuirá, no modificará …”. Cuando se usa para describir la certeza para cierta recomendación: significa que nuestra confianza en la evidencia usada para tomar la decisión es baja. | |
| Muy baja (⨁◯◯◯) | Cuando se usa para describir la certeza para cierto desenlace: significa que existe mucha incertidumbre sobre los efectos evaluados. Para expresar esta certeza en los efectos de los desenlaces se utilizó el fraseo “posiblemente se evitarán/causarán, incrementará/disminuirá, no modificará… pero esto es incierto”. Cuando se usa para describir la certeza para cierta recomendación: significa que nuestra confianza en la evidencia usada para tomar la decisión es muy baja. | |
| Fuerza de la recomendación | Recomendación fuerte (a favor o en contra) | El GEG considera que esta recomendación debe seguirse en todos o casi todos los casos, salvo excepciones puntuales y bien justificadas. En la formulación de la recomendación se usa el término “ recomendamos ”. |
| Recomendación condicional (a favor o en contra) | El GEG considera que esta recomendación se seguirá en la mayoría de los casos, aunque podría ser oportuno no aplicarlas en algunos casos, siempre que esto sea justificado. En la formulación de la recomendación se usa el término “ sugerimos ”. | |
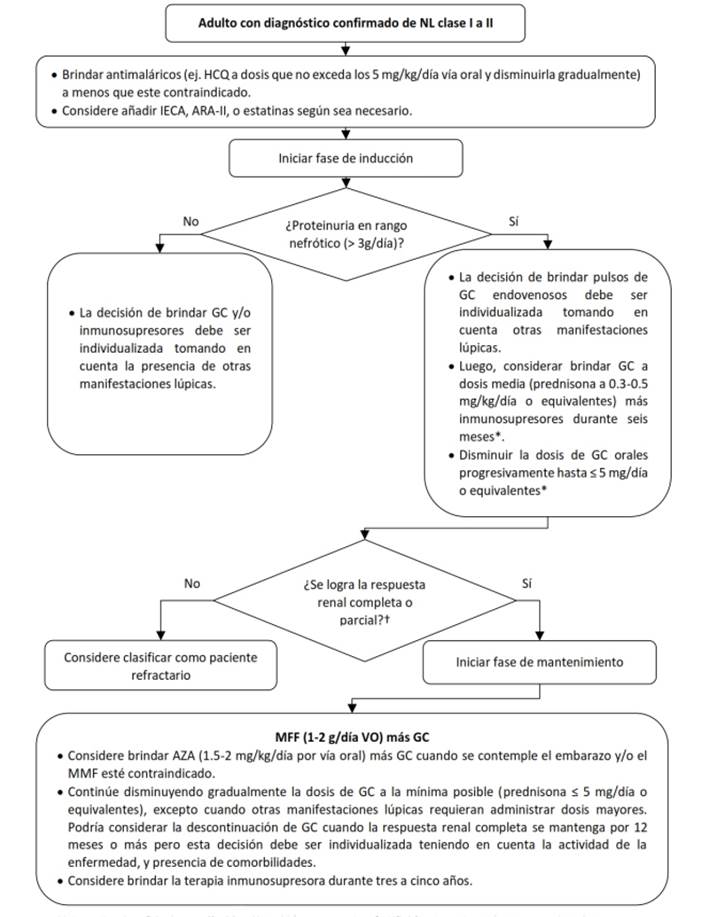
Figura 1 Flujograma para el tratamiento farmacológico inicial de adultos con nefritis lúpica clases I a II.
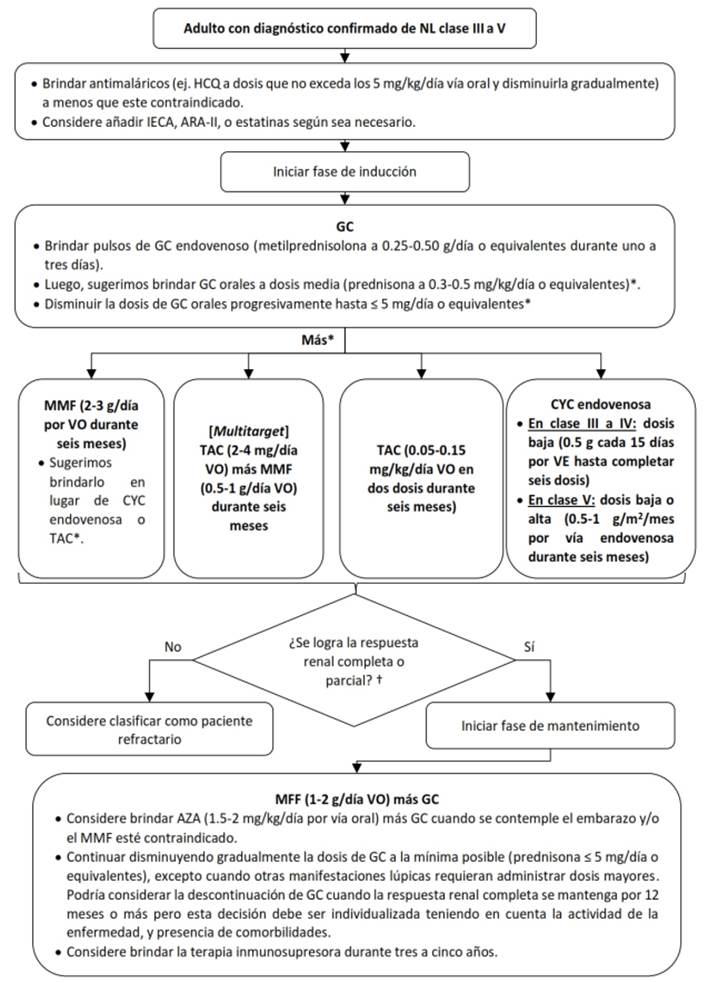
Figura 2 Flujograma para el tratamiento farmacológico inicial de adultos con nefritis lúpica clases III a V.
A continuación, se expondrán las recomendaciones para cada pregunta clínica, así como un resumen del razonamiento seguido para llegar a cada recomendación. No se incluyó la justificación de las BPC, las cuales se pueden leer en el documento in-extenso.
Tratamiento farmacológico inicial en fase de inducción
Pregunta 1. En adultos con nefritis lúpica (NL) clase I a V no refractarios, ¿se debería iniciar la fase de inducción brindando glucocorticoides (GC) orales a dosis medias en lugar de dosis altas?
Subpoblación de adultos con NL clase I a V
Se establecieron BPC ya que no se encontró evidencia que permitió emitir una recomendación.
Subpoblación de adultos con NL clase III a V
Evidencia: En la búsqueda sistemática se encontró una RS11, la cual se eligió por tener calidad metodológica aceptable. A continuación, se muestran los beneficios y daños de brindar -en combinación con inmunosupresores- GC a dosis medias (0.5 mg/día) en lugar de brindar GC a dosis altas (1 mg/día).
Beneficios: Posiblemente no modificaríamos la respuesta renal parcial. Además, posiblemente no modificaríamos la mortalidad, remisión respuesta renal completa ni la frecuencia de recaídas, pero esto es incierto. Sin embargo, una cohorte en adultos con NL sugiere que los GC orales a dosis medias podrían asociarse a un menor riesgo de toxicidad global y metabólica a un tiempo de seguimiento de 11.5 años. Cabe mencionar que este estudio tiene limitaciones y estos efectos tendrían que confirmarse con estudios mejor diseñados12.
Daños: Posiblemente no modificaríamos el riesgo de infección de cualquier tipo, infección por virus de Herpes Zoster, hipertensión arterial, ni de eventos adversos gastrointestinales, pero esto es incierto.
Recomendación: Los beneficios se consideraron pequeños (puesto que el inicio con GC a dosis media podría ser más seguro a largo plazo plazo) y los daños se consideraron triviales (puesto que posiblemente no haya diferencias en otros eventos adversos). Por ello, se emitió una recomendación a favor de la intervención. Puesto que la certeza de evidencia fue muy baja, no se conocen los efectos en otros desenlaces importantes para los pacientes, y la aceptabilidad puede ser variable, esta recomendación fue condicional.
Pregunta 2. En adultos con nefritis lúpica (NL) clase III a V no refractarios, ¿se debería brindar micofenolato mofetilo (MMF) en lugar de ciclofosfamida (CYC) endovenosa como terapia inicial de la fase de inducción?
Subpoblación de adultos con NL clase III a IV
Evidencia: En la búsqueda sistemática se encontraron tres RS11,13,14, de las cuales se eligieron las que tuvieron búsquedas recientes, y mayor número de estudios incluidos11,13. A continuación, se muestran los beneficios y daños de brindar -en combinación con GC- MMF a 1000 personas en lugar de CYC endovenosa.
Beneficios: Posiblemente evitaríamos 146 casos de infección de cualquier tipo (IC95%: -88 a -188), 166 casos de falla ovárica (IC95%: -128 a -187), 57 casos de leucopenia (IC95%: -17 a -78), 140 casos de alopecia (IC95%: -100 a -153), y 110 casos de eventos adversos gastrointestinales (IC95%: -61 a -144). En contraste, posiblemente no modificaríamos la mortalidad, la falla renal, respuesta renal completa, respuesta renal parcial, recaída renal, o el mantenimiento de la función renal estable. En hispanos, posiblemente causaríamos 225 casos más de respuesta renal parcial (IC95%: +44 a +376) pero esto es incierto.
Daños: Posiblemente no modificaríamos el riesgo de infección por virus Herpes Zoster e irregularidad menstrual pero esto es incierto.
Recomendación: Los beneficios se consideraron moderados (puesto que el tamaño del efecto sobre la respuesta renal parcial en hispanos y falla ovárica se sería importante. Además, los efectos sobre la alopecia, infección de cualquier tipo, leucopenia, y eventos adversos gastrointestinales importantes no serían despreciables) y los daños se consideraron triviales (puesto que el tamaño del efecto sobre la infección por virus Herpes Zoster e irregularidad menstrual posiblemente sean similares con el uso de ambas terapias y poco frecuentes). Por ello, se emitió una recomendación a favor de la intervención. Dado que la certeza de evidencia fue baja, no se conocen los efectos en otros desenlaces importantes para los pacientes hispanos, y la aceptabilidad puede ser variable, esta recomendación fue condicional.
Subpoblación de adultos con NL clase V
Evidencia: En la búsqueda sistemática se encontró una RS15, la cual se eligió por tener calidad metodológica aceptable. A continuación, se muestran los beneficios y daños de la comparación mencionada en esta pregunta.
Beneficios: En hispanos, posiblemente causaríamos 225 casos más de respuesta renal parcial (IC95%: +44 a +376) pero esto es incierto. En contraste, posiblemente no modificaríamos la mortalidad ni la respuesta renal completa pero esto es incierto.
Daños: Posiblemente no modificaríamos el riesgo de infección de cualquier tipo pero esto es incierto.
Recomendación: Los beneficios se consideraron pequeños (puesto que el tamaño del efecto sobre la respuesta renal parcial en hispanos no sería despreciable y es incierto si modifique la mortalidad o respuesta renal completa) y los daños se consideraron triviales (puesto que el tamaño del efecto sobre la infección de cualquier tipo posiblemente sea similar con el uso de ambas terapias). Por ello, se emitió una recomendación a favor de la intervención. Puesto que la certeza de evidencia fue muy baja, no se conocen los efectos en otros desenlaces importantes para hispanos, y la aceptabilidad puede ser variable, esta recomendación fue condicional.
Pregunta 3. En adultos con nefritis lúpica (NL) clase III a V no refractarios, en quienes se decida iniciar la fase de inducción con ciclofosfamida (CYC) endovenosa, ¿se debería brindar CYC a dosis bajas en lugar de dosis altas?
Subpoblación de adultos con NL clase III a IV
Evidencia: En la búsqueda sistemática se encontraron tres RS11,16,17, de las cuales se eligieron las que tuvieron calidad metodológica aceptable, búsquedas recientes, y mostraron los efectos para esta comparación11,16. A continuación, se muestran los beneficios y daños de brindar -en combinación con GC- CYC endovenosa a dosis bajas a 1000 personas en lugar de dosis altas.
Beneficios: Probablemente evitaríamos 73 casos menos de infección de cualquier tipo (IC95%: -6 a -124) y 121 casos menos de irregularidad menstrual (IC95%: -72 a -155). En contraste probablemente no modificaríamos la respuesta renal completa, respuesta renal parcial, y posiblemente no modificaríamos la mortalidad a 6 ni 12 meses, actividad de la enfermedad. Además, posiblemente no modificaríamos la mortalidad a 5-10 años, falla renal a 5-10 años, ni la recaída renal pero esto es incierto.
Daños: Probablemente no modificaríamos el riesgo de eventos adversos gastrointestinales y posiblemente no modificaríamos el riesgo de hematotoxicidad. Además, posiblemente no modificaríamos el riesgo de falla ovárica pero esto es incierto.
Recomendación: Los beneficios se consideraron pequeños (puesto que el tamaño de los efectos para evitar infecciones de cualquier tipo así como irregularidad menstrual, podrían ser importantes para un grupo de pacientes) y los daños se consideraron triviales (puesto que el tamaño del efecto sobre los eventos adversos gastrointestinales, hematotoxicidad y falla ovárica posiblemente sean similares con el uso de ambas dosis y poco frecuentes). Por ello, se emitió una recomendación a favor de la intervención. Puesto que la certeza de la evidencia fue baja y la aceptabilidad puede ser variable, esta recomendación fue condicional.
Subpoblación de adultos con NL clase V
Evidencia: En la búsqueda sistemática se encontró una RS16, la cual se eligió por tener calidad metodológica aceptable. A continuación, se muestran los beneficios y daños de la comparación mencionada en esta pregunta.
Beneficios: Probablemente no modificaríamos la respuesta renal completa o parcial, y posiblemente no modificaríamos la actividad de la enfermedad. En adición, posiblemente no modificaríamos la recaída renal pero esto es incierto.
Daños: Posiblemente no modificaríamos el riesgo de infección de cualquier tipo, irregularidad menstrual, hematotoxicidad, ni de eventos adversos gastrointestinales pero esto es incierto.
Recomendación: Los beneficios se consideraron triviales (puesto que el tamaño de los efectos en la respuesta renal completa o parcial, recaída renal, y actividad de la enfermedad podrían ser similares entre las dosis) y los daños se consideraron triviales (puesto que el tamaño de los efectos en la infección de cualquier tipo, irregularidad menstrual, hematotoxicidad, y eventos adversos gastrointestinales podrían ser similares entre las dosis). Por ello, esta recomendación fue a favor de ambas opciones. Puesto que la certeza de evidencia fue muy baja, no se conocen los efectos en otros desenlaces importantes, y la aceptabilidad de las terapias puede ser variable, esta recomendación fue condicional.
Pregunta 4. En adultos con nefritis lúpica (NL) clase III a V no refractarios, ¿se debería brindar tacrolimus (TAC) en lugar de los inmunosupresores convencionales (micofenolato mofetilo (MMF) o ciclofosfamida (CYC) endovenosa) como terapia inicial de la fase de inducción?
Subpoblación de adultos con NL clase III a IV
Evidencia: En la búsqueda sistemática se encontraron diez RS11,14,18-25, de las cuales se eligieron las que tuvieron calidad metodológica aceptable, búsquedas recientes, e incluyeron la mayor cantidad de estudios11,22. A continuación, se muestran los beneficios y daños de brindar -en combinación con GC- TAC a 1000 personas en lugar de CYC endovenosa y en lugar de MMF.
Tacrolimus versus micofenolato mofetilo
Beneficios: Posiblemente evitaríamos 157 casos de infección por virus Herpes Zoster (IC95%: -70 a -179) pero esto es incierto. En contraste, posiblemente no modificaríamos la mortalidad, falla renal, respuesta renal completa o parcial, respuesta renal completa, respuesta renal parcial, función renal estable ni la actividad de la enfermedad pero esto es incierto.
Daños: Posiblemente causemos 200 casos más de recaída renal (IC95%: +33 a +436) pero esto es incierto. En contraste, posiblemente no modificaríamos el riesgo de nefrotoxicidad, infección de cualquier tipo, irregularidad menstrual, leucopenia ni alopecia pero esto es incierto.
Recomendación: Los beneficios se consideraron pequeños (puesto que la cantidad de casos que se evitarían de infección por virus Herpes Zoster no sería despreciable) y los daños se consideraron moderados (puesto que la cantidad de casos de recaída renal sería considerable y las consecuencias serían importantes). Por ello, se emitió una recomendación a favor del control. Puesto que la certeza de la evidencia fue muy baja y puede haber casos especiales en los que el médico tratante considere iniciar con TAC, esta recomendación fue condicional.
Tacrolimus versus ciclofosfamida
Beneficios: Posiblemente causemos 18 casos más de respuesta renal completa o parcial (IC95%: +18 a +192) pero esto es incierto. En contraste, posiblemente no modificaríamos la mortalidad, respuesta renal completa ni parcial (evaluados individualmente), ni la función renal estable pero esto es incierto.
Daños: Posiblemente no modificaríamos el riesgo de duplicación de la creatinina sérica, infección de cualquier tipo, infección por virus Herpes Zoster, falla ovárica, irregularidad menstrual, leucopenia, alopecia ni eventos adversos gastrointestinales pero esto es incierto.
Recomendación: Los beneficios se consideraron triviales (puesto que el efecto encontrado fue en la respuesta renal completa o parcial, el cual es un desenlace compuesto con un tamaño del efecto que no se consideró importante, y que no evidenció beneficios al ser evaluado individualmente con evidencia más robusta) y los daños se consideraron triviales (puesto que los riesgos de los eventos adversos posiblemente sean similares con el uso de ambas terapias). Por ello, se emitió una recomendación a favor de ambas opciones. Puesto que la certeza de la evidencia fue muy baja, no se conocen los efectos en otros desenlaces críticos para la decisión, y la aceptabilidad puede ser variable, esta recomendación fue condicional.
Subpoblación de adultos con NL clase V
Evidencia: En la búsqueda sistemática no se encontraron RS. Se realizó una búsqueda de ECA, en la cual se encontraron dos ECA26,27 que fueron meta-analizados. A continuación, se muestran los beneficios y daños de brindar -en combinación con GC- TAC a 1000 personas en lugar de MMF (los ECA no evaluaron la comparación con CYC endovenosa).
Beneficios: Posiblemente evitaríamos 139 casos de infección por virus Herpes Zoster (IC95%: -56 a -168) pero esto es incierto. En contraste, posiblemente, no modificaríamos la mortalidad, falla renal, respuesta renal completa o parcial, respuesta renal completa, respuesta renal parcial ni la actividad de la enfermedad pero esto es incierto.
Daños: Posiblemente causaríamos 200 casos más de recaída renal (IC95%: +33 a +436) y tanto el riesgo de nefrotoxicidad como de tremor tendería a incrementarse pero esto es incierto. En contraste, posiblemente no modificaríamos el riesgo de infección de cualquier tipo, leucopenia, alopecia, evento adverso gastrointestinal, cefalea, tinnitus, ni calambre pero esto es incierto.
Recomendación: Los beneficios se consideraron pequeños (puesto que la cantidad de casos de infección por virus Herpes Zoster no sería despreciable) y los daños se consideraron moderados (puesto que la cantidad de casos de recaída renal sería considerable y las consecuencias serían importantes. Además, posiblemente el riesgo de nefrotoxicidad y tremor tienda a ser mayor). Por ello, se emitió una recomendación a favor del control. Puesto que la certeza de la evidencia fue muy baja, no se conocen los efectos sobre otros desenlaces importantes, y puede haber casos especiales en los que el médico tratante considere iniciar con esta terapia, esta recomendación fue condicional.
Pregunta 5. En adultos con nefritis lúpica (NL) clase III a V no refractarios, ¿se debería brindar terapia combinada de tacrolimus (TAC) más micofenolato mofetilo (MMF) (terapia multitarget) en lugar de monoterapia con ciclofosfamida (CYC) endovenosa como terapia inicial de la fase de inducción?
Subpoblación de adultos con NL clase III a IV
Evidencia: En la búsqueda sistemática se encontraron ocho RS11,14,21,24,28-31, de las cuales se eligieron las que tuvieron calidad metodológica aceptable, búsqueda reciente, e incluyeron mayor número de estudios11,30,31. A continuación, se muestran los beneficios y daños de brinda -en combinación con GC- TAC más MMF (multitarget) a 1000 personas en lugar de CYC endovenosa.
Beneficios: Posiblemente causaríamos 255 casos más de respuesta renal completa (IC95%: +165 a +360), 221 casos más de mantención de la función renal estable (IC95%: +113 a +357), evitaríamos 62 casos de leucopenia (IC95%: -34 a -76), y 110 casos de eventos adversos gastrointestinales (IC95%: -65 a -142). Además, posiblemente evitaríamos 43 casos de irregularidad menstrual (IC95%: -11 a -57) pero esto es incierto. En contraste, posiblemente no modificaríamos la respuesta renal parcial y la disminución del puntaje de actividad de la enfermedad posiblemente no se clínicamente importante (punto de corte de -4.0 puntos)32.
Daños: Posiblemente causaríamos 44 casos más de hipertensión arterial (IC95%: +8 a +124). En contraste, posiblemente no modificaríamos el riesgo de infección de cualquier tipo, infección por virus de Herpes Zoster e hipertensión arterial. Además, posiblemente no modificaríamos el riesgo de duplicación de la creatinina sérica y alopecia pero esto es incierto.
Recomendación: Los beneficios se consideraron moderados (puesto que el tamaño del efecto sobre la de respuesta renal completa y función renal estable se consideró importante, y el tamaño de los efectos sobre la leucopenia e irregularidad menstrual no serían despreciables) y los daños se consideraron pequeños (puesto que el tamaño del efecto sobre la hipertensión arterial no sería importante y, en caso ocurriera, sería manejable). Por ello, se emitió una recomendación a favor de la intervención. Puesto que la certeza de la evidencia fue baja, no se conocen los efectos en otros desenlaces importantes, y la aceptabilidad puede ser variable, esta recomendación fue condicional.
Subpoblación de adultos con NL clase V
Evidencia: En la búsqueda sistemática se encontró una RS30, la cual se eligió por tener calidad metodológica aceptable. A continuación, se muestran los beneficios y daños de la comparación mencionada en esta pregunta.
Beneficios: Posiblemente causaríamos 272 casos más de respuesta renal completa (IC95%: +122 a +486). En contraste, posiblemente no modifiquemos la respuesta renal parcial pero esto es incierto.
Daños: Posiblemente no modificaríamos el riesgo de duplicación de la creatinina sérica, infección por virus de Herpes Zoster, irregularidad menstrual, leucopenia, hipertensión arterial, alopecia, y eventos adversos gastrointestinales pero esto es incierto.
Recomendación: Los beneficios se consideraron moderados (puesto que el tamaño del efecto sobre la de respuesta renal completa y función renal estable se consideró importante) y los daños se consideraron triviales (puesto que los riesgos posiblemente sean similares con el uso de ambas terapias y relativamente infrecuentes). Por ello, se emitió una recomendación a favor de la intervención. Puesto que la certeza de la evidencia fue muy baja, no se conocen los efectos en otros desenlaces importantes, y la aceptabilidad puede ser variable, esta recomendación fue condicional.
Tratamiento farmacológico inicial en fase de mantenimiento
Pregunta 6. En adultos con nefritis lúpica (NL) clase I a V no refractarios, ¿se debería brindar micofenolato mofetilo (MMF) en lugar azatioprina (AZA) como terapia inicial de la fase de mantenimiento?
Evidencia: En la búsqueda sistemática se encontraron diez RS11,13,29,33-39, de las cuales se eligieron las de calidad metodológica aceptable, búsqueda más reciente, y que incluyeron mayor número de estudios11,35,39. A continuación, se muestran los beneficios y daños de brinda -en combinación con GC- MMF a 1000 personas en lugar de AZA.
Beneficios: Posiblemente evitaríamos 92 casos menos de irregularidad menstrual (IC95%: -116 a -28) y 95 casos menos de leucopenia (IC95%: -68 a -106). Además, posiblemente la descontinuación del tratamiento sea menor pero esto es incierto. En contraste, posiblemente no modificaríamos la mortalidad, falla renal ni el riesgo de recaída renal pero esto es incierto.
Daños: Posiblemente no modificaríamos el riesgo de duplicación de la creatinina sérica, infección de cualquier tipo, infección por virus Herpes Zoster, falla ovárica, alopecia, ni eventos adversos gastrointestinales pero esto es incierto.
Recomendación: Los beneficios se consideraron pequeños (puesto que el tamaño del efecto sobre leucopenia, amenorrea y descontinuación del tratamiento no serían despreciables) y los daños se consideraron triviales (puesto que los riesgos posiblemente sean similares con el uso de ambas terapias y relativamente infrecuentes y/o manejables). Por ello, se emitió una recomendación a favor de la intervención. Puesto que la certeza de la evidencia fue muy baja, y la aceptabilidad puede ser variable, esta recomendación fue condicional.















