INTRODUCCIÓN
Desde Adam Smith, las teorías económicas proponen que la toma decisiones (TD) son racionales, si son informadas 1. Sin embargo, nuevas investigaciones que sólo serían parcialmente racionales, ya que integran otros factores como las emociones, solidaridad, sesgos cognitivos, heurística y experiencia previa 2.
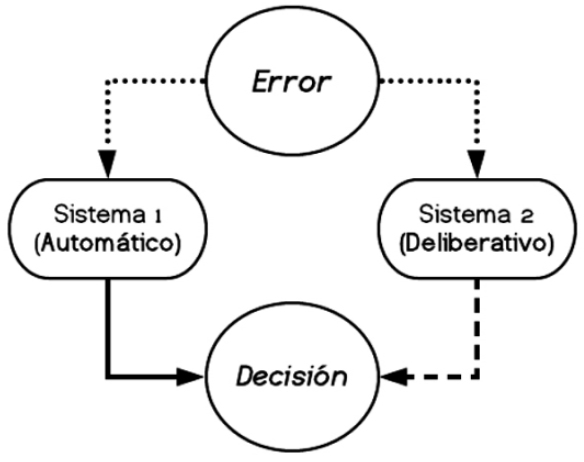
Daniel Kahneman 3,4, plantea que el ser humano toma decisiones mediante dos sistemas hipotéticos diferentes pero interrelacionados (Tabla 1):
“Sistema 1” o automático: inmediato, intuitivo y emocional, que permiten resolver las tareas simples como cruzar la calle ante un semáforo en verde o, en el área médica, aplicar antipiréticos a una persona con fiebre.
“Sistema 2” o deliberativo: prolongado, racional y de mayor marco informativo, que permiten resolver tareas complejas como decidir ante un semáforo en amarillo o determinar la causa de fiebre e indicar un tratamiento específico.
Tabla 1 Sistemas y situaciones de toma de decisiones en la práctica clínica neurológica
| Toma de decisiones | Situación hipotética |
|---|---|
| “Sistema 1” | Administrar algún antiagregante plaquetario a pacientes con diagnóstico de ictus isquémico del tipo aterotrombótico. |
| “Sistema 2” | En pacientes que presentan un nuevo ictus isquémico y que se encuentren en periodo de ventana (3 a 4.5 horas) para aplicar reperfusión terapéutica se debe elegir entre realizar solo tomografía sin contraste, angio-tomografía o angio-resonancia para mejorar la precisión diagnóstica. |
Estos dos sistemas teóricos no se basan en un sistema neurológico binario; sólo simplifican conceptualmente el proceso complejo de muchos sustratos neurofisiológicos 5,6. Según estudios de neuroimagen funcional 6, los sistemas neuroanatómicos implicados en TD son circuitos: a) corticales: prefrontal-ventromedial (evalúa el desenlace esperado), órbito-fronto-medial (el desenlace obtenido), órbito-fronto-lateral (asignación de un valor específico), prefrontal anterior (evalúa decisiones alternas), cingular anterior e ínsula (prevenir pérdidas o daños); b) subcorticales: sistemas dopaminérgicos mesolímbicos y mesocorticales (sensación placentera inmediata), amígdala (componente emocional) y núcleos basales (para actividades habituales ).
La propuesta de Kahneman, a pesar de la simplificación 7, permite explicar que la mayor parte de las situaciones diarias, requieren soluciones simples pero inmediatas y son resueltas con el “sistema 1” (predominantemente subcortical); sin embargo bajo ciertas circunstancias (sin estrés, información disponible, etc.) ciertos procesos cognitivos más complejos serían procesados por el “sistema 2” (predominantemente cortical) ponderando pros, contras, costes y efectos en la TD.
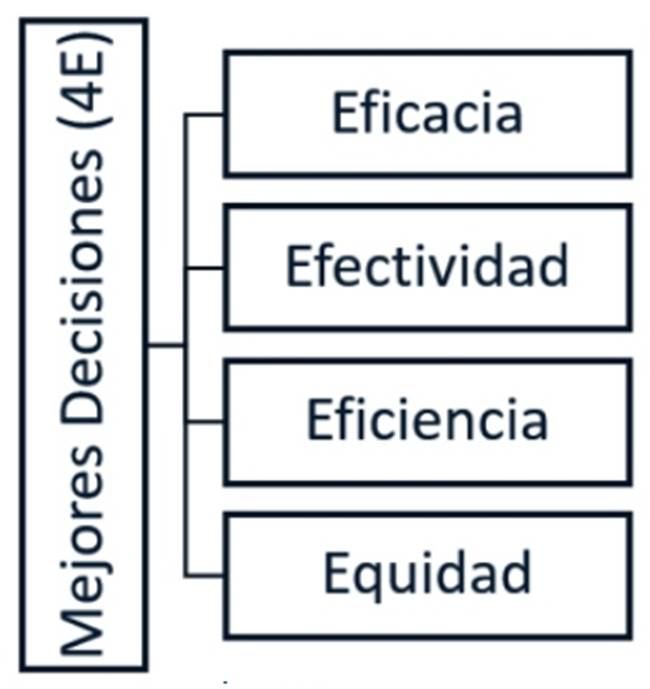
En esta revisión analizamos la TD en el quehacer médico y proponemos un marco teórico de “4E” (“eficacia”, “efectividad”, “eficiencia” y “equidad”) para mejorarlo, promoviendo un “sistema 2” alimentado por la mejor evidencia disponible y guiado por los valores-circunstancias de los pacientes.
DESARROLLO
Toma de decisiones y el error médico
La TD en la atención a pacientes en general, muchas veces se da en escenarios críticos y de alta incertidumbre, por lo que dichas decisiones estarían afectadas por factores similares a los escenarios económicos.
Los errores médicos son frecuentes, se ha estimado que hasta 98.000 personas mueren en un año por errores médicos hospitalarios 8. El paradigma cognitivo de la TD nos permite entender qué factores podrían contribuir a explicar y controlarlos, evitando sus consecuencias.
Los errores surgen en cualquier etapa del proceso de TD, en la automática (sistema 1) - p.e., prescripciones inadecuadas basadas en recomendación de expertos o por influencia del marketing farmacéutico - como en la deliberativa (sistema 2) - p.e., no incorporar o entender críticamente nueva información disponible para decidir sobre alternativas de solución 3,4 (Figura 1).
La medicina científica y la toma de decisiones sanitarias
La medicina basada en evidencias (MBE) se propone como el uso de la mejor evidencia científica disponible, la experiencia del profesional sanitario y los valores-circunstancias del paciente para la solución de sus problemas de salud 9,10. Este enfoque propone usar críticamente evidencia, con lo cual optimizaría los recursos informativos para la TD, reduciendo el riesgo de errores médicos, tanto para las decisiones automáticas en situaciones comunes como las deliberativas en las complejas.
En la Tabla 1 mostramos dos escenarios en la toma de decisiones del área de neurología vascular, en las cuales se usa tanto el sistema 1 como 2, luego de que la información es evaluada e integrada en los sistemas cognitivos del neurólogo tratante. Sin embargo, la alta tasa de producción científica obliga a contar con un enfoque que nos permita organizar y sintetizar la información para ser evaluada y utilizada.
Proponemos un enfoque “4E” desde la MBE que sistematice la evidencia de intervenciones (preventivas, diagnósticas o terapéuticas) para obtener decisiones eficaces, efectivas, eficientes y que promuevan equidad: Decisiones eficaces de intervenciones probadas en escenarios controlados (“paciente ideal”), de los ensayos clínicos aleatorizados (ECA). Decisiones efectivas en escenarios no controlados (“paciente real”), de los ensayos clínicos pragmáticos o estudios de “Real world” (ECP-RW). Decisiones eficientes donde se evalúen los beneficios en relación con sus costos, propio de las evaluaciones económicas (EE). Decisiones que promueven equidad cuando son recomendadas de acuerdo a las necesidades de cada paciente, evitando barreras económicas, geográficas o sociales; y se contienen en Guías de Práctica Clínica Basadas en Evidencia o Evaluaciones de Tecnología Sanitaría (GPC-BE/ETS) que usen una metodología estandarizada, como el Grading of Recommendations Assessment, Development and Evaluation (GRADE) (11), seguidas de un adecuado plan de implementación adaptado según un sistema de salud específico. (Figura 2).
Desarrollaremos cada etapa de este enfoque usando como ejemplo el caso de pacientes con ictus isquémico y el uso de trombólisis, resaltando la importancia de definir la población, intervenciones, controles y los desenlaces principales en la Tabla 2. Sin embargo, dada la amplitud de este enfoque podría a su vez ser aplicable en escenarios de investigación o en la TD en salud pública, para lo que se debería tener consideraciones como la constitución de equipos metodológicos y presupuestos específicos.
Tabla 2 Diseños de estudios para evaluar eficacia, efectividad, costo efectividad y promover equidad: ejemplos del área de enfermedad cerebrovascular.
| Estudio | Población | I/C | Desenlaces | Resultado principal (I/C) |
|---|---|---|---|---|
| Eficacia | ||||
| ECA: ECASS III (2008) (12) | Pacientes de 18-80 años con ictus isquémico moderado/severo (NIHSS<25) y TE entre 3-4,5 horas. | Alteplase 0.9 mg/kg (N=1515) vs. Placebo (N=1520) | Discapacidad ausente o leve (mRS 0-1) a los 90 días | mRS 0-1 a los 90 días: 52,4% vs 45,2% (RR: 1,16; IC95% 1,01-1,34; p=0,04) (a favor de la intervención). |
| RS: Wardlaw 2014 (13) | 10 estudios incluidos de pacientes con ictus isquémico por TC o RMN. | Cualquier trombolítico en cualquier dosis, por vía endovenosa o intraarterial (N=3483) vs Placebo u open control (N=3404) | Discapacidad ausente o leve (mRS 0-1) al finalizar seguimiento | mRS 0-1 al finalizar seguimiento: OR: 1,29; IC95% 1,16-1,43; Chi2=21,16; I2 =57%; p<0.00001 (a favor de la intervención)- |
| Efectividad | ||||
| Estudio de Real-world: Betts 2016 (14) Estudio de cohorte prospectiva | Pacientes de 18-80 años con al menos una hospitalización por ictus isquémico sin contraindicaciones para trombólisis | Trombólisis (N=513) vs no trombólisis (N=513) | Tiempo de independencia (mRS 0-2 a los 90 días) | Tiempo de independencia HR: 1,42; IC95% 1,17-1.71; p<0.001. (a favor de la intervención). |
| Eficiencia | ||||
| Araujo (2010) (15) Brasil Estudio Costo/Utilidad (Modelo de Markov) | Pacientes >18 años con ACVi | Trombólisis antes de las 3 horas vs. tratamiento conservador | QALY: Incapacidad por secuelas que comprometen la calidad de vida de pacientes post-ACVi en un año. | ICER: $28,956 por QALY ganado usando trombólisis vs. tratamiento conservador. Resultado costoefectivo (umbral de $29,100). |
| Promoviendo equidad | ||||
| GPC-BE (Sistema) | Población | I/C | Recomendación | |
| AHA-ASA 2018 (16) (AHA/ASA) | Pacientes de 18-80 años con ACVi moderado/severo (NIHSS<25) y TE entre 3-4,5 horas. | Trombólisis vs no trombólisis | -Trombólisis antes de las 3 horas Recomendación I Nivel de evidencia A -Trombólisis 3-4.5 horas Recomendación I Nivel de evidencia: B-R | |
| AUSTRALIAN GPC -STROKE (17) (GRADE) | Pacientes de 18-80 años con ACVi moderado/severo (NIHSS<25) y TE entre 3-4,5 horas. | Trombólisis vs no trombólisis | Para los pacientes con accidente cerebrovascular isquémico potencialmente incapacitante dentro de las 4.5 horas posteriores al inicio que cumplen con los criterios específicos de elegibilidad, la trombólisis intravenosa debe administrarse lo antes posible después del inicio del accidente cerebrovascular. (Recomendación fuerte) | |
| GPC ACV-IETSI 2018 (18) (GRADE) | Pacientes de 18-80 años con ACVi moderado/severo (NIHSS<25) y TE entre 3-4,5 horas. | Trombólisis vs no trombólisis | En pacientes con ACVi que cumplan criterios de elegibilidad, se recomienda usar trombólisis endovenosa inmediatamente dentro de las 4.5 h del inicio de síntomas. | (Recomendación fuerte a favor, calidad de evidencia: moderada ⊕⊕⊕⊝). |
(I/C: Intervención/Comparador); ECA: Ensayo clínico aleatorizado, ECASS: European Cooperatie Acute Stroke Study; NIHSS: National Institutes of Health Stroke Scale; mRS: Modified Rankin scale; RS: Revisión sistemática; TC: Tomografía computarizada; RMN: Resonancia Magnética nuclear; RR: Riesgo relativo; OR: Odds Ratio; HR: Hazard Ratio; QALY: Quality adjusted life years; ICER: Incremental cost-effectiveness ratio; CE: Costo-efectividad; GPC-BE: Guía de práctica clínica basada en evidencia; GRADE: Grading of Recommendations Assessment, Development and Evaluation)
Decisiones eficaces
Los ECA son estudios experimentales, donde los pacientes son seleccionados de acuerdo a estrictos criterios vigilando la adherencia y otros factores que pudiesen alterar la relación entre el tratamiento y los resultados a alcanzar (validez interna) (19). Se prefieren resultados terapéuticos críticos como reducir la morbi-mortalidad o mejorar la calidad de vida; y resultados importantes, pero no críticos (subrogados) como reducir la presión arterial o la glucemia que se asocian a objetivos críticos. También se prueban para objetivos secundarios, ni críticos ni importantes, como alivio de síntomas (ej. flatulencia) o cambios en medidas fisiológicas que revelan información importante o permite plantear nuevas hipótesis terapéuticas (20). Caso ECASS III (Tabla 2).
La eficacia terapéutica resulta de alcanzar los objetivos críticos o importantes en escenarios controlados donde los beneficios superan los daños (10). Se cuestiona que estos escenarios controlados difieren de la práctica asistencial donde se brinda atención a pacientes con comorbilidades y menor adherencia terapéutica (menor generalizabilidad). Se duda de sus resultados publicados por sesgos y conflicto de interés debido a sus financiamientos (21).
Decisiones efectivas
Los ECP-RW, experimentales controlados (EC pragmáticos) u observacionales prospectivos, se realizan para verificar los beneficios y riesgos de nuevas intervenciones que ya cuentan con autorización de entidades regulatorias. En escenarios de práctica asistencial real, incluyendo pacientes comórbidos, con potenciales factores confusores o riesgos de adherencia (mayor generalizabilidad)22. Caso Betts 2016 (Tabla 2).
La efectividad terapéutica en salud resultaría de alcanzar los objetivos propuestos en escenarios reales o menos controlados, donde las condiciones de atención son semejantes a los de la práctica asistencial. Estos estudios se complementan con los ECAS, pudiendo confirmar o contradecir la generalizabilidad de intervenciones eficaces, pero no efectivas.
Decisiones eficientes
Las EE comparan 2 alternativas de intervención en relación con sus beneficios y costos. Utilizan diferentes modelos matemático-econométricos (árboles de decisión, modelos de Markov, etc.), perspectivas temporales, de gasto (del médico, del paciente, de la institución o de la sociedad) y de contexto. Existen diferentes tipos de EE: costo-minimización, costo-efectividad, costo-utilidad, costo-beneficio 23 e incluso los análisis de impacto presupuestario para decidir si una intervención es financiable 24.
La costo-efectividad en salud resultaría de alcanzar los mejores resultados en salud a costos razonables, siendo su principal indicador la “razón de costo-efectividad incremental” (ICER, por sus siglas en inglés). Además de usarse como un indicador comparativo entre alternativas terapéuticas, el ICER puede compararse con un determinado umbral de costo-efectividad que cada país o institución estima concluyendo si una intervención es o no costo-efectiva. En pacientes con ictus isquémico, la trombólisis después de haber obtenido resultados eficaces y efectivos, el siguiente paso es evaluar si esa intervención es eficiente (Tabla 2).
Promoviendo equidad en salud
Las GPC-BE y ETS cuando se realizan bajo metodologías estandarizadas y transparentes (revisión sistemática, evaluación de calidad, síntesis de evidencia y sistema de formulación de recomendaciones) proponen recomendaciones de intervenciones eficaces, efectivas y/o costo-efectivas, que permiten guiar y estandarizar la práctica asistencial y sanitaria, promoviendo equidad en salud. Aunque no siempre se logra obtener las mejores evidencias para alcanzar estos tres objetivos, el estándar mínimo en las que las recomendaciones deben basarse es la seguridad y eficacia de las intervenciones. Cuando estas son de elevado costo, la realización de estudios de costo-efectividad es un paso necesario para formular recomendaciones 25.
Las GPC y ETS al promover el uso adecuado de intervenciones en salud, podrían mejorar los indicadores de morbimortalidad y reducir los gastos innecesarios de los sistemas sanitarios 26. Promueven la equidad al establecer criterios clínicos objetivos que permitan valorarse en cada paciente para decidir usar determinadas intervenciones sanitarias, y no excluirlos por barreras económicas, geográficas o culturales, o incluso debido a prácticas médicas arraigadas pero inadecuadas. Además, cuando son bien elaboradas incluyen la perspectiva de los pacientes y/o cuidadores. Finalmente, es importante un plan de implementación de GPC, ya que se necesita un análisis contextual e institucional para que las recomendaciones se logren aplicar. Recomendaciones sobre trombólisis son ya un consenso entre GPC neurológicas basadas en evidencia (Tabla 2).
Existen limitaciones que afectaría la aplicabilidad del enfoque 4E relacionadas a la poca disponibilidad de evidencia médica confiable para los diferentes contextos y realidades de cada país o localidad, además de la disposición del profesional de la salud para aplicar el esquema completo debido a aspectos relacionados con los tiempos de atención de los que se disponen en escenarios clínicos y de gestión. Sin embargo se podrían aplicar estrategias diferenciadas de acuerdo a los escenarios de toma de decisiones, ya sean clínicas o de salud pública. Estrategias de tipo educativas, uso de tecnologías de información o administrativas podrían hacer más factible su aplicación.
CONCLUSIONES
El uso del enfoque de MBE mejora el proceso de TD, tanto las automáticas (“sistema 1”) como las deliberativas (“sistema 2”). Permite reducir el riesgo de error al mejorar la elección de las alternativas terapéuticas, reducir la variabilidad asistencial, mejorar las decisiones sobre el financiamiento de tecnologías sanitarias y promover equidad.
Existen factores que dificultan su aplicación. Desde personales, como mantener prácticas rutinarias arraigadas pero inadecuadas; intereses económicos particulares al indicar terapias de menor eficacia y mayor costo; desconfianza infundada para usar GPC-BE/ETS. Hasta institucionales, limitado acceso a nuevas intervenciones por bajos presupuestos, gestiones ineficientes o prácticas asistenciales desactualizadas.
Es un paso clave contar con evidencias confiables de intervenciones de alta calidad, pero no suficiente para garantizar su incorporación y uso. También es importante promover una dinámica organizativa, institucional, y política en sistemas sanitarios para conseguir una cultura de lectura crítica de la evidencia, que permita una mejor atención de pacientes y una mejora de los indicadores de salud de cada país. Proponemos este enfoque para organizar el marco de información y tomar mejores decisiones, que guíen una práctica clínica y sanitaria que alcance las 4E: Eficacia, Efectividad, Eficiencia y Equidad.