Introducción
El hallazgo de tumores de distinta estirpe celular colisionando en un mismo órgano constituye una infrecuencia dentro de los reportes presentados. Liu et al., en el 2002 reportaron GIST gástrico y adenocarcinoma a la vez. Sin embargo, la aparición de un segundo tumor primario de origen epitelial como el adenomioma gastrointestinal, merece una explicación e investigación mayor; se han descrito la relación de GIST y adenocarcinomas gástricos y duodenales, bajo el concepto del complejo neuro-ectodermal-endodermo que existe a nivel de duodeno1,3.
Reporte del caso
Presentamos el caso clínico de una paciente mujer de 57 años de edad quien consulta por epigastralgia y sensación de llenura precoz, en el examen endoscópico (Figura 1). Presentó doble lesión submucosa en cuerpo en cara anterior de 25 a 30 mm, y otra en antro, a nivel de curvatura mayor tercio medio de 15 x 18 mm. Ambas sospechosas de leiomiomas. Las imágenes de TAC abdominal muestran: dos formaciones expansivas localizadas a nivel de cuerpo, en la cara anterior y antro gástrico, que captan ligeramente contraste de 35,4 x 24 x 23,18 mm (Figura 2) y 24,94 x 20,13 x 18 mm (Figura 3), cuyas características son compatibles con: a. Leiomioma, b. Tumor de GIST.
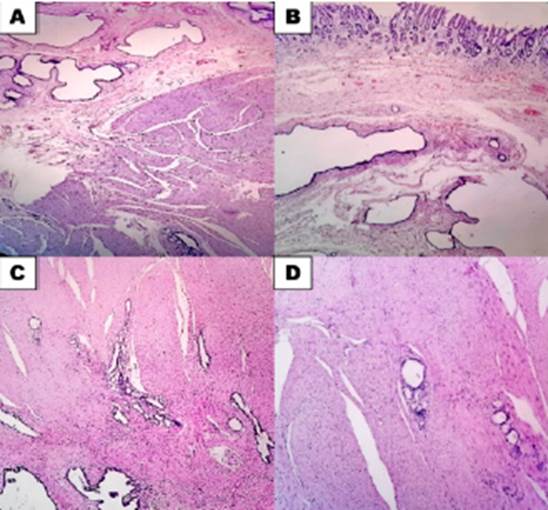
En el acto quirúrgico se confirmó las lesiones gástricas en cuerpo y antro y se realizó resección en cuña en ambos casos. Al estudio patológico, macroscópicamente se recibió dos nódulos de 3 cm de aspecto fibroso y el menor de 2cm, de aspecto fibroso con áreas microquísticas de 0.2cm. A la vista microscópica presentó patrón fusocelular, sin atipia, ni mitosis, ni necrosis, que fue positivo para c-kit, ki-67 4%, que correspondía a un tumor estromal gastrointestinal (GIST) de bajo grado (Figura 4). Y la segunda tumoración presentó tejido muscular liso con presencia de glándulas gástricas, y antrales, dilatadas en submucosa, y muscular propia (Figura 5). La paciente evolucionó favorablemente, sin complicaciones. Actualmente la paciente se encuentra en control oncológico siendo el GIST de bajo riesgo, se ha realizado estudios de endoscopia de control observando mucosa gástrica sin alteraciones, clínicamente paciente asintomática. Se programa control endoscopio anual, no se ha realizado control imagenologico.
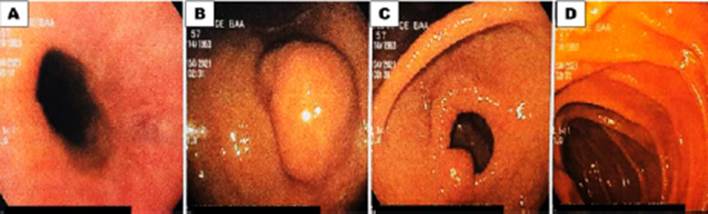
Figura 1 A. Eritema en cuerpo. B. Lesión submucosa en cuerpo. C. Lesión submucosa en antro. D. Eritema en duodeno.
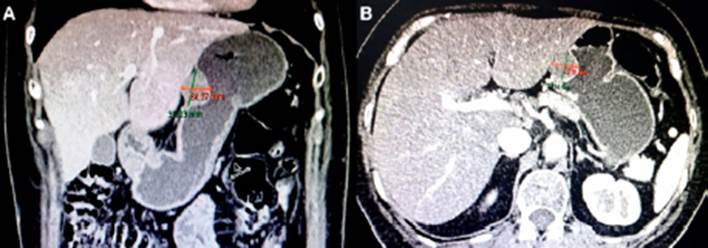
Figura 2 A y B. Se aprecia lesión sólida expansiva de bordes bien definidos, con cierta captación a la sustancia de contraste localizada en el cuerpo hacia la cara anterior, de 35.03 mm de diámetro cráneo-caudal x 24 mm de diámetro ántero-posterior x 23.18 mm de diámetro transversal.
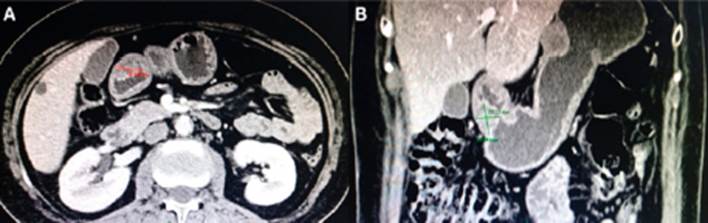
Figura 3 A y B. Se aprecia lesión en el antro gástrico con cierta captación a la sustancia de contraste, de bordes bien definidos, mide 24.94 mm de diámetro cráneo-caudal x 20.13 mm de diámetro ántero-posterior x 18mm de diámetro transversal.
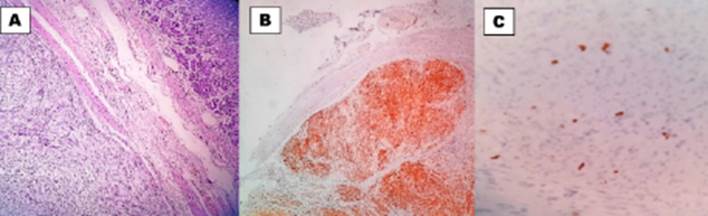
Figura 4 GIST intramuscular patrón fusocelular, HE 10X. B. CD 117 positivo, 10X. C. KI67 postiivo 4%, 40X.
Discusión
A nivel gastrointestinal, se han descrito asociación de tumores con hiperplasias submucosas de los plexos mioentéricos, GIST, carcinomas y carcinoides periampulares, y a veces feocromocitomas, así como paragangliomas duodenales4,5. Sin embargo, la asociación de GIST con adenomioma gástrico no está reportado.
Los GIST, derivan de las células intersticiales de Cajal, que controlan el peristaltismo gastrointestinal, morfológicamente se clasifican en fusiformes y epiteliales, una de las variantes que procede de los plexos entéricos son los tumores de los nervios autonómicos gastrointestinales (GANT). Los GIST pueden ser únicos o múltiples, pueden crecer hacia la luz, o hacia la serosa. Al corte presentan coloración oscura y carecen del patrón arremolinado de los leiomiomas y leiomiosarcomas. Puede contener áreas de hemorragia, la necrosis puede estar asociada a crecimiento mayor y de alto riesgo de metástasis, al microscopio presentan patrón fusiforme y epitelioide o mixtas, la actividad mitótica es variable, la mayor parte 90% son positivas para c-KIT. El c-KIT es el receptor del factor de célula madre, y el PDGFRA es un receptor del factor de crecimiento derivado de las plaquetas (PDGF), se sabe que el 85% de los GIST tienen mutaciones de c-KIT y el 35% de los GIST con c-KIT normal tienen mutaciones de PDGFRA, y tanto el c-KIT como el PDGFRA tienen tirosincinasa citoplásmicas que activan vías intracelulares similares. Estas señales favorecen la proliferación celular e inhibe la apoptosis, las mutaciones de c-KIT y las de PDGFRA parecen ser mutuamente excluyentes6,7.
El adenomioma gástrico es una tumoración benigna rara, constituida por tejido muscular hipertrofiado con presencia de glándulas sin atipia intramusculares8. En 1903, Magnus-Alsleben, reportaron cinco casos de tumores mioepiteliales(9, 10). A los adenomiomas gástricos e intestinales, en la literatura se los ha denominado de diferente maneras, como hematomas mioepitelial, mioglandular, adenomiomatoso, algunos autores consideran como parte de la heterotopía pancreática; sin embargo, la diferenciación glandular aleja el origen pancreático11. Se presenta en cualquier grupo etario, más frecuente en la cuarta y quinta década de la vida. Con presentación gástrica prevalente seguida de intestino delgado y grueso. Asociado a Gastritis quística profunda, como causa de una diverticulosis polipoidea11.
La colisión o sincronismo de dos tumores de diferente estirpe celular en un mismo órgano es infrecuente; se han descrito tumores sincrónicos y metacrónicos, con GIST gástricos y carcinoma neuroendocrino12, así como sincrónicos de linfomas y GIST gástricos13. Sin embargo, la asociación de GIST y adenomioma no ha sido descrita. El componente glandular en un GIST, figura en casos excepcionales14, así como su comportamiento maligno.
La presencia de tumores como neurofibromas y carcinoides en el tubo gastrointestinal tienen bases embriológicas descritas por Von Capenhout y mencionado por Klein en 1989, bajo la hipótesis del origen embriológico de las células en el complejo neuroectodermal-endodermal, que comparte las estirpes neurales, endocrinas, y epiteliales esta hipótesis es base también para suponer el origen epitelial de los adenocarcinomas asociados a NF14. Rara vez los GIST forman parte de un síndrome tumoral como la triada de Carney (GIST gastrointestinal, paraganglioma y condroma pulmonar)15.
Conclusión
Los GIST pueden estar asociados a diferentes tumores ya sea de origen epitelial o neural, así como a tumores mesenquimales mixtos como el adenomioma gástrico, el componente glandular también puede formar parte de la clasificación de GIST aún no descrita, debemos tener presente las diferentes presentaciones y asociaciones de tumores GIST.