Introducción
El HTLV-1 causa diversos síndromes clínicos, pero los más graves son una enfermedad hematológica agresiva la leucemia/linfoma de células T del adulto (LLTA) y una afección neurológica la paraparesia espástica tropical (1.
Los países a nivel mundial que muestran áreas con alta endemicidad al HTLV-1 son Guinea, Zaire, Gabón, Japón, la cuenca del Caribe, Irán, Melanesia y Australia 1; en Sudamérica destacan Brasil, Perú, Chile, Argentina y Colombia. Estos países sudamericanos realizan el cribado del virus en sus bancos de sangre y previenen su transmisión en la transfusión sanguínea 1 pero solamente Brasil 2,3 y Chile 4 han implementado un protocolo o guía de atención de pacientes con HTLV-1 para contrarrestar la transmisión vertical y sexual 2-4.
En Perú las muestras de los pacientes con diagnóstico presuntivo al HTLV-1 son tamizadas por Ensayo Inmunoabsorción ligado a enzimas (ELISA) 5 y las de donantes de sangre por quimioluminiscencia (CLIA) o electroquimioluminiscencia (ECLIA) 6, las muestras reactivas son confirmadas por Inmunofluorescencia Indirecta (IFI) o Inmunoblot 5.
Murex (fabricación italiana) 7 y Wantai (fabricación China) 8 fueron las dos marcas comerciales de ELISA HTLV-1/2 más usadas en la vigilancia peruana del bienio 2020 20215. El rendimiento diagnóstico reportado en sus insertos de ambas marcas, destacan un 100% de sensibilidad y un 99,9% de especificidad 7,8, sin embargo, lo ideal es evaluar el rendimiento en el país donde se usan los kits y así proveer de datos más cercanos a la realidad con la finalidad de elegir un kit con mejor desempeño 9.
La IFI que se usa para la confirmación de anticuerpos anti HTLV-1 es una prueba in house elaborada y validada por el Instituto Nacional de Salud (INS) de Perú y su principal ventaja radica en que tiene un costo seis veces menor que el Inmunoblot (10 versus 60 dólares por cada ensayo) (10,11. La validación de la IFI-HTLV-1 de INS-Perú mostró una sensibilidad de 98,8% y una especificidad de 98,7%, siendo una limitante que en dicho estudio no se evaluó la prueba frente a muestras de pacientes con diagnóstico presuntivo a HTLV-1/2 y tampoco se evaluó el tiempo de estabilidad de las láminas IFI que contenían la impregnación de las líneas celulares MT2 (linfocitos infectados con HTLV-1) y la línea celular K562 (macrófagos no infectados: control) 10.
Con la finalidad de mejorar o aportar más a los estudios descritos, se propuso como objetivo determinar el rendimiento de tres pruebas serológicas ELISA Murex, ELISA Wantai e IFI INS-Perú para la detección de anticuerpos anti HTLV-1 frente a muestras peruanas.
El estudio
Se realizó un estudio observacional prospectivo de evaluación de prueba diagnóstica durante enero de 2022. El tamaño de muestra fue elegido por conveniencia y fue de 405 sueros procedentes de la seroteca de HTLV del Laboratorio de Referencia Nacional de Virus de Transmisión Sexual (LRN VTS) del INS de Perú, correspondiendo al total de muestras de suero de personas con diagnóstico presuntivo a HTLV-1/2 que fueron enviadas al INS por los diversos establecimientos del Ministerio de Salud para su descarte o confirmación de HTLV-1/2 mediante la prueba Inmunoblot de la marca Fujirebio entre el 1 de enero y el 31 de diciembre de 2021; se excluyeron 23 muestras: 4 por volumen insuficiente y 19 por no ser positivo ni negativo a HTLV-1 (Indeterminado: once; HTLV-2: cinco; HTLV no tipificable: tres).
Finalmente, se estudiaron 382 sueros, de los cuales fueron 215 positivos y 167 negativos a HTLV-1, siendo inmunoblot la prueba de referencia o Estándar de oro (Fujirebio, Bélgica. “INNO-LIA HTLV I/II”; sensibilidad: 100%, especificidad: 99 a 99,7%; capacidad de diferenciación: 98,8%) 11.
Los 215 sueros positivos a HTLV-1 procedieron de pacientes de los siguientes departamentos del Perú: Lima (90), Apurímac (27), Junín (25), Ayacucho (21), Cusco (15), La Libertad (14), Arequipa (6), Lambayeque (5), San Marín (5), Huancavelica (3), Cajamarca (1), Loreto (1), Madre de Dios (1) y Tacna (1). Como dato importante señalamos que de las 90 muestras que procedieron de Lima, 73 de ellas fueron enviadas por el Instituto Nacional de Enfermedades Neoplásicas (nosocomio especializado que maneja pacientes con LLTA).
Los 382 sueros fueron procesados por las tres pruebas serológicas: Murex ELISA HTLV 1/2 7, Wantai ELISA HTLV-1/28 e IFI-HTLV-1 de INS-Perú 10 (fecha de preparación de las láminas IFI: octubre 2018; lote: 0618). Los ensayos de ELISA fueron realizados de acuerdo a las instrucciones del fabricante (inserto) 7,8 y el de IFI de acuerdo a lo descrito en su metodología estandarizada y validada 10.
Con la finalidad de verificar los resultados falsos positivos y falsos negativos obtenidos en alguna de las tres pruebas serológicas, se realizó la reevaluación de dichas muestras; asimismo, las muestras también fueron nuevamente procesadas por la Prueba de Referencia de Inmunoblot para verificar su veracidad.
El análisis estadístico se estimó haciendo uso de una tabla de contingencia, el programa Epidat v3.1 y Excel. Se informó los parámetros de exactitud diagnóstica: Sensibilidad, Especificidad, Índice de validez, Valor predictivo positivo (VPP), Valor predictivo negativo (VPN) e Índice de Youden considerando un nivel de confianza de 95% (IC 95%).
No se estimó los parámetros de la repetibilidad, reproducibilidad y límite de detección de las pruebas en estudio por razones de presupuesto limitado, sin embargo, se destaca que la repetibilidad y reproducibilidad de la prueba IFI-HTLV-1 de INS-Perú el 2017 mostró un 100% de concordancia al ser evaluada en cinco regiones peruanas 10.
Todas las muestras fueron decodificadas y anonimizadas sin acceso a la identificación de pacientes; las muestras procedieron de una seroteca que correspondieron a pacientes que fueron atendidos por el diagnóstico presuntivo a HTLV-1/2 y forman parte de la vigilancia en salud pública del HTLV. El estudio se realizó en el marco de las actividades regulares del Instituto Nacional de Salud.
Hallazgos
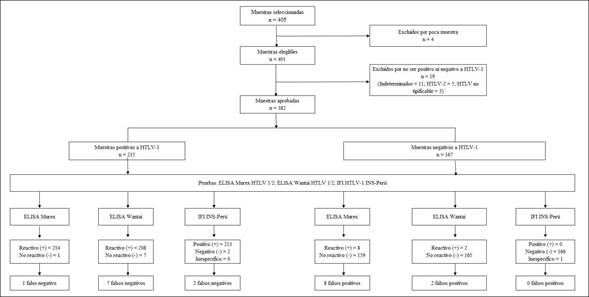
La prueba IFI HTLV-1 de INS-Perú no presentó ningún falso positivo y sólo presentó dos falsos negativos; además, ELISA Wantai fue la marca que obtuvo más falsos negativos (siete), mientras que ELISA Murex fue la marca que obtuvo más falsos positivos (ocho) (Figura 1).
Las dos muestras de los dos falsos negativos que presentó IFI HTLV-1 INS-Perú fueron identificadas correctamente (positivo) por las marcas ELISA Murex y Wantai.
La única muestra que dio falso negativo a ELISA Murex, también dio falso negativo a ELISA Wantai, pero si fue identificado correctamente (positivo) por IFI HTLV-1 INS-Perú.
Las dos muestras que dieron falsos positivos a ELISA Wantai, también dieron falsos positivos a ELISA Murex, pero si fueron identificadas correctamente (negativo) por IFI HTLV-1 INS-Perú.
Otros hallazgos importantes mostraron que la prueba de IFI HTLV-1 INS-Perú y ELISA Murex tuvieron una sensibilidad superior a ELISA Wantai; también la prueba con mejor especificidad y mejor índice de validez fue IFI HTLV-1 INS-Perú. Asimismo, el índice de Youden de las tres pruebas serológicas evaluadas fue igual o superior a 0.95, lo cual nos confirma que la posibilidad de tener falsos positivos o negativos es baja (Tabla 1).
Tabla 1 Resultados de los parámetros evaluados de las tres pruebas serológicas para la detección de anticuerpos anti HTLV-1
| PARÁMETROS | ELISA Murex | ELISA Wantai | IFI INS-Perú | |||
|---|---|---|---|---|---|---|
| Valor | (IC 95%) | Valor | (IC 95%) | Valor | (IC 95%) | |
| Sensibilidad (%) | 99,5 | (98,4 - 100,0) | 96,7 | (94,1 - 99,4) | 99,1 | (97,6 - 100,0) |
| Especificidad (%) | 95,2 | 91,7 - 98,8) | 98,8 | (96,9 - 100,0) | 99,4 | (97,9 - 100,0) |
| Índice de validez (%) | 97,6 | (96,0 - 99,3) | 97,6 | (96,0 - 99,3) | 99,2 | (98,2 - 100,0) |
| Valor predictivo + (%) | 96,4 | (93,7 - 99,1) | 99,1 | (97,5 - 100,0) | 99,5 | (98,4 - 100,0) |
| Valor predictivo - (%) | 99,4 | (97,8 - 100,0) | 95,9 | (92,7 - 99,2) | 98,8 | (96,9 - 100,0) |
| Índice de Youden | 0,95 | (0,91 - 0,98) | 0,96 | (0,93 - 0,98) | 0,98 | (0,97 - 1,00) |
Se destaca que la prueba de IFI HTLV-1 INS-Perú obtuvo resultados superiores de sensibilidad y especificidad frente a los valores reportados en su estandarización, mientras que las otras dos pruebas serológicas evaluadas tuvieron resultados inferiores a los valores reportados por los fabricantes (Tabla 2).
Tabla 2 Resultados de la sensibilidad y especificidad de las tres pruebas serológicas para la detección de anticuerpos anti HTLV-1 frente a los valores reportados por los fabricantes y por otros países
| Evaluación del estudio | Reporte de los fabricantes | Reporte de Argentina | Reporte de Brasil | Reporte de Ecuador | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| ELISA Murex | ELISA Wantai | IFI INS-Perú | ELISA Murex | ELISA Wantai | IFI INS-Perú | ELISA Murex | IFI Argetina | ELISA Murex | IFI Ecuador | |
| Sensibilidad (%) | 99,5 | 96,7 | 99,1 | 100,0 | 100,0 | 98,8 | 100,0 | 97,9 | 100,0 | 100,0 |
| Especificidad (%) | 95,2 | 98,8 | 99,4 | 99,9 | 99,9 | 98,7 | 98,0 | 100,0 | 92,0 | 100,0 |
Discusión
El estudio demostró un alto rendimiento diagnóstico de la prueba IFI HTLV-1 de INS-Perú; sus valores de sensibilidad y especificidad fueron semejantes a resultados anteriores en Perú 10 y también a estudios realizados en Argentina, 97,9% sensible y 100,0% específico 12. No hubo falsos positivos a la prueba de IFI HTLV-1 en ninguno de estos estudios ni en la presente evaluación, asegurándonos la utilidad como prueba confirmatoria para la detección de anticuerpos contra HTLV-1 10,12.
La prueba de IFI no está disponible como marca comercial, es por ello que países como Brasil 3, Chile 4, Perú 10, Argentina 12 y Ecuador 13 cultivan la línea celular MT2 y la línea celular K562 para preparar sus propias láminas y su kit in house; un valor agregado en ésta evaluación es que se usó el lote de láminas preparadas el 2018 y siendo conservadas a -70 °C hasta la fecha del procesamiento (enero, 2022) mostraron muy buenos resultados, en consecuencia se concluye que el tiempo de la estabilidad de las láminas de IFI HTLV-1 INS-Perú tendrían una vigencia útil de hasta tres años.
El 100 % de sensibilidad reportada por el fabricante de la marca Murex ELISA HTLV 1/2 (Italia) 7 es similar a la que obtuvieron países como Brasil 100% (170/170) 14 y Argentina 100% (74/74) 15. Nuestro resultado para éste parámetro que usó un número más robusto de muestras positivas fue de 99,5% (214/215), a pesar que se tuvo un falso negativo la sensibilidad alcanzada fue comparable a los estudios señalados. En ésta marca se obtuvo 8 falsos positivos y 95,2% (159/167) de especificidad, la cual difiere con lo reportado por el fabricante (99.9%) 7 y al de otros estudios realizados en Brasil (92%) 14 y Argentina (98%) 15. Sin embargo, su utilidad no se vería afectada por ser una prueba de tamizaje.
Distintas y numerosas investigaciones de varios países emplean la marca Murex ELISA HTLV 1/2 para realizar estudios epidemiológicos en población de donantes de sangre 16, nativos 17, áreas de alta y baja endemia 14,15,18. Los resultados de sus parámetros que hallamos en la evaluación frente a muestras peruanas, la hacen posicionarla como una buena candidata de prueba de tamizaje para Perú.
Para la marca Wantai ELISA HTLV 1/2, la especificidad tuvo resultado acorde, pero el valor de la sensibilidad fue significativamente inferior al reportado por el fabricante, 96,7% versus 100,0% 8; una investigación previa en Perú reportó una sensibilidad de 99,2% (122/123) 9, atribuyéndole un falso negativo frente a los siete falsos negativos que hallamos. Siendo las pruebas de ELISA usadas como tamizaje, lo ideal es que presenten la máxima sensibilidad (100%) para no tener falsos negativos y dejar de diagnosticar sujetos infectados.
La marca Wantai para pruebas de ELISA es muy usada en distintas investigaciones de diferentes países para detectar anticuerpos de diferentes infecciones virales, sin embargo, es escasamente usada para HTLV-1/2 (búsqueda realizada en Scielo, Pubmed y Scopus), probablemente por tener una menor sensibilidad de la prueba diagnóstica 9,19
La discordancia entre los resultados de las pruebas ELISA, podrían estar relacionados al origen y cantidad de antígenos de HTLV-1/2 que utilizan los fabricantes en la producción de sus kits 9,10.
Una limitante fue no haber evaluado sueros positivos a HTLV-2, debido a que sólo hubo disponible cinco casos de HTLV-2, los cuales fueron excluidos del estudio. Otra limitación fue que no se evaluaron otras marcas de ELISA, anteriormente se usaba con frecuencia la marca Biokit Bioelisa 9,20 pero se descontinuó su producción. Una última limitación fue no contar con insumos biológicos para la prueba molecular PCR HTLV-1 (20, 21), por lo que no se logró definir el estado definitivo de los once pacientes que dieron resultados Indeterminados al Inmunoblot y que fueron excluidos del estudio.
De acuerdo a los resultados, concluimos que la marca Murex ELISA HTLV 1/2 y la prueba IFI HTLV-1 INS-Perú tuvieron resultados satisfactorios con buen rendimiento diagnóstico para la detección de anticuerpos contra HTLV-1 y son buenos candidatos para continuar siendo utilizados en Perú.