Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Ginecología y Obstetricia
versión On-line ISSN 2304-5132
Rev. peru. ginecol. obstet. v.58 n.4 Lima 2012
ARTÍCULO ORIGINAL
Maduración in vitro de ovocitos: alternativa efectiva en reproducción asistida
In vitro maturation of oocytes: effective alternative in assisted reproduction
Luis Vargas Tominaga1,a; Ricardo Pella Cáceres1,b; Alberto Vargas Lechuga1,a; Livia Bartolo Durán1,c
1 Centro de Fertilidad y Ginecología del Sur
a Médico Ginecólogo-Obstetra
b Biólogo con mención en Genética
c Bióloga
Trabajo ganador del Segundo Premio de los Temas Libres presentados al XIX Congreso Peruano de Obstetricia y Ginecología, 27 al 30 de noviembre de 2012.
Resumen
Objetivos: Determinar la efectividad de la maduración in vitro (MIV) de ovocitos, como método de reproducción asistida. Diseño: Estudio descriptivo. Institución: Centro de Fertilidad y Ginecología del Sur (CFGS), Cusco, Perú. Participantes: Mujeres con diagnóstico de infertilidad. Intervenciones: Fueron ocho mujeres en las que se realizó MIV de ovocitos, seguido de ICSI, cultivo y vitrificación de embriones. Posteriormente, se preparó el endometrio de las pacientes y se realizó descongelación y transferencia de embriones. Principales medidas de resultados: Tasas de maduración de ovocitos, de fecundación, de embarazo clínico y de implantación. Resultados: La tasa de maduración de ovocitos fue 82,1%, de fecundación 95,7%, de embarazo clínico 62,5% y de implantación 29,4%. Conclusión: La MIV de ovocitos es una alternativa efectiva en reproducción asistida.
Palabras clave: Maduración in vitro de ovocitos, fertilización in vitro, inyección intracitoplasmática de espermatozoides.
Abstract
Objectives: To determine the effectiveness of in vitro maturation (IVM) of oocytes in assisted reproduction. Design: Descriptive study. Setting: Centro de Fertilidad y Ginecología del Sur (CFGS), Cusco, Peru. Participants: Women with diagnosis of infertility. Interventions: In eight women we performed IVM of oocytes, followed by ICSI, culture and vitrification of embryos. Thereafter, patients endometrium was prepared and the embryos were thawed and transferred. Main outcome measures: Maturation of oocytes, fertilization, clinical pregnancy and implantation rates. Results: Maturation of oocytes rate was 82.1%, fertilization rate 95.7%, clinical pregnancy 62.5% and implantation rate 29.4%. Conclusion: IVM of oocytes is an effective alternative in assisted reproduction.
Key words: In vitro maturation of oocytes, in vitro fertilization, intracytoplasmic sperm injection.
INTRODUCCIÓN
La fertilización in vitro (FIV) es un procedimiento utilizado cada vez con mayor frecuencia en el manejo de parejas con infertilidad. Para incrementar la posibilidad de embarazo a través de FIV, se asocia al uso de inductores de ovulación con el objetivo de lograr mayor número de ovocitos y, por consiguiente, de embriones en cultivo.
La inducción de ovulación permite la maduración in vivo de ovocitos. Sin embargo, este mismo proceso de maduración puede ser logrado in vitro. La maduración in vitro (MIV) de ovocitos consiste en obtener ovocitos inmaduros (en estadio de vesícula germinal) de folículos ováricos antrales sin estimulación, o mínimamente estimulados con gonadotropinas, para luego ser madurados bajo condiciones de laboratorio en medios de cultivo suplementados con hormonas. Esta técnica permite obtener ovocitos en metafase II, a fin de poder ser fecundados.
La MIV fue propuesta, en 1935, por Pincus y Enzmann(1), y más tarde por Edwards, en 1969(2). En 1991, Cha logró el primer embarazo por medio de esta técnica(3). Al no ser necesaria la estimulación con dosis altas de gonadotropinas, como en la FIV convencional, la MIV de ovocitos es ideal para pacientes con ovarios poliquísticos (OP), debido a su difícil respuesta a la estimulación y al riesgo de síndrome de hiperestimulación ovárica. Sin embargo, esta técnica puede brindar una alternativa real a pacientes con infertilidad asociada a otros factores. El presente describe la experiencia en el manejo de ocho casos por medio de MIV.
MÉTODOS
Desde octubre de 2011 a agosto de 2012, se realizó MIV de ovocitos en ocho mujeres con diagnóstico de infertilidad. Los procedimientos fueron realizados en el Laboratorio de Embriología del Centro de Fertilidad y Ginecología del Sur, en la ciudad de Cusco, a 3 330 m.s.n.m. Las pacientes procedían de las regiones de Cusco, Apurímac, Puno y Madre de Dios.
Las características de las pacientes son descritas en la tabla 1. Se define OP ante un recuento de folículos mayor a 12 (entre 2 y 9 mm), en uno o ambos ovarios(4, 5).
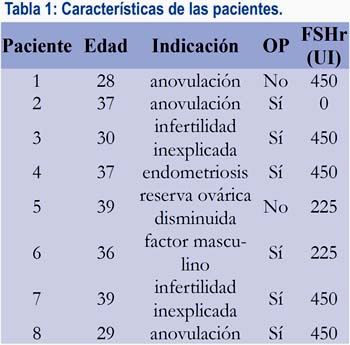
Se administró entre 75 y 150 UI de FSHr por 3 días consecutivos, entre el segundo y quinto día del ciclo (una de las pacientes no utilizó gonadotropinas). No se administró hCG. Entre el sexto y octavo día del ciclo, se realizó aspiración folicular bajo sedación endovenosa, utilizando aguja de 18 de un solo lumen (Vitrolife) o aguja de aspiración de ovocitos inmaduros (Cook).
Los complejos cúmulo-ovocitos (CCO) fueron cultivados en medio de maduración conteniendo 75 mUI/mL de FSHr y 100 mUI/mL de hCG (Pregnyl, Schering-Plough), suplementado al 10% con suero inactivado de la paciente; 36 horas después, los CCO fueron evaluados y los ovocitos en metafase II fueron inseminados mediante inyección intracitoplasmática de espermatozoides (ICSI) y cultivados en medio global (LifeGlobal). Dieciocho horas después del ICSI se evaluó la fecundación de los ovocitos, manteniéndolos en el mismo medio por 24 horas más.
Como existía un desfase entre el desarrollo embrionario y el endometrial, se realizó congelación de los embriones por vitrificación(6), en el dispositivo McGill Cryoleaf (Origio), y fueron almacenados en nitrógeno líquido.
Entre 45 y 60 días después, iniciando la menstruación, se utilizó dosis progresivamente ascendentes de valerato de estradiol, vía oral, desde 2 mg hasta 12 mg diarios, logrando un grosor endometrial por encima de 8 mm. Se adicionó 200 mg de progesterona micronizada (Utrogestan, Ferring, o Geslutin PNM, Tecnofarma) y 90 mg de gel de progesterona (Crinone 8%, Merk-Serono) diario, ambos por vía vaginal, o la asociación de 600 mg de progesterona micronizada y la aplicación de anillo vaginal de progesterona (Fertiring, ABL Pharma).
Los embriones fueron descongelados y cultivados por 24 horas. Luego, transferidos a la cavidad uterina, utilizando un catéter Frydman Ultrasoft (Laboratorio CCD), bajo guía de ultrasonido abdominal.
Trece días después de la transferencia, se realizó dosaje de β-hCG. En caso de presentar dosaje positivo, se hizo ultrasonido vaginal en una y dos semanas posterior a la prueba, para evidenciar presencia de saco gestacional y de actividad cardiaca en el embrión.
RESULTADOS
La tabla 2 describe el desarrollo de ovocitos y embriones.

La tabla 3 describe los resultados de embarazo y su evolución. El primer bebe de esta serie fue una niña que nació el 7 de agosto de 2012, con un peso de 1 800 gramos, a las 36 semanas de gestación, por cesárea de emergencia, debido a sufrimiento fetal asociado a oligohidramnios y restricción de crecimiento intrauterino (RCIU), en paciente con antecedentes de anovulación, amenorrea y anorexia nervosa(7).

Actualmente, una segunda paciente lleva gestación progresiva de 30 semanas sin complicaciones, y una tercera paciente progresa una gestación de nueve semanas.
Dos pacientes que cursaban con gestación activa, tuvieron desaparición de actividad cardiaca embrionaria en la octava semana de gestación.
DISCUSIÓN
El número de ovocitos obtenidos por aspiración fue 3,5 en promedio. Sin embargo, a pesar del número limitado de ovocitos, las tasas de maduración, fecundación y clivaje fueron altas, así como las tasas de embarazo clínico e implantación.
A pesar de comunicaciones que manifiestan la ventaja de la administración de hCG previa a la obtención de ovocitos(8-11), también se ha manifestado que la hCG interrumpe la comunicación entre las células foliculares y el ovocito, evento importante para la adquisición de un adecuado potencial de desarrollo embrionario(12). En nuestro protocolo de MIV no utilizamos hCG in vivo; hacemos madurar completamente los ovocitos in vitro, sometiéndolos a la presencia de FSH y hCG en el medio de cultivo, habiéndose encontrado resultados satisfactorios con esta estrategia(13). La ventaja de combinar MIV de ovocitos con la vitrificación es la de posponer la transferencia embrionaria cuando el endometrio esté suficientemente receptivo.
El desarrollo de oligohidramnios y RCIU se encuentra relacionado a posibles factores inmunológicos asociados al diagnóstico de anovulación y amenorrea de la madre. El desarrollo de aborto en dos de las pacientes con gestación clínica puede estar asociado al diagnóstico de ovario poliquístico, así como a factores intrínsecos por la edad (37 y 38 años, respectivamente). Es decir, complicaciones desarrolladas no por el procedimiento de MIV de ovocitos, sino relacionadas a características propias de las pacientes.
La MIV de ovocitos se constituye como una alternativa adicional a los procedimientos convencionales de reproducción asistida, no solo en mujeres con disfunción ovulatoria o con condición de ovarios poliquísticos, sino para cualquier pareja con diagnóstico de infertilidad. La MIV de ovocitos les brinda una alternativa interesante al lograr la maduración de ovocitos en solo 36 horas, a diferencia de los diferentes protocolos de inducción de ovulación, que pueden requerir dosis elevadas y prolongadas, y en algunos casos, enfrentarnos tanto a situaciones de resistencia al uso de los inductores de ovulación o a síndrome de hiperestimulación ovárica, o simplemente como una alternativa más confortable para la paciente.
Referencias Bibliográficas
1. Pincus G, Enzmann EV. Can mammalian eggs undergo normal development in vitro? Proc Natl Acad Sci USA. 1934;20(2):121-2.
2. Edwards RG, Bavister BD, Steptoe PC. Early stages of fertilization in vitro of human oocytes matured in vitro. Nature. 1969;221(5181):632-5.
3. Cha KY, Koo JJ, Ko JJ, Choi DH, Han SY, Yoon TK. Pregnancy after in vitro fertilization of human follicular oocytes collected from nonstimulated cycles, their culture in vitro and their transfer in a donor oocyte program. Fertil Steril. 1991;55:109–13.
4. Pacheco, J. Manejo del síndrome de ovario poliquístico en la mujer infértil. Notas recientes sobre el Consenso de Thessaloniki. Rev peru ginecol obstet. 2008;54:143- 8.
5. Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group. Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome. Fertil Steril. 2004;81(1):19-25.
6. Kuwayama M, Vajta G, Ieda S, Kato O. Comparison of open and closed methods for vitrification of human embryos and the elimination of potential contamination. Reprod Biomed Online. 2005;11:608-14.
7. Vargas-Tominaga L, Pella-Cáceres R, Vargas-Lechuga A, Bartolo-Durán L. Embarazo mediante tratamiento de maduración in vitro de ovocitos en paciente amenorreica y con historia de anorexia nervosa. Rev peru ginecol obstet. 2012;58:133-6.
8. Son WY, Chung JT, Herrero B, Dean N , Demirtas E, Holzer H, Elizur S, Chian RC, Tan SL. Selection of the optimal day for oocyte retrieval based on the diameter of the dominant follicle in hCG-primed in vitro maturation cycles. Hum Reprod. 2008;23(12):2680-5.
9. Tan SL, Child TJ. In vitro maturation of oocytes from unstimulated polycyctic ovaries. Reprod Biomed Online. 2002;4 Suppl 1:18-23.
10. Son WY, Chung JT, Dermitas E, Holzer H , Sylvestre C, Buckett W, Chian RC, Tan SL. Comparison of in-vitro maturation cycles with and without in-vivo matured oocytes retrieved. Reprod Biomed Online. 2008;17(1):59- 67.
11. Chian RC. In-vivo maturation of immature oocytes for infertile women with PCOS. Reprod Biomed Online. 2004;8:547-52.
12. Albertini DF, Combelles CM, Benecchi E, Carabatsos MJ. Cellular basis for paracrine regulation of ovarían follicle development. Reproduction. 2001;121:647-53.
13. De Vos M, Ortega-Hrepich C, Albuz FK, Guzman L, Polyzos NP, Smitz J, Devroey P. Clinical outcome of non hCGprimed oocyte in vitro maturation treatment in patients with polycystic ovaries and polycyctic ovary syndrome. Fertil Steril. 2011;96(4):860-4.
Correspondencia:
Dr. Luis Vargas Tominaga
Urbanización Mariscal Gamarra B-11
Segunda Etapa, Cusco, Perú
Correo electrónico: tominaga@fertilidadcusco.com.pe
El material no ha sido presentado anteriormente a ningún medio de publicación.
Financiamiento propio.
No existe conflicto de interés en ninguno de los autores.













