Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Ginecología y Obstetricia
versión On-line ISSN 2304-5132
Rev. peru. ginecol. obstet. vol.60 no.4 Lima oct./dic. 2014
SIMPOSIO PREECLAMPSIA, VIEJO PROBLEMA AÚN NO RESUELTO: CONCEPTOS ACTUALES
Manejo de la preeclampsia/eclampsia en el Perú
Treatment of preeclampsia/eclampsia in Peru
Enrique Guevara Ríos 1,2,3, Luis Meza Santibáñez 2,4,5
1 Médico Gineco-Obstetra, Jefe del Servicio de Emergencia del Instituto Nacional Materno Perinatal, Lima, Perú.
2 Docente de la Facultad de Medicina de la Universidad Nacional Mayor de San Marcos, Lima, Perú.
3 Miembro Asociado de la Sociedad Peruana de Obstetricia y Ginecología, Perú.
4 Médico Gineco-Obstetra, Médico Asistente del Servicio de Obstetricia C del Instituto Nacional Materno Perinatal, Lima, Perú.
5 Miembro Titular de la Sociedad Peruana de Obstetricia y Ginecología, Perú.
RESUMEN
La preeclampsia es una enfermedad del embarazo que afecta a la madre y al feto, siendo responsable de una proporción considerable de muertes maternas y perinatales. Complica de 3 a 22% de los embarazos y es la segunda causa de muerte materna en el Perú, con 32%, y la primera causa de muerte materna en el Instituto Nacional Materno Perinatal, con 43%. Se hace una revisión de los nuevos aportes en el manejo de la preeclampsia severa y eclampsia y de una de sus complicaciones más graves, como es la rotura hepática.
Palabras clave: Preeclampsia, eclampsia, sindrome HELLP.
ABSTRACT
Preeclampsia is a disease of pregnancy that affects mother and fetus and is responsible for a considerable proportion of maternal and perinatal deaths. It complicates 3 to 22% of pregnancies and is the second leading cause of maternal death in Peru with 32%, as well as the leading cause of maternal death at the National Maternal Perinatal Institute with 43%. A review of new contributions on severe preeclampsia and eclampsia management and treatment of one of its most serious complications liver rupture are done.
Keywords: Preeclampsia, eclampsia, HELLP syndrome.
INTRODUCCIÓN
La preclampsia es una enfermedad de carácter progresivo e irreversible que afecta múltiples órganos(1), siendo responsable de una proporción considerable de muertes maternas y perinatales. Complica de 3 a 22% de los embarazos(2). En el Perú, su incidencia fluctúa entre 10 y 15% en la población hospitalaria(3). La incidencia de la enfermedad hipertensiva del embarazo es mayor en la costa que en la sierra, pero la mortalidad materna por esta causa es mayor en la sierra; no parecen existir diferencias mayores entre las características de esta enfermedad en ambas regiones(4). En el Perú, es la segunda causa de muerte materna, con 32%(5). En la Dirección de Salud de Lima Ciudad es la primera causa de muerte, entre los años 2000 a 2009, con 33%. En el Instituto Nacional Materno Perinatal es también la primera causa de muerte materna, entre los años 2003 y 2013, con 43%(5). Durante 2013, se atendió un total de 16 972 partos, de los cuales 1 427 (8,4%) estuvieron complicados con problemas de hipertensión arterial y 975 casos (5,74%) con preeclampsia/eclampsia(6).
De las 975 gestantes con preeclampsia/eclampsia, 483 fueron diagnosticadas con preeclampsia leve, 468 con preeclampsia severa, 18 con eclampsia y 16 con síndrome de HELLP. En 9 gestantes (1%) complicadas con preeclampsia/ eclampsia, el parto se produjo antes de las 28 semanas de gestación, en 165 (17%) entre las 28 y 34 semanas y en 801 (82%) después de las 34 semanas. El parto fue vaginal en 186 casos (19%) y por cesárea en 789 casos (81%). Se hospitalizó 449 recién nacidos (46%) de gestantes con preeclampsia/eclampsia, lo cual evidencia la morbilidad neonatal por razón de esta patología; 75 recién nacidos (17%) fueron pequeños para edad gestacional y 330 (73%), adecuados para la edad gestacional.
DIAGNÓSTICO DE LA PREECLAMPSIA
El espectro clínico de la preeclampsia varía desde formas leves a severas. En la mayoría de las mujeres, la progresión a través de este espectro es lenta, y el diagnóstico de preeclampsia leve debe ser interpretado como una fase de la enfermedad(1). En otros, la enfermedad progresa más rápidamente, cambiando de leve a grave en días o semanas. En los casos más graves, la progresión puede ser fulminante, con evolución a preeclampsia severa o eclampsia en cuestión de días o incluso horas. Por lo tanto, para el manejo clínico, la preeclampsia debe ser sobrediagnosticada, pues el objetivo más importante es la prevención de la morbimortalidad materna y perinatal.
Los criterios de diagnóstico de la preeclampsia son hipertensión y proteinuria(1,7-10). La hipertensión es definida como la presión arterial sistólica igual o mayor de 140 mmHg o diastólica igual o mayor de 90 mmHg, tomada en dos ocasiones y con un intervalo de 4 horas, y que ocurre después de las 20 semanas de embarazo en mujeres con presión arterial previa normal; o presión arterial sistólica igual o mayor de 160 mmHg o diastólica igual o mayor de 110 mmHg en cualquier momento(1,7-10). La elevación de la presión arterial (PA) a valores menores de 140/90 debe ser un signo de alerta y requiere una vigilancia muy estrecha. Se señala que las pacientes menores de 18 años fisiológicamente presentan cifras tensionales menores que las mujeres adultas.
La proteinuria es definida como una excreción urinaria de proteínas igual o mayor de 0,3 g en orina de 24 horas (se correlaciona con 30 mg/ dL o reactividad de tira 1+)(7-10). Ante el hallazgo de proteinuria, debe descartarse infección del tracto urinario. En vista de que recientes investigaciones no han encontrado relación entre la cantidad de proteína en orina y el pronóstico de la preeclampsia, la proteinuria mayor de 5 g ya no se considera como un criterio de preeclampsia severa(1,8).
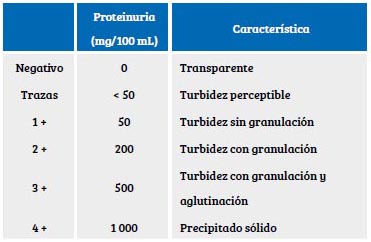
En el Instituto Nacional Materno Perinatal se realiza la prueba con ácido sulfosalicílico (ASS) al 3%, mezclando 1 mL de ASS (conservado en frasco oscuro) con 1 mL de orina centrifugada o decantada 1 hora; se toma muestra del sobrenadante, se mezcla por inversión, se deja reposar por 5 minutos y luego se realiza la lectura(12):

La muestra aislada presenta una tasa alta de falsos negativos de proteinuria, por lo que se ha tratado de recomendar la relación proteinuria/creatinuria, para evitar la necesidad de realizar recolecciones de orina de 24 horas(13). El valor clásico de 300 mg de proteína en orina de 24 horas es obtenido de estudios de mala calidad. Sin embargo, se le continúa utilizando(14).
En muchos casos se presentan gestantes con hipertensión sin proteinuria, que pueden ser diagnosticadas de preeclampsia si presentan alguno de los siguientes criterios(1): presión arterial sistólica ≥ 160 y diastólica ≥ 110 mmHg tomadas en por lo menos dos ocasiones y con un intervalo de 4 horas; trombocitopenia con un recuento de plaquetas menor de 100 000/microlitro; aumento de enzimas transaminasas hepáticas al doble de los valores normales; insuficiencia renal progresiva con una concentración de creatinina mayor de 1,1 mg/dL o un aumento al doble en ausencia de una enfermedad renal; edema pulmonar; síntomas cerebrales o visuales; o dolor severo o persistente en el hipocondrio derecho o en epigastrio. En la última Guía del Colegio Americano de Obstetras y Ginecólogos, de noviembre de 2013, no consideran como criterio de preeclampsia severa la restricción del crecimiento intrauterino y el oligohidramnios(1).
El edema no es incluido actualmente en el diagnóstico de preeclampsia porque aparece clínicamente hasta en 80% de las gestantes normales(15). Sin embargo, en nuestro medio es conveniente considerar los edemas patológicos de rápida instauración confirmados por ganancias ponderales anormales (ganancia de peso materno mayor a 800 g/semana) como un signo para el diagnóstico temprano de la entidad(15).
MANEJO DE LA PREECLAMPSIA
Establecido el diagnóstico de preeclampsia, se requiere inmediatamente evaluar el estado de salud de la gestante y el feto. En la gestante se debe realizar una evaluación clínica de las funciones neurológica, respiratoria y cardiovascular; al mismo tiempo se realizará una evaluación hematológica y bioquímica del número de plaquetas, pruebas de función renal (urea, creatinina y ácido úrico) y pruebas de función hepática (transaminasas y lactato deshidrogenasa)(1,9-11). Se evaluará el bienestar fetal con el monitoreo fetal electrónico -pruebas no estresante o estresante-, el perfil biofísico y estudio Doppler de las arterias umbilical y uterina. Si se considerara necesaria la valoración del grado de madurez pulmonar fetal(20), se realizará la amniocentesis, que tiene riesgos inherentes.
La gestante con preeclampsia con signos de severidad o eclampsia requiere hospitalización inmediata para su manejo respectivo(16), con el objetivo terapéutico(10,16) de controlar la hipertensión arterial, prevenir la ocurrencia de convulsiones o su repetición, optimizar el volumen intravascular, mantener una oxigenación arterial adecuada y diagnosticar y tratar precozmente las complicaciones.
En la preeclampsia, el tratamiento final es la interrupción del embarazo y generalmente se toma en cuenta las condiciones maternas para dicha interrupción, antes que la edad gestacional y la salud fetal.
MANEJO GENERAL DE LA PREECLAMPSIA Y ECLAMPSIA
Las gestantes con diagnóstico de preeclampsia o eclampsia deben ser hospitalizadas en un establecimiento de segundo nivel de atención y de categoría II-2 o III, que disponga de una unidad de cuidados intensivos materna y banco de sangre. Durante la hospitalización se monitorizará la presión arterial cada 4 horas, así como las funciones vitales, latidos cardiacos fetales y contracciones uterinas; del mismo modo, se controlará la diuresis y realizará el control bioquímico y hematológico, que incluye perfil de coagulación, perfil renal (creatinina, urea y ácido úrico, depuración de creatinina), proteinuria cualitativa diaria, control diario de peso, balance de líquidos administrados y eliminados, perfil hepático (enzimas hepáticas) diario o más seguido, de ser necesario. Se evaluará el bienestar fetal por lo menos cada 72 horas.
MANEJO DE LA PREECLAMPSIA SIN CRITERIOS DE SEVERIDAD
La preeclampsia sin criterios de severidad es aquella que solo presenta hipertensión mayor o igual a 140/90 mmHg pero menor de 160/110 mmHg, sin ninguna disfunción hematológica, renal, hepática, pulmonar o neurológica y sin signos de compromiso fetal. Se indicará reposo relativo(1,17-19) y dieta normocalórica, normoproteica y normosódica(17). No está indicado el uso de antihipertensivos(1,17-19). El tratamiento definitivo de la preeclampsia es culminar la gestación. Si la gestante tiene 37 semanas o más, se debe culminar la gestación por vía vaginal o por cesárea(1,17-21). Si la gestante tiene menos de 37 semanas y no hay afectación materna o fetal, se puede tener una conducta expectante, continuando con las medidas generales y una estricta vigilancia materna y fetal(18-21). Si a pesar del manejo no se controla la hipertensión arterial o la enfermedad progresa a preeclampsia severa, o existe pródromos de eclampsia o signos de sufrimiento fetal, de disfunción hematológica, renal, hepática, pulmonar o neurológica, se finalizará la gestación inmediatamente, independiente de la edad gestacional, por vía vaginal o por cesárea(1,10,18-21).
MANEJO DE LA PREECLAMPSIA CON CRITERIOS DE SEVERIDAD
La preeclampsia con criterios de severidad evoluciona hacia complicaciones graves como edema agudo de pulmón, falla renal, encefalopatía hipertensiva con hemorragia cerebral, desprendimiento de retina, desprendimiento prematuro de placenta, hematoma subcapsular hepático o rotura hepática, sindrome HELLP, que pueden llevar a la muerte de la gestante y del feto o recién nacido(1,17-21). Por lo tanto, el manejo debe ser oportuno, multidisciplinario y efectivo(8,15,21,23). En una gestante que presenta sangrado vaginal y signos de desprendimiento prematuro de placenta, siempre sospechar en una preeclampsia como cuadro de fondo.
En la preeclampsia hay una contracción del contenido intravascular, a diferencia de la hipervolemia usual de la gestante; hay tendencia a oliguria por falta de fluidos, a pesar del edema. Deberá asegurarse una expansión adecuada del intravascular con solución salina al 9 o/oo, a razón de 50 a 60 gotas por minuto el primer litro; y, en caso de persistir la oliguria, iniciar coloides 500 mL a goteo rápido, seguido de furosemida 10 mg e.v. Administrar por lo menos tres litros de cristaloides durante las primeras 24 horas(10). Se controlará la diuresis con sonda de Foley y bolsa colectora; se monitorea la presión arterial, frecuencia cardiaca, frecuencia respiratoria y saturación de oxígeno cada 15 minutos. Iniciar por vía venosa una infusión de sulfato de magnesio(1,9,10,17-21) para la prevención de convulsiones. La infusión se prepara combinando 5 ampollas de sulfato de magnesio al 20% (ampollas de 10 mL) con solución salina 9 o/oo 50 mL(22). Esta solución proporciona 1 g de sulfato de Mg por cada 10 mL, y debe administrarse 4 gramos (40 mL) en 15 a 20 minutos por volutrol, como dosis inicial de ataque; se continuará con una infusión de 1 g por hora (10 mL por hora) y mantener la infusión por 24 horas después del parto(1,10,22). Durante la administración del sulfato de magnesio se controlará los reflejos rotulianos, la frecuencia respiratoria -que debe ser por lo menos 14 respiraciones/minuto- y la diuresis, que no debe ser menor de 25 a 30 mL/hora. Se recomienda también el control de la saturación de O2 mediante pulsioximetría(10).
Se suspenderá la administración de sulfato de magnesio si se detecta arreflexia tendinosa, si hay depresión del estado de conciencia o si se presenta tendencia a la ventilación superficial o lenta; en este caso, administrar gluconato de calcio, 1 a 2 gramos vía endovenosa. En casos de insuficiencia renal aguda, el sulfato de magnesio debe ser administrado en forma prudente. El tratamiento antihipertensivo solo debe ser utilizado si la presión arterial sistólica es ≥ 160 mmHg o si la presión arterial diastólica es ≥ 110 mmHg, en cuyo caso se recomienda usar los siguientes fármacos(17,18,21,23):
-
Labetalol :
Hidralacina:
Metildopa
Nifedipino:
La medicación para controlar la hipertensión arterial deberá disminuirse según evolución, sobre todo después de producido el parto. El tratamiento se continuará durante 7 días.
El atenolol, los inhibidores de la enzima convertidora de angiotensina y los bloqueadores de los receptores de la angiotensina están contraindicados en el embarazo.
Las pacientes con preeclampsia severa deben tener una evaluación por la unidad de cuidados intensivos materna(10).
En caso de gestación mayor o igual a 34 semanas o si se tiene la seguridad de madurez pulmonar fetal, se concluirá el embarazo en el menor tiempo posible, ya sea por vía vaginal o por cesárea(1,10,17,18).
En caso de gestaciones menores de 34 semanas sin disfunción orgánica materna y fetal, se procederá a administrar corticoides para maduración pulmonar fetal: betametasona 12 mg endovenoso cada 24 horas en 2 dosis o dexametasona 6 mg endovenoso cada 12 horas en 4 dosis(23,24). Se puede tener una conducta expectante durante 48 horas para inducir la maduración pulmonar, lo que podría mejorar el pronóstico fetal; sin embargo, hay que hacer una evaluación muy estricta de los parámetros de la función hepática, hematológica y renal materna, así como evaluar el bienestar fetal(24). Retrasar el término del embarazo podría significar una alta morbilidad materna y fetal(1).
Vigil de Gracia(25) demostró en el estudio MEXPRE 2913 que el manejo expectante de la preeclampsia severa en gestaciones de 28 a 34 semanas no muestra un beneficio neonatal. Además encontró que un enfoque conservador puede aumentar el riesgo de desprendimiento prematuro de placenta y recién nacidos pequeños para la edad gestacional. En el Instituto Nacional Materno Perinatal el manejo de la preeclampsia severa antes de las 34 semanas sigue las conclusiones de este estudio: administrar corticoides para inducir la maduración pulmonar y terminar la gestación, generalmente por cesárea. Este manejo ha permitido mejorar el pronóstico materno perinatal.
En gestaciones menores de 24 semanas, la supervivencia perinatal es de 6,7%; por lo tanto, debe culminarse la gestación a la brevedad posible para evitar mayor morbilidad materna.
Las indicaciones de finalización del embarazo, independientes de las semanas de gestación, son(1,10,17,18,21):
-
Indicaciones maternas: plaquetopenia menor de 100 000 o plaquetopenia progresiva, persistencia de hipertensión severa a pesar del tratamiento, signos prodrómicos de eclampsia, eclampsia, deterioro progresivo de la función renal u oligoanuria persistente, deterioro progresivo de la función hepática, hemorragia cerebral, edema pulmonar, hematoma subcapsular hepático o rotura hepática, desprendimiento prematuro de placenta, cefalea persistente o alteraciones visuales y dolor persistente en epigastrio o hipocondrio derecho.
-
Indicaciones fetales: cuando existan signos de riesgo de pérdida del bienestar fetal demostrado en un registro cardiotocográfico patológico o un perfil biofísico menor de 4 o restricción severa del crecimiento fetal, con Doppler de arteria umbilical que muestra diástole ausente o revertida, presencia de oligohidramnios o signos de restricción del crecimiento intrauterino.
MANEJO DE LA ECLAMPSIA
Las convulsiones eclámpticas amenazan la vida y deben ser consideradas como una urgencia vital. Estas pueden producirse antes del parto, durante o después del mismo y pueden aparecer aún con niveles de hipertensión no consideradas graves.
El manejo de la eclampsia requiere el control de las convulsiones y prevención de las recurrencias con sulfato de magnesio(26), a las mismas dosis indicadas en la preeclampsia severa: sulfato de magnesio 4 gramos endovenosos en 20 minutos; el sulfato de magnesio está asociado con reducciones clínicamente significativas en la muerte materna. Es accesible y su administración y control resultan relativamente sencillos. Se le puede administrar por vía intramuscular cuando no se dispone de personal con experiencia en la administración intravenosa(1,10).
Al mismo tiempo, se realizará la corrección de la hipoxemia materna y/o acidosis, controlar la hipertensión arterial y las funciones vitales maternas. Se solicitará pruebas hepáticas, pruebas renales, perfil de coagulación y hemoglobina; evaluar el bienestar fetal. Se coordinará con la unidad de cuidados intensivos materna y con la unidad de cuidados intensivos neonatal, así como con anestesiología.
Una vez estabilizada la paciente, se iniciará el proceso de parto, que en la mayoría de veces consiste de una cesárea de emergencia. En el posparto, la paciente continuará su hospitalización en la unidad de cuidados intensivos materna(10).
MANEJO DEL SÍNDROME DE HELLP
El síndrome HELLP es un trastorno severo del estado gestacional y puerperal relacionado con las formas graves de preeclampsia y eclampsia. Algunos autores admiten la posibilidad de que esta noxa exista sin vínculo alguno con la preeclampsia. Se discute si se trata de un síndrome o debe ser identificado como una entidad con características clínicas propias .
Louis Weinstein, en 1982, publicó los primeros 29 casos diagnosticados en pacientes con preeclampsia y eclampsia. Requiere internamiento de urgencia en una unidad de cuidados intensivos, estabilizar la condición materna y culminar la gestación en el menor tiempo posible, independientemente de la edad gestacional, y que en la mayoría de casos es por cesárea. El manejo expectante no está recomendado(1,9). Algunos estudios están considerando el uso de corticoides para mejorar el estado materno y fetal, especialmente cuando el recuento plaquetario es muy bajo(1,9). El síndrome de HELLP se complica muy frecuentemente con insuficiencia respiratoria, cardiaca, hematoma subcapsular hepático o rotura hepática, insuficiencia renal, desprendimiento prematuro de placenta y hemorragia posparto, disfunción hematológica y disfunción neurológica. La morbilidad materna extrema y mortalidad materna son muy altas(27).
HEMATOMA SUBCAPSULAR HEPÁTICO Y ROTURA HEPÁTICA
Aberombic(28) describió el hematoma subcapsular hepático, que se presenta en 1:45 000 a 225 000 embarazos, o lo que es lo mismo, en 1% de los casos de síndrome de HELLP. La posibilidad de recurrencia en embarazos posteriores oscila entre el 4 y 27%(29).
La sospecha clínica, el diagnóstico rápido y un tratamiento multidisciplinario son fundamentales para mejorar la morbimortalidad de estas pacientes. El tratamiento abarca desde la conducta expectante y seguimiento clínico(30), la embolización de las arterias hepáticas(31) o tratamiento quirúrgico en presencia de inestabilidad hemodinámica, persistencia de sangrado o aumento del dolor(32).
El tratamiento clásico se basa en el abordaje quirúrgico de la rotura hepática. Pueden ser el empaquetamiento con gasas o la ligadura de las arterias hepáticas, e incluso trasplante hepático(33). En el Instituto Nacional Materno Perinatal se viene usando el empaquetamiento hepático temporal para controlar la hemorragia, con colocación de bolsa de Bogotá, que consiste en dejar abierta la cavidad abdominal y suturar a la aponeurosis una lámina de plástico con el objeto de disminuir la tensión de la pared abdominal y evitar el síndrome compartimental(34).
Se ha descrito también técnicas utilizando el bisturí de argón(35) y la administración de factor VIIa recombinante(36), para la hemostasia hepática.
Ante la sospecha de un síndrome de HELLP complicado con rotura hepática y la necesidad de practicar una cesárea urgente, se recomienda el abordaje quirúrgico del hígado en el mismo acto. Si el síndrome de HELLP se desarrolla en el puerperio y en un hígado sano, se puede valorar un manejo más conservador mediante la embolización de la arteria hepática común o bien de una de sus ramas principales.
VÍA DEL PARTO
En general se acepta que para el nacimiento del feto el parto sea por vía vaginal mejor que por cesárea(1,10,17-21). Para la elección de la vía de parto, habrá que tener en cuenta factores tales como la presentación, las condiciones cervicales, la edad gestacional, entre otros(1,10,16,18,19). En el Instituto Nacional Materno Perinatal, la preeclampsia es la segunda causa de cesáreas(6). Se puede utilizar las prostaglandinas locales para la maduración cervical(37).
En las gestantes con preeclampsia severa se solicitará consulta preanestésica previa al parto. La anestesia regional (epidural, espinal o combinadas) consigue un buen control de la hipertensión y mejora el flujo sanguíneo útero-placentario, por lo que es la técnica de elección en estas pacientes, siempre que no existan contraindicaciones.
CONTROL POSPARTO(1,36)
En el posparto se debe continuar el monitoreo de las funciones vitales: presión arterial, frecuencia cardiaca, frecuencia respiratoria y saturación de oxígeno, control de la diuresis horaria, control hemático y bioquímico del recuento de plaquetas, urea, creatinina y transaminasas.
Controlar estrictamente la administración de líquidos, por el riesgo incrementado de exacerbación de la hipertensión y de edema del pulmón en esta fase por aumento de la infusión de líquidos durante el periparto (prehidratación para anestesia, administración de varias medicaciones en perfusión continua) y la movilización de líquidos desde el espacio extravascular hacia el intravascular. La infusión total de líquidos debe limitarse durante la fase intraparto y posparto a 80 mL por hora o 1 mL/kg/hora.
Se continuará con los mismos fármacos antihipertensivos utilizados en el anteparto, ya sea por vía endovenosa u oral, dependiendo de la respuesta y el estado de la paciente. La hipertensión, después de una fase inicial de mejoría, puede empeorar entre el tercer y sexto día. En esta fase, se puede usar otros antihipertensivos, tipo inhibidores de la enzima convertidora de angiotensina. El tratamiento hipotensor se suspenderá tras 48 horas de presión arterial normal.
La infusión de sulfato de magnesio se mantendrá por un periodo de 24 a 48 horas. En casos de normalización de la presión arterial y sin signos prodrómicos de eclampsia, se puede suspender a las 24 horas. Si transcurridas 48 horas persisten los signos o síntomas prodrómicos, se mantendrá el tratamiento 24 horas más.
Los criterios para el alta de las pacientes son la normalización de la presión arterial, la evolución clínica y la normalización de los exámenes de laboratorio. En caso de persistencia de la hipertensión arterial, proteinuria u otras alteraciones analíticas, transcurrido este período, deberá sospecharse una alteración subyacente, por lo que se recomienda poner en marcha las investigaciones necesarias para llegar a un diagnóstico correcto.
REFERENCIA Y CONTRARREFERENCIA
En el primer nivel (postas, centros de salud, hospitales nivel I) se realizará el control prenatal de las gestantes sin complicaciones o sin factores de riesgo; si se encontrase una gestante con presión arterial elevada, esta debe ser referida al nivel inmediato superior para el manejo respectivo.
Si la paciente llega en trabajo de parto a un centro materno u hospital nivel II-1, y se le detecta hipertensión arterial, se procederá a la atención del parto y al mismo tiempo se establecerá si se trata de un caso de preeclampsia y si presenta criterios de severidad. De ser catalogada como preeclampsia severa, la paciente será transferida a un hospital nivel II-2 o III.
Las pacientes atendidas en los hospitales nivel II serán referidas al nivel III en caso sean diagnosticadas como preeclampsia severa/eclampsia/síndrome HELLP y por embarazo pretérmino(37-39).
REFERENCIAS BIBLIOGRÁFICAS
1. Report of the American College of Obstetricians and Gynecologists. Task Force on Hypertension in Pregnancy. Hypertension in Pregnancy. Obstet Gynecol. 2013 Nov;122(5):1122-31. doi: 10.1097/01.AOG.0000437382.03963.88.
2. Pacheco J. Peeclampsia/eclampsia: reto para el gineco-obstetra. Acta Méd Per. 2006;23(2):100-11.
3. Pacheco J, Wagner P, Williams N, Sánchez S. Enfermedad hipertensiva de la gestación. En: Pacheco J (ed). Ginecología, Obstetricia y Reproducción. Segunda Edición. Lima: REP SAC, 2007.
4. Chirinos J. Incidencia y características de la enfermedad hipertensiva en el embarazo: estudio retrospectivo a nivel del mar y en la altura. Acta Andina. 1995;4(1):25-34.
5. Dirección General de Epidemiología. Ministerio de Salud. Sistema Nacional de Vigilancia Epidemiológica. Reporte Epidemiológico de la Mortalidad materna en el Perú 2012. 2013.
6. Instituto Nacional Materno Perinatal. Oficina de Estadística e Informática. Información para la red 2013.
7. National High Blood Pressure Education Program. Working Group Report on High Blood Pressure in Pregnancy. National Institute of Health Publication No. 00-3029 Originally Printed 1990. Revised July 2000;1 - 83.
8. American College of Obstetricians and Gynecologists. Task Force on Hypertension in Pregnancy. Hypertension in Pregnancy. ISBN 978-1-934984-28-4. 2013; Pg 1 - 89.
9. American College of Obstetricians and Gynecologists. Diagnosis and Management of Preeclampsia and Eclampsia. Practice Bulletin Clinical Management Guidelines for Obstetrician-Gynecologists. Number 33, January 2002:159-67.
10. Instituto Nacional Materno Perinatal. Guías de Práctica Clínica y de Procedimientos en Obstetricia y Perinatologia. 2014:69-83.
11. Chobanian AV, Bakris GL, Black HR, Cushman WC, Green LA, Izzo JL Jr, Jones DW, Materson BJ, Oparil S, Wright JT Jr, Roccella EJ; National Heart, Lung, and Blood Institute Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure; National High Blood Pressure Education Program Coordinating Committee. The Seventh Report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure: the JNC 7 report. JAMA. 2003 May 21;289(19):2560-72.
12. Henry JB. El Laboratorio en el Diagnóstico Clínico. España: Editorial Marban Libros S.L. 2007:633-4.
13. Maybury H, Waugh J. Proteinuria in pregnancy - Just what is significant? Fetal and Maternal Medicine Review. 2004;16:71-95. doi.org/10.1017/S0965539504001445.
14. Kuo VS, Koumantakis G, Gallery EDM. Proteinuria and its assessment in normal and hypertensive pregnancy. Am J Obstet Gynecol. 1992;167:723-8.
15. Brown MA. Diagnosis and classification of preeclampsia and other hypertensive disorders of pregnancy. En: Belfort MA, Thornton S and Saade GR (eds). Hypertension in Pregnancy: New York: Marcel Dekker, 2003:1-16.
16. Bautista A. Hipertensión y embarazo. Toxemia gravídica. En: Ñáñez H, Ruiz AI, eds. Texto de obstetricia y perinatología. Una contribución a la enseñanza del arte, ciencia y tecnología. Pharmacia Upjohn. Cap. 33. 1999:487-524.
17. Federación Latinoamericana de Sociedades de Obstetricia y Ginecología. Módulo de capacitación en Pre-Eclampsia/ Eclampsia. Diciembre 2012:1-53.
18. World Health Organization. WHO recommendations for prevention and treatment of pre-eclampsia and eclampsia. 2011:1-38.
19. Royal College of Obstetricians and Gynaecologists. Hypertension in pregnancy: the management of hypertensive disorders during pregnancy. Agosto 2010:111-78.
20. Magee LA, Helewa M, Moutquin JM, von Dadelszen P; Hypertension Guideline Committee; Strategic Training Initiative in Research in the Reproductive Health Sciences (STIRRHS) Scholars. Diagnosis, evaluation, and management of the hypertensive disorders of pregnancy. J Obstet Gynaecol Canada. 2008 Mar;30(3):S1-48.
21. Sociedad Española de Ginecología y Obstetricia. Guía Práctica de Urgencias en Obstetricia y Ginecología. Hipertensión arterial y gestación. Mayo 2008:33-6.
22. Khan KS. Sulfato de magnesio y otros anticonvulsivos en mujeres con preeclampsia: comentario de la BSR (última revisión: 8 de septiembre de 2003). Biblioteca de Salud Re-productiva de la OMS; Ginebra: Organización Mundial de la Salud.
23. Uzan J, Carbonnel M, Piconne O, Asmar R, Ayoubi JM. Preeclampsia fisiopatología, diagnóstico y tratamiento. Vasc Health Risk Management. 2011:7:467-74. doi: 10.2147/ VHRM.S20181.
24. Ganzevoort W, Sibai B. Temporising versus interventionist management (preterm and at term). Best Pract Res Clin Obstet Gynaecol. 2011 Aug;25(4):463-76. doi: 10.1016/j.bpobgyn.2011.01.004.
25. Vigil-De Gracia P, Reyes Tejada O, Calle Miñaca A, Tellez G, Chon VY, Herrarte E, Villar A, Ludmir J. Expectant management of severe preeclampsia remote from term: the MEXPRE Latin Study, a randomized, multicenter clinical trial. Am J Obstet Gynecol. 2013 Nov;209(5):425.e1-8. doi: 10.1016/j.ajog.2013.08.016.
26. Lombaard H, Pattinson B. Conducta activa versus conducta expectante para la preeclampsia severa antes de término: Comentario de la BSR (última revisión: 5 de agosto de 2004). La Biblioteca de Salud Reproductiva de la OMS; Ginebra: Organización Mundial de la Salud).
27. Atallah AN. Tratamiento anticonvulsivo para la eclampsia: comentario de la BSR (última revisión: 14 de noviembre de 2003). La Biblioteca de Salud Reproductiva de la OMS; Ginebra: Organización Mundial de la Salud.
28. Reubinoff BE, Schenker IG. HELLP syndrome complicating preeclampsia, eclampsia. Int J Gyneacol Obstet. 1991;36:95-102.
29. Aberombic J. Haemorrhage of the liver. London Medical Gazette. 1984;34:792-4.
30. Rojas G. HELLP syndrome. Critical state. Current concepts. Ginecol Obstet Mex. 1996;64:64-72.
31. Pilco P. Ruptured subcapsular hepatic hematoma associated with HELLP syndrome. Rev Gastroenterol Peru. 2006;26:207-10.
32. Rinehart BK, Terrone DA, Magann EF, Martin RW, May WL, Martin JN Jr. Preeclampsia-associated hepatic hemorrhage and rupture: mode of management related to maternal and perinatal outcome. Obstet Gynecol Survey. 1999;54:196-202. doi: 10.1097/00006254-19990300000024.
33. Wilson RH. Postpartum rupture of subcapsular hematoma of the liver. Acta Obstet Gynecol Scandinav. 1992;71:394.
34. Reck T. Surgical treatment of HELLP syndrome-associated liver rupture. An update. Eur J Gynecol Reprod Biol. 2001;99:57-65.
35. Shrivastava VK. Argon beam coagulator for treatment of hepatic rupture with hemolysis, elevated liver enzymes, low platelets (HELLP) syndrome. Obstet Gynecol. 2006;107:525-6.
36. Dart BW. A novel use of recombinant factor VIIa in HELLP associated with spontaneous hepatic rupture and abdominal compartment syndrome. J Trauma. 2004;57:171-4.
37. Hofmeyr G Justus, Gülmezoglu A Metin, Pileggi Cynthia. Vaginal misoprostol for cervical ripening and induction of labour. Cochrane Database of Systematic Reviews, Issue 02, 2011. Copyright © 2009 The Cochrane Collaboration. Published by John Wiley & Sons, Ltd. DOI: 10.1002/14651858.CD000941.pub1
38. Sibai B. Etiology and management of postpartum hypertension-preeclampsia. Am J Obstet Gynecol. 2012 Jun;206(6):470-5. doi: 10.1016/j.ajog.2011.09.002.
39. Ministerio de Salud. Dirección General de Salud de las Personas. Estrategia Sanitaria Nacional de Salud Sexual y Reproductiva. Guías de Práctica Clínica para la Atención de Emergencias Obstétricas según nivel de Capacidad Resolutiva. Lima; 2007:53-62.
40. Ministerio de Salud. Dirección General de Salud de las Personas. Dirección Ejecutiva de Atención Integral de Salud. Guías Nacionales de Atención Integral de Salud sexual y Reproductiva. Módulo III Emergencias Obstétricas: Lima, 2004:16-20.
41. Organización Panamericana de la Salud. Manejo de las complicaciones del embarazo y el parto: Guía para obste-trices y médicos. Sección II. 2002:S39-62.
Conflictos de interés: No existen en el presente artículo.
Lugar de correspondencia:
Dr. Enrique Guevara Ríos.
enriqueguevararios@gmail.com; eguevara@iemp.gob.pe; enriqueg@pathfinder.org; eguevara@insap.org.pe














