Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Peruana de Ginecología y Obstetricia
On-line version ISSN 2304-5132
Rev. peru. ginecol. obstet. vol.62 no.4 Lima Oct. 2016
ARTÍCULO ORIGINAL
Diez años de reproducción asistida de alta complejidad en los Andes del Perú
Ten years of high complexity assisted reproduction techniques in the Peruvian Andes
Luis Alberto Vargas Tominaga1,a,b, Ricardo Pella1,c, Livia Bartolo1,d, Fiorella Alarcón1, Alberto Vargas1,a, Andrea Vargas1,d, Gaby Bernal1,d, María Gallegos1,e, Deny Escobedo1,e, Maritza Gómez1,f, Hilda Huaynapata1,e
1 Centro de Fertilidad y Ginecología del Sur (CFGS)
a Ginecólogo-Obstetra b Director Médico c Biólogo con mención en Genética d Bióloga e Técnica de Enfermería f Licenciada en Enfermería
Resumen
Introducción: La infertilidad es un diagnóstico cada vez más frecuente, tanto a nivel del mar como en las grandes alturas, y el desarrollo de técnicas de reproducción asistida de alta complejidad en los Andes del Perú es imprescindible. Objetivo: Definir los resultados de estas técnicas en una institución a 3 330 metros sobre el nivel del mar. Diseño: Estudio descriptivo y retrospectivo. Institución: Centro de Fertilidad y Ginecología del Sur, Cusco, Perú. Pacientes: 576 pacientes con infertilidad atendidas entre los años 2005 al 2015. Métodos: Se revisó los registros de los procedimientos realizados y se estableció las tasas de embarazo clínico según la edad y días de cultivo, tanto en ovocitos autólogos como en ovodonación. Lasignificancia estadística de las diferencias encontradas fue analizada por medio de la prueba exacta de Fisher. Principal medida de resultados: Tasa de embarazo clínico. Resultados: Las tasas de embarazo clínico fueron: 30,4% en ovocitos autólogos, 42,4% en ovodonación y 25,0% en maduración in vitro de ovocitos. La frecuencia de embarazo doble fue 31,6%, y triple, 7,9%. Conclusiones: Las tasas de embarazo clínico fueron similares a las observadas internacionalmente. Destaca la necesidad de estrategias para disminuir la pluralidad de los embarazos, así como para mejorar la tasa de embarazo en las mujeres ≥ 37 años.
Palabras clave: Fertilización In Vitro - FIV; Inyección Intracitoplasmática de Espermatozoides -ICSI.
Abstract
Introduction: Infertility is currently a more frequent diagnosis, at sea level and at high altitudes, and development of high complexity assisted reproduction techniques in the Andes of Peru is essential. Objective: To define the results of the application of these techniques in an institution at 3 330 meters above sea level. Design: Descriptive and retrospective study. Setting: Centro de Fertilidad y Ginecología del Sur, Cusco, Peru. Patients: 576 patients with infertility attended between years 2005-2015. Methods: Records of the procedures performed were reviewed and rates of clinical pregnancy according to age and days of culture were established for both autologous oocytes and ovodonation. Statistical significance of differences found was analyzed by Fisher exact test. Main outcome measure: Rate of clinical pregnancy. Results: Rates of clinical pregnancy were: 30.4% in autologous oocytes, 42.4% in ovodonation, and 25% in in vitro maturation oocytes. Frequency of twin pregnancy was 31.6%, and of triple pregnancy, 7.9%. Conclusions: Rates of clinical pregnancy were similar to those observed internationally. This emphasizes the need of strategies to diminish the plurality of pregnancies, as well as to improve the rate of pregnancy in women ≥ 37 years old.
Keywords: In Vitro Fertilization - IVF; Intracytoplasmic Sperm Injection - ICSI.
Introducción
Debido a la alta tasa de natalidad en el Perú, uno de los programas de salud más importantes es el de anticoncepción y planificación familiar. Sin embargo, un diagnóstico que desde hace unos años se constituye casi como un problema de salud pública es la infertilidad, pues se calcula que cerca de 1 millón de personas en el Perú son infértiles(1).
El Perú tiene una gran diversidad geográfica, con centros poblados tanto a nivel del mar como a grandes alturas. El vivir a grandes alturas (por encima de los 1 500 metros sobre el nivel del mar (m.s.n.m) somete a la persona a hipoxia, frío, sequedad e irradiación ultravioleta(2), condiciones que exigen al organismo y que requiere de mecanismos de adaptación en su morfología y fisiología(3-5). Para el año 2014, más de 10 millones de peruanos habitaban las grandes alturas(6).
En la altura, la menarquía es más tardía, y la menopausia, más temprana(5). Las patologías relacionadas a infertilidad son probablemente similares a nivel del mar y en la altura. Sin embargo, la disminución más temprana de la reserva ovárica (RO) y el inicio más temprano de la menopausia complican más la búsqueda de embarazo en las poblaciones que viven a grandes alturas.
Una de las áreas más fascinantes de la medicina moderna es el de las técnicas de reproducción asistida (TRA) de alta complejidad. La fertilización in vitro (FIV) lleva más de 35 años incorporada en la práctica clínica, y su trascendencia se objetiva por las siguientes cifras: cerca de 48 millones de personas en el mundo son infértiles(7), 1,6% de los niños nacidos en Estados Unidos y entre 2 a 6%, en Europa, son producto de estos procedimientos; a nivel mundial se realizan 1,5 millones de ciclos de FIV cada año, y a la actualidad son ya cerca de 7 millones los niños logrados por FIV.
El Centro de Fertilidad y Ginecología del Sur (CFGS), instalado en la ciudad de Cusco, en los Andes del Perú, desde el año 1999 realiza TRA de baja complejidad, como estimulación ovárica e inseminación intrauterina, y desde el año 2005, las TRA de alta complejidad, iniciando con FIV, luego la inyección intracitoplasmática de espermatozoides (ICSI, por sus siglas en inglés), y en los últimos años, la maduración in vitro de ovocitos (IVM, por sus siglas en inglés).
El presente documento revisa la experiencia y resultados de las TRA de alta complejidad en el CFGS.
Métodos
El CFGS se encuentra instalado en la ciudad de Cusco, a 3 330 m.s.n.m. y la población a la que asiste es procedente de las regiones de Cusco, Puno, Apurímac y Madre de Dios.
Se realiza un estudio descriptivo y restrospectivo, revisando los registros de procedimientos de FIV e ICSI (FIV/ICSI) realizados desde mayo de 2005 hasta diciembre de 2015, con ovocitos autólogos y ovodonación.
En los primeros ciclos de FIV, se realizó la estimulación ovárica con el uso de agonistas GnRH (a-GnRH) en protocolo largo o corto asociados a gonadotropina menopáusica humana (HMG) o FSH recombinante (FSHr)(8). El seguimiento de la estimulación se realiza a través de ultrasonido vaginal y se programa la aspiración folicular luego de 36 horas de la aplicación de gonadotropina coriónica humana (hCG). Desde febrero de 2008 iniciamos el uso de antagonistas GnRH (ant-GnRH)(9) y desde junio de 2010, el uso de hCG recombinante (r-hCG).
La aspiración folicular se realiza bajo neuroleptoanalgesia con aguja de un solo lumen y bajo guía de ultrasonido vaginal. Se inicia soporte lúteo con 600 a 800 mg de progesterona micronizada o anillo de progesterona, por vía vaginal, o progesterona 50 mg diario por vía intramuscular.
Se utilizó medio de cultivo Life-Global™ para la manipulación de gametos y cultivo de embriones en incubadora de CO2 a 37ºC. En el caso de FIV, los ovocitos aspirados son colocados en placas petri con medio de cultivo, con 100 000 a 200 000 espermatozoides capacitados. En el caso de ICSI, los espermatozoides son preparados mediante gradientes de densidad y seleccionados por swim-out en gotas de 5 μl en el plato de ICSI. A las 16 horas, se verifica la fecundación y se coloca los embriones en medio de cultivo hasta el estadio de clivaje.
En el año 2008 iniciamos el cultivo de embriones hasta el estadio de blastocisto, procediendo a ello cuando el número de ovocitos fecundados es > 5, y manteniendo los embriones sin realizar cambio de medio de cultivo para el paso del es tadio de clivaje hacia blastocisto.
La transferencia de embriones es bajo guía de ultrasonido abdominal, con vejiga llena, utilizando catéter flexible y la paciente queda en reposo durante 45 minutos. Se realiza dosaje de subunidad β-hCG a los 17 días de la aspiración folicular, y ultrasonido vaginal, luego de 10 días, para evidenciar el número de embriones implantados y la actividad cardiaca.
La vitrificación y desvitrificación para las transferencias diferidas de embriones la realizamos bajo la técnica de Kuwayama(10).
La tasa de embarazo clínico (TEC) se define como el número de pacientes con gestación activa en relación al número de pacientes con transferencia embrionaria.
La significancia estadística de las diferencias encontradas se analizó a través de la prueba exacta de Fisher.
Resultados
El mes de mayo del año 2005 marcó el inicio de nuestro trabajo en TRA de alta complejidad, tanto con ovocitos autólogos como con ovodonación.
En junio de 2006 se produjo el nacimiento del primer niño producto de FIV, de paciente receptora de óvulos donados. Luego, en marzo de 2007, el nacimiento de dos niños, producto del primer embarazo logrado por FIV con ovocitos autólogos, y es en este año que publicamos la experiencia con los primeros 8 casos de FIV(8).
En junio de 2009 se logró el nacimiento del primer niño producto de transferencia de blastocistos y en febrero de ese año presentamos ante el XVII Congreso Peruano de Obstetricia y Ginecología(9), los primeros 27 casos de FIV en el CFGS.
En el año 2010 iniciamos los procedimientos de ICSI, con el nacimiento de los primeros niños producto de esta técnica en octubre del mismo año. Debido a la elevada frecuencia de factor masculino asociado, desde abril de 2010 realiza mos ICSI en todas las pacientes que requieren FIV.
A diciembre de 2015 hemos realizado 576 casos de FIV/ICSI, correspondiendo 55,4% a ovocitos autólogos y 44,6% a ovodonación. A continuación describimos los resultados de cada una de las TRA desarrolladas en el CFGS.
Fueron 319 los casos de FIV/ICSI con ovocitos autólogos, de los cuales, 21,0% correspondieron a FIV y 79,0% a ICSI. Se realizó la transferencia de embriones en estadio de clivaje (TED3) en 71,8% de pacientes y en estadio de blastocisto (TED5) en 28,2%.
La edad de las pacientes se distribuyó de la siguiente forma: 45,8% fueron mujeres ≤ 34 años, 39,5%, entre 35 a 39 años, y 14,7%, ≥ 40 años.
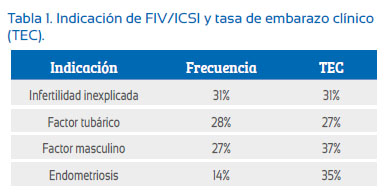
La indicación de FIV/ICSI fue en el 31% por infertilidad inexplicada, en 28% por factor tubárico, en 27% por factor masculino y en 14% por endometriosis (Tabla 1).
La TEC de FIV/ICSI fue 30,4% por transferencia embrionaria, 25,4% en FIV y 31,7% en ICSI, respectivamente. La TEC fue 31% en infertilidad inexplicada, 27% en factor tubárico, 37% en factor masculino y 35% en endometriosis.
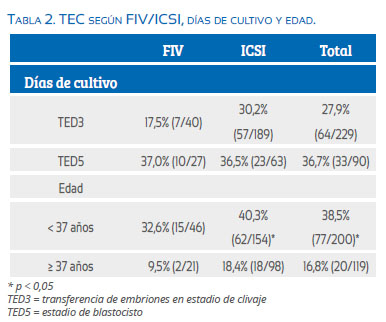
La TED3 logró una TEC de 27,9%, y la TED5, de 36,7%. Esta última es similar tanto para FIV e ICSI, 37,0% y 36,5%, respectivamente, mientras que la TED3 logró una TEC de 17,5% en FIV y 30,2% en ICSI (Tabla 2).
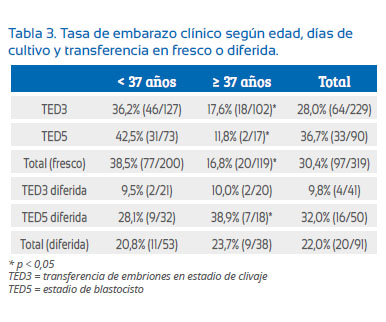
Los resultados fueron mejores cuando la paciente tenía < 37 años, con una TEC de 38,5% (36,2% en TED3 y 42,5% en TED5), mientras que, cuando la paciente tenía ≥ 37 años, la TEC fue 16,8% (17,6% en TED3 y 11,8% en TED5) (tablas 2 y 3).
La transferencia diferida de embriones (91 casos) logró una TEC de 22,0%, siendo 9,8% en TED3 y 32,0% en TED5. Considerando el grupo de mujeres ≥ 37 años, la TEC fue 10,0% en TED3 y 38,9% en TED5.
La transferencia diferida logró el nacimiento de un primer niño en marzo de 2012 (a diciembre de 2015 son 160 casos de transferencia de embriones desvitrificados, tanto en ovocitos autólogos como ovodonación).
En mujeres < 37 años, el uso de a-GnRH logró una TEC de 30,9%, y el uso de ant-GnRH, 40,7%. En mujeres ≥ 37 años con reserva ovárica (RO) adecuada (recuento de folículos antrales ≥ 7), la TEC fue 22,2% con a-GnRH y 21,4% con ant-GnRH, mientras que cuando la RO estuvo disminuida, la TEC fue 10,5% y 4,8%, respectivamente.
De otro lado, el trabajo con ovocitos donados representó 257 casos, con una TEC de 42,4% (36,8% en TED3 y 47,1% en TED5), y la transferencia diferida (75 casos) logró una TEC de 36,0% (tanto en TED3 como en TED5).
En el año 2011 iniciamos los procedimientos de IVM, siempre asociados a transferencia diferida. de 25,0%. Sin embargo, esta fue 44,0% cuando observamos solo el grupo de pacientes con ova rio poliquístico. En agosto de 2012 logramos el nacimiento de la primera niña peruana producto de esta técnica(11-13).
Dentro de las TRA, en los casos de azoospermia se realizó biopsia testicular para la obtención de espermatozoides y posterior ICSI. Hemos realizado este procedimiento en 14 parejas, logrando embarazo clínico en 5 (TEC de 35,7%), siendo el primer nacimiento producto de esta metodología en abril de 2012.
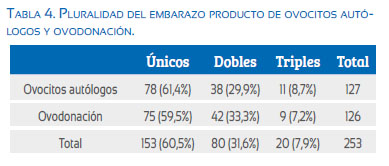
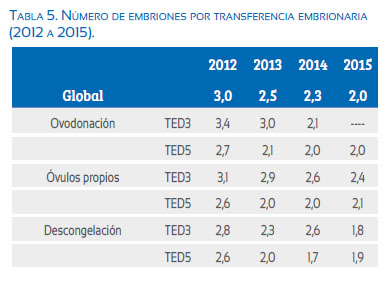
La Tabla 4 resume la pluralidad de los embarazos logrados, destacando el 31,6% de embarazo gemelar y 7,9% de embarazo triple del total de gestaciones. Esto depende del número de embriones transferidos.
El número de embarazos triples en los procedimientos con ovocitos autólogos con TED3 se observó en 6 ocasiones: 4 al transferir 3 embriones, 1 al transferir 4, y 1 al transferir 5; y con TED5, se observó en 5: uno al transferir 2 y 4 al transferir 3; y en las transferencias diferidas, no se presentaron. En los procedimientos de ovo-donación con TED3 se observó 4 embarazos triples al transferir 3 embriones; y con TED5, 2 al transferir 3; y en transferencias diferidas, con TED3, 3 al transferir 4, y con TED5, no se presentaron.
En los últimos años hemos disminuido el número de embriones transferidos, de tal forma que de 3 embriones por transferencia en el año 2012, en el 2015 transferimos 2 en promedio (Tabla 5). Así mismo, en los casos de ovodonación, desde el año 2015 hemos dejado la TED3 y solo realizamos TED5.
En el año 2015 tuvimos un embarazo triple (3,0% del total de embarazos), producto de la transferencia de 2 blastocistos, uno de los cuales se dividió hacia un gemelar monocigótico. El embarazo doble constituyó el 39,4% del total de embarazos en este último año.
Discusión
Entre los años 2005 al 2015, la TEC de FIV/ICSI con ovocitos autólogos en el CFGS (25,4% en FIV y 31,7% en ICSI, por transferencia embrionaria) fue similar a la reportada internacionalmente. En América Latina, para el año 2013, se reporta una TEC por aspiración de 31,5% en FIV y 25,8% en ICSI(14); en Europa, para el año 2011, 33,2% y 31,6%(15); y en el reporte mundial correspondiente al año 2006, 30,7% y 29,7%(16), respectivamente.
La TED3 en el CFGS se realiza cuando el número de ovocitos fecundados es menor de 6, generalmente en pacientes con una menor reserva ovárica. El desarrollo de ICSI nos permitió elevar la TEC en este grupo de pacientes, de 17,5% con FIV a 30,2% con ICSI (Tabla 2). En pacientes con TED5, la TEC se mantuvo igual (37,0% en FIV y 36,5% en ICSI). Para llevar el cultivo a blastocisto, la cantidad de embriones necesaria para ello es manifestación de una mejor reserva ovárica y, por ende, un mejor pronóstico.
Existen pocos estudios controlados y aleatorios que comparen la TED3 y la TED5. Sin embargo, la mayoría de ellos muestra que en pacientes con buen pronóstico las tasas de embarazo clínico son equivalentes, y las diferencias se encuentran en las tasas de implantación. En el CFGS, este grupo de pacientes es representado por las mujeres < 37 años, y la TEC es similar tanto en TED3 y TED5 (36,2 y 42,5%, respectivamente) (Tabla 3).
La población que requiere FIV/ICSI en el CFGS tiende a ser joven (45,8% son ≤ 34 años, y 14,7%, ≥ 40 años), a diferencia de lo observado en América Latina (29,2% son ≤ 34 años, y 30,9%, ≥ 40 años)(14). Esta distribución etárea puede expresar dos tendencias: o las pacientes desde edad temprana presentan indicaciones para FIV/ICSI, o las pacientes de mayor edad, al presentar pobre pronóstico, optan por ovodonación.
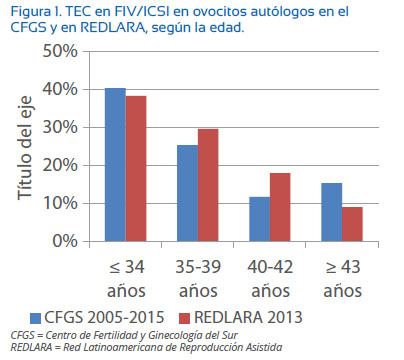
La TEC disminuye conforme mayor es la edad, de manera similar a lo observado en América Latina (Figura 1). En el CFGS consideramos los 37 años como la edad determinante, con una menor TEC en las mujeres ≥ 37 años(17), tanto en TED3 como en TED5 (17,6 y 11,8%, respectivamente) (tablas 2 y 3).
Sin embargo, la transferencia diferida de blastocistos en mujeres ≥ 37 años, logró una TEC comparable a la transferencia de blastocistos en fresco de mujeres < 37 años (38,9% y 42,5%, respectivamente) (Tabla 3). En las mujeres mayores, la TED3 tuvo una TEC baja tanto en fresco como en desvitrificación, posiblemente debido a factores relacionados a la calidad ovocitaria. Ello nos orienta a pensar que hay un grupo de mujeres ≥ 37 años con buen pronóstico de embarazo, en caso tengan una reserva ovárica suficiente como para la generación de blastocistos, pero en quienes la receptividad endometrial se ve afectada por la estimulación ovárica(17), siendo la transferencia diferida una mejor alternativa de manejo en este grupo específico.
Como el factor de la edad y RO son determinantes, la ovodonación surge como una alternativa cuando el pronóstico de embarazo con los ovocitos propios es muy pobre. La ovodonación en América Latina tiene una TEC de 47,3%, y de 38,2% con embriones desvitrificados(14), siendo tasas similares a las del CFGS (42,4% y 36,0%, respectivamente).
La transferencia diferida de embriones constituye el 25,6% del total de transferencias en el CFGS (198 transferencias de un total de 774). En los Estados Unidos, es 17%.
El desarrollo de IVM en el CFGS busca innovar alternativas efectivas, pero evitando las dosis elevadas y prolongadas de gonadotropinas, además de brindar una opción más confortable y económica para las parejas. La TEC es mejor en el grupo de pacientes con ovario poliquístico (44,0%), y considerando que este diagnóstico se encuentra asociado en el 18% de las pacientes que realizan FIV/ICSI(13), definitivamente el desarrollo de esta tecnología es prioridad en nuestro centro.
La disminución en el número de embriones transferidos por ciclo de FIV/ICSI es determinante en la menor frecuencia de embarazos múltiples, y en la morbi-mortalidad de los niños logrados por estos procedimientos.
En los Estados Unidos, en el año 2014, el 25% de los nacimientos logrados a través de FIV/ICSI fueron gemelares, 15 veces la frecuencia normal, de los cuales el 60% nació prematuramente y 50% presentó peso bajo al nacer. La incidencia de embarazos triples fue 3,7% en los años pasados y a la actualidad llega a ser 1% en mujeres < 35 años y cerca del 0,5% en mujeres entre los 38 a 42 años. En el CFGS, observamos un 31,6% de embarazo gemelar y 7,9% de embarazo triple, del total de gestaciones durante el periodo de los años 2005 a 2015.
Debido a nuestra elevada tasa de embarazo múltiple, hemos disminuido el número de embriones por transferencia (Tabla 5), y para el año 2015 hemos transferido solo 2 embriones en promedio. A nivel mundial se tiene esta tendencia, y muchos investigadores, instituciones y laboratorios recomiendan la transferencia de un solo embrión (eSET, por sus siglas en inglés). En América Latina se observa que de un promedio de 3,2 embriones por transferencia en el año 2000 se ha llegado a 2,2 en el año 2012(18).
La tasa de embarazo gemelar en el CFGS aún se mantiene elevada, en 39,4% el año 2015. Es nuestro compromiso evaluar y hacer una mejor selección de las pacientes con el objetivo de realizar eSET con mayor frecuencia y disminuir dicha tasa sin afectar la TEC.
Estos diez años en TRA de alta complejidad nos permite definir nuestra población como cronológicamente joven, pero que desarrolla dificultades de fertilidad que requieren de asistencia especializada con TRA, tanto de baja como de alta complejidad.
Asimismo, el manejo de la paciente ≥ 37 años es un desafío. El desarrollo de ICSI así como la transferencia diferida de blastocistos nos ha permitido mejorar los resultados en este grupo de pacientes. Otras estrategias a evaluar son la transferencia de mayor número de embriones y el banking de ovocitos(19) o embriones.
Referencias Bibliográficas
1. Roa-Meggo Y. La infertilidad como problema de salud pública en el Perú. Rev peru ginecol obstet. 2012;58(2):79-85. [ Links ]
2. Hackett PH, Roach RD. High altitude medicine and physiology. en: Auerbach OS, ed. Wilderness Medicine. Philadelphia, PA: Elsevier; 2012:2-32. [ Links ]
3. Gonzales GF, Gasco M, Córdova A, Chung A, Rubio J, Villegas L. Effect of high altitude exposure on spermatogenesis and epididymal sperm count in male rats. J Endocrinol. 2004;180:87-95. [ Links ]
4. Reynafarje C. La adaptación a las grandes alturas. Contribución peruana a su estudio. Lima. Propaceb. 1990. [ Links ]
5. Gonzales GF. Endocrinología en las grandes alturas. Acta Andina. 1994;3(2):83-111. [ Links ]
6. INEI. Censos Nacionales 2014, XI de Población, VI de Vivienda 2014. [ Links ]
7. Mascarenhas MN, Flaxman SR, Boerma T, Vanderpoel S, Stevens GS. National, regional and global trends in infertility prevalence since 1990: A systematic analysis of 277 health surveys. PLoS Med. 2012;9(12):e1001356. doi:10.1371/journal. pmed.1001356. [ Links ]
8. Vargas L, Pella R, Perez, Y. Fertilización in vitro en la altura. Rev peru ginecol obstet. 2007;53(1):18-21. [ Links ]
9. Vargas-Tominaga L, Vargas-Lechuga A, Pella R, Sierra J. Fertilización in vitro y transferencia de embriones. Experiencia de un programa de reproducción asistida, a 3330 metros sobre el nivel del mar. Rev peru ginecol obstet. 2009;55:126-8. [ Links ]
10. Kuwayama M, Vajta G, Ieda S, Kato O. Comparison of open and closed methods for vitrification of human embryos and the elimination of potential contamination. Reprod Biomed Online. 2005;11:608-14. [ Links ]
11. Vargas-Tominaga L, Pella-Caceres R, Vargas-Lechuga A, Bartolo- Duran L. Embarazo mediante tratamiento de maduración in vitro de ovocitos en paciente amenorreica y con historia de anorexia nervosa. Rev peru ginecol obstet. 2012;58:133-6. [ Links ]
12. Vargas L, Pella R, Vargas A, Bartolo L. Maduración in vitro de ovocitos: alternativa efectiva en reproducción asistida. Rev peru ginecol obstet. 2012;58:263-6. [ Links ]
13. Vargas L, Pella R, Vargas J, Bartolo L, Serrano M. In vitro maturation of oocytes in high altitude women with polycystic ovaries. JBRA Assist Reprod. 2015;19(2):83-6. [ Links ]
14. Zegers-Hochschild F, Schwarze JE, Crosby JA, Musri C, Urbina MT on behalf of the Latin America Network of Assisted Reproduction (REDLARA). Assisted reproductive techniques in Latin America: the Latin American Registry, 2013. Reproductive BioMedicine Online (2016). doi: 10.1016/j. rbmo.2016.02.012. [ Links ]
15. ESHRE. Assisted reproductive technology and intrauterine inseminations in Europe, 2011: results generated from European registers by ESHRE, presented at 2014 Annual Meeting of ESHRE, Munich. [ Links ]
16. Mansour R, Ishihara O, Adamson GD, Dyer S, de Mouzon J, Nygren KG, Sullivan E, Zegers-Hochschild F. International Committee for Monitoring Assisted Reproductive Technologies world report: Assisted Reproductive Technology 2006. Hum Reprod. 2014;29(7):1536-51. [ Links ]
17. Vargas L, Pella R, Bartolo L, Vargas A, Vargas A, Pella A. Blastocyst transfer in women over 35 years of age not achieve pregnancy: Experience at 11,000 feet above sea level. Fertil Steril. 2013;100(3):S500. [ Links ]
18. Red Latinoamericana de Reproducción Asistida. [en línea]. [Fecha de consulta: 10 Julio 2016]. Disponible en: www. rla-registry.org. [ Links ]
19. Cobo A, Garrido N, Crespo J, Remohí J, Pellicer A. Accumulation of oocytes: a new strategy for managing low-responder patients. Reprod Biomed Online. 2012;24:424-32. [ Links ]
El material no ha sido presentado anteriormente a ningún medio de publicación. Financiamiento propio.
No existe conflicto de interés en ninguno de los autores.
Trabajo de investigación que obtuvo el Segundo Premio de la Sección Temas Libres del XXI Congreso Peruano de Obstetricia y Ginecología, Lima, Perú, octubre de 2016.
Correspondencia: Dr. Luis Vargas Tominaga Centro de Fertilidad y Ginecología del Sur, Urbanización Mariscal Gamarra B-11 Segunda Etapa, Cusco, Perú