Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista Peruana de Ginecología y Obstetricia
On-line version ISSN 2304-5132
Rev. peru. ginecol. obstet. vol.65 no.3 Lima July/Dec 2019
http://dx.doi.org/10.31403/rpgo.v66i2182
ARTÍCULO ORIGINAL
Correlación entre el diagnóstico ecográfico prenatal y posnatal en casos de hidronefrosis fetal
Correlation between prenatal and postnatal ultrasound diagnosis of fetal hydronephrosis
Anna Vilà Famada1,2,a, Silvia Pina Pérez2,b, Jordi Costa Pueyo2,b,c, Laura Serra Azuara2,b
1 Servicio de Ginecología y Obstetricia y Unidad de Diagnóstico Prenatal. Parc Taulí Hospital Universitario, Barcelona, España
2 Instituto de Investigación y Innovación Parc Taulí I3PT. Universidad Autónoma de Barcelona. Sabadell (08208), España
a Médico residente de tercer año
b Médico adjunto
c Professor asociado
ABSTRACT
Introduction: Prenatal ultrasound detects fetal anomalies in 1% of pregnancies, about 20-30% of them are urogenital and among them 50% are fetal urinary tract dilatations (UTD). Objective: To establish the correlation between prenatal and postnatal hydronephrosis diagnosis, as well as to analyze the prognosis. Design, patients, interventions and main outcome measure: Retrospective observational study performed by the Prenatal Diagnosis Unit of Parc Taulí Hospital (Sabadell), which included 177 pregnant women with ultrasound diagnosis of UTD between January 2011 and December 2016. We performed a descriptive analysis of the most important ultrasound and perinatal variables. The main outcome measure was the degree of dilatation of UTD. Results: The prevalence of HNF was 1.17%; 82.8% were diagnosed in the second trimester ultrasound; 42.9% of fetal hydronephrosis cases were bilateral and, in 95.6%, the urogenital pathology was not associated with other malformations. Congenital heart disease was the most frequently associated prenatal anomaly (3.3%). Among 93 low-risk hydronephrosis cases diagnosed in the second trimester, 53.8% resolved spontaneously in the third trimester, 30.1% remained stable and 16.1% worsened. Of the 32 cases of moderate-severe UTD diagnosed in the second trimester, only 9.4% improved in the third trimester. Complementary examination was required in 46.9% of the neonates and 14.1% required surgical intervention. Conclusions: Most cases of fetal hydronephrosis were diagnosed by second trimester ultrasound. Mild UTD presents good prognosis as opposed to moderate-severe cases, which usually persist after birth.
Key words: Urinary tract dilatation, Fetal hydronephrosis, Prenatal diagnosis.
RESUMEN
Introducción. La ecografía prenatal permite detectar una anomalía significativa en 1% de los embarazos; de ellos, 20 a 30% son genitourinarias y 50% de estas son hidronefrosis fetales (HNF). Objetivo. Establecer una correlación entre el grado de hidronefrosis prenatal y posnatal, así como analizar las implicaciones pronósticas. Diseño, pacientes, intervenciones y variables principales. Estudio observacional retrospectivo realizado por la Unidad de Diagnóstico Prenatal del hospital Parc Taulí de Sabadell, que incluyó un total de 177 gestantes con diagnóstico ecográfico de HNF entre enero de 2011 y diciembre de 2016. Se realizó un análisis descriptivo de las variables ecográficas y perinatales más importantes. La principal variable de estudio fue el grado de dilatación de la HNF. Resultados. La prevalencia de HNF fue 1,17%. El 82,8% de los casos fue diagnosticado en la ecografía del 2º trimestre. En 42,9%, la afectación fue bilateral, y en 95,6% la malformación renal fue aislada. La cardiopatía fue la anomalía congénita asociada con más frecuencia (3,3%). De las 93 hidronefrosis de riesgo bajo diagnosticadas en el 2º trimestre, 53,8% se normalizaron en el 3er trimestre, 30,1% permanecieron estables y 16,1% progresaron. De los 32 casos de HNF moderadas-severas diagnosticadas en el 2º trimestre, solo 9,4% se normalizaron en el 3er trimestre. El 46,9% de los neonatos precisó exploraciones complementarias y 14,1% intervención quirúrgica. Conclusiones. Existe buena correlación de la HNF prenatal y posnatal. La HNF leve presenta buen pronóstico, mientras que la moderada-severa suele persistir posnatalmente.
Palabras clave. Dilatación urinaria, Hidronefrosis fetal, Diagnóstico prenatal.
Introducción
La hidronefrosis fetal (HNF) consiste en la dilatación de la pelvis renal fetal, con o sin dilatación de los cálices renales, debido a dificultad en la eliminación de la orina. Su prevalencia es 0,6 a 5,4%(1-6).
La identificación prenatal de esta patología permite detectar aquellos casos que pueden presentar complicaciones en la vida posnatal y prevenirlas con conductas diagnósticas y terapéuticas precoces.
Existen múltiples clasificaciones para el diagnóstico y seguimiento de la HNF, todas ellas basadas en la dilatación de la vía urinaria fetal objetivadas por medio de la ecografía prenatal. Una de las más utilizadas es la clasificación descriptiva de la Sociedad de Urología Fetal(7). También es muy utilizada la clasificación de Nguyen(8), más cuantitativa, basada en el diámetro antero-posterior (APRPD) de la pelvis renal.
En 2014, se publicó un consenso con la intención de unificar los criterios para un adecuado manejo y seguimiento perinatal: UTD classification system(9-10).
Diferentes estudios han demostrado que la ecografía es el mejor método de seguimiento posnatal(11). Los recién nacidos con HNF severas (UTD A2 o A3 a nivel prenatal o P2 o P3 a nivel posnatal) requerirán mayor seguimiento, estudio y prevención, necesitando pruebas funcionales renales y tratamiento antibiótico profiláctico para evitar infecciones del tracto urinario(12,13). En líneas generales, el abordaje de la patología congénita del tracto urinario requiere de un manejo multidisciplinar que implique a ginecoobstetras, genetistas, radiólogos, neonatólogos y cirujanos pediátricos. Existen entidades con carácter hereditario (1 a 3% de los casos con aumento del riesgo de trisomías 21(14)); en otras ocasiones puesto describir el comportamiento de las HNF fetales de diagnóstico prenatal en nuestra población, su asociación con otras malformaciones y cromosomopatías y las implicaciones en la vida posnatal.
Método
Estudio observacional retrospectivo de las hidronefrosis diagnosticadas per ecografía prenatal, entre enero de 2011 y diciembre de 2016, en el hospital Parc Taulí de Sabadell. Las variables más importantes estudiadas han sido el grado de HNF y la edad gestacional. Se ha realizado análisis descriptivo de la media, el intervalo y la desviación estándar para las variables continuas y un análisis de frecuencias absolutas y porcentajes para las variables categóricas.
Resultados
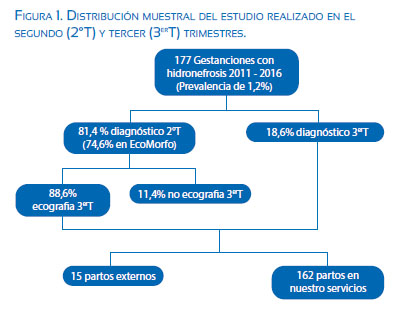
Del total de 15 130 partos durante el periodo de estudio, se ha diagnosticado 177 gestantes que portaban fetos con hidronefrosis. De ellas, en 151 (85,3%) se pudo realizar un seguimiento completo (figura 1). La prevalencia de la HNF fue 1,17%. La edad media de las gestantes fue 31,5+/-5,8 años. El 36,2% era nulípara.
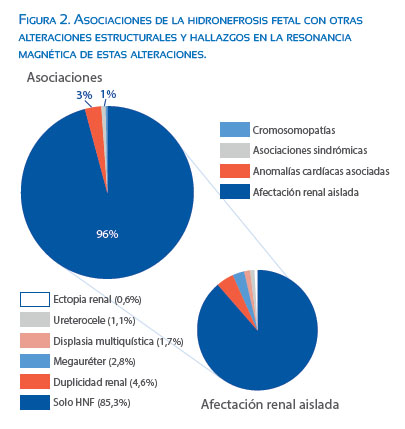
En 57,1% de los casos, el diagnóstico fue de alteración unilateral, con mayor afectación del riñón izquierdo (32,4%) que del derecho (23,9%). El 82,8% de las hidronefrosis fetales se diagnosticaron en el 2º trimestre, en la 23,6 +/6,1 semanas de gestación. El 17,2% fue diagnosticado durante el 3er trimestre. En 14,7% de los casos, la HNF se asociaba con anomalías congénitas del riñón y tracto urinario (figura 2).
En 95,7% de los casos, la malformación renal fue aislada. En el resto (4,3%), se diagnosticaron anomalías estructurales asociadas. La cardiopatía congénita fue la malformación fetal asociada a la HNF diagnosticada con más frecuencia. Se detectó en 3,3% de los fetos. La ecocardiografía fetal confirmó el diagnóstico en todos los casos, encontrando dos comunicaciones interventriculares, una insuficiencia cardíaca, una insuficiencia tricuspídea y una discordancia de cavidades cardíacas.
En 19,2% de las gestaciones con HNF se realizaron pruebas invasivas, sin detectar cromosomopatías asociadas.
En 29 casos (16,4%), se realizó resonancia magnética (RNM) fetal. En 23 de ellos, la RNM aportó información adicional de la alteración renal fetal.
Solo en un caso, la gestante solicitó la interrupción legal de la gestación, dado que el feto presentaba múltiples malformaciones.
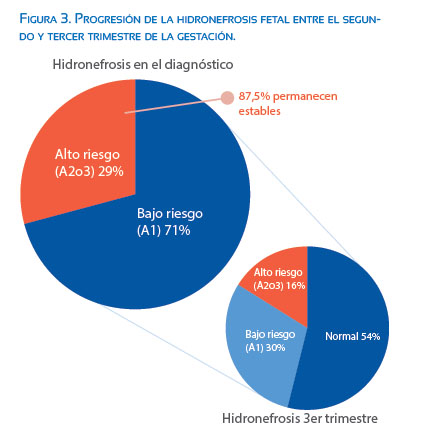
Diagnosticamos 93 HNF de bajo riesgo (A1), en el segundo trimestre de la gestación. En el seguimiento de estas gestantes durante el III trimestre, observamos que en 53,8% de los casos la HNF desapareció, en 30,1% permaneció estable y en 16,1%, la patología renal progresó.
Si analizamos el subgrupo A1 de las HNF que aún persistían durante el tercer trimestre, el 35% de los casos retornó a la normalidad posparto, siendo el estudio ecográfico posnatal normal.
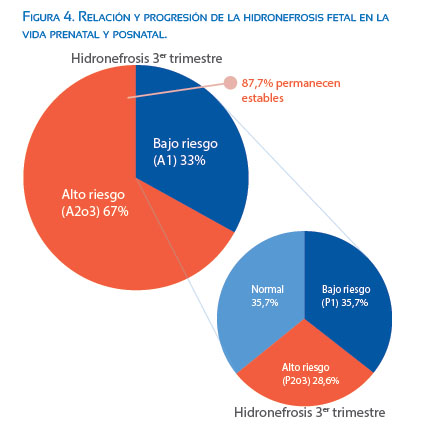
Diagnosticamos 32 HNF de alto riesgo (A2 o A3), en el segundo trimestre de la gestación. Solo 9,4% se normalizaron a lo largo del tercer trimestre y un caso retronó a la normalidad espontáneamente postparto (figuras 3 y 4).
La relación varón-mujer fue 2:1 entre los recién nacidos del estudio. La edad gestacional media del parto fue 39,2 +/- 2,1 semanas, y el peso neonatal medio 3 275,5 +/- 535,1 gramos (percentil 53,9 +/- 26,3). Si comparamos estos datos con la población obstétrica general, no encontramos diferencias, ni tampoco en la vía del parto, prematuridad y prueba de Apgar.
Para el estudio de la hidronefrosis en la vida posnatal, de igual manera que en la vida intrauterina, se utilizó la ecografía renal. Del total de neonatos con HNF, solo hallamos alteraciones renales en la ecografía en la mitad de ellos (76). En 46,9% de los neonatos se realizaron otras exploraciones complementarias: 74 urosonografías (15 de ellas diagnosticaron reflujo vesicoureteral) y 43 renogramas, con resultado patológico en 28 de ellos.
El 14,1% de los recién nacidos con diagnóstico de HNF en la vida prenatal requirieron intervención quirúrgica. Se realizaron 9 pieloplastias Andersen-Hynes, 5 heminefrectomías, 4 nefrectomías totales, 4 reimplantaciones de megauréteres y en 3 casos, intervenciones combinadas.
Además, diagnosticamos posnatalmente un síndrome de Pierre-Robin.
Discusión
El significado clínico del grado de dilatación del tracto urinario prenatal sigue siendo incierto y el tratamiento posnatal aún no está del todo claro. En la mayoría de los casos, la dilatación renal se estabiliza o se resuelve sin que haya insuficiencia renal o válvulas de uretra posterior que requieran intervención. Aun así, hay casos en los que esta patología evoluciona; la hidronefrosis puede ser un predictor de patología renal subyacente.
El seguimiento y la conducta en estos neonatos sigue siendo debatidas al día de hoy. Existe una variabilidad importante en el manejo clínico de los neonatos con dilatación del tracto urinario prenatal, debido a la falta de consenso y uniformidad en la definición y clasificación de la dilatación del tracto urinario(7,8). Con el consenso publicado en 2014 por la UTD classification system(9), en el que participaron varias sociedades científicas internacionales (American College of Radiology, American Institute of Ultrasound in Medicine, American Society of Pediatric Nephrology, Society for Fetal Urology, Society for Maternal-Fetal Medicine, Society for Pediatric Urology, Society for Pediatric Radiology y la Society of Radiologists in Ultrasounds), se empezó a establecer pautas para unificar criterios. Los fetos con UTD A1, con un diámetro antero-posterior (DAP) de la pelvis renal de 4 a 7 mm en <28 semanas y de 7 a 10 mm en ≥28 semanas, son considerados de bajo riesgo para las uropatías posnatales. A los fetos con UTD A2–3 se les considera de mayor riesgo para uropatía posnatal, con un DAP de la pelvis renal ≥7 mm a las <28 semanas y ≥10 mm a las ≥28 semanas. Esta última clasificación incluye parámetros ecográficos que permiten prever la evolución desfavorable de la HNF, como son: el oligohidramnios, la alteración en el parénquima cortical renal o la precocidad del diagnóstico prenatal (antes de las 24 semanas de gestación)(10).
Se ha objetivado que, si la HNF se diagnostica en el 2º trimestre y no va acompañada de otras malformaciones fetales, únicamente presentarán patología posnatal en 12% de los casos. Pero, si el hallazgo de HNF es objetivado en el 2º trimestre y persiste o progresa durante el 3er trimestre, pueden llegar a presentar patología posnatal el 40% de los fetos(15). En múltiples ocasiones, estos fetos son candidatos a estudios adicionales, que pueden incluir: ecocardiografía, estudio cromosómico y RNM, con la intencionalidad de descartar alteraciones asociadas. Es conocida la asociación de cardiopatías congénitas a otras malformaciones extracardíacas. Egbe y col. reportan en su serie un 3,9% de casos en los cuales la cardiopatía congénita se presentó asociada a una anomalía de tracto urinario(16). En nuestra casuística, 3,3% de los fetos presentaron además de la HNF otras malformaciones estructurales, todas ellas cardiopatías congénitas.
En nuestra serie observamos que en más de la mitad de los casos las hidronefrosis afectaban a varones (64,8%), tal y como se especifica en la literatura y publican autores como Ismaili, en el 2002(15). En esta publicación se comentó también el mayor riesgo de trisomía 21 en casos de hidronefrosis renal transitoria prenatal y la necesidad de un estudio ecográfico más exhaustivo para detectar cambios relacionados con aneuploidías. Estamos de acuerdo con el hecho de que la dilatación piélica fetal leve puede alertar sobre aneuploidías, pero recomendamos aplicar un sonograma genético en tales casos para corroborar el riesgo de trisomía, y solo en casos de alto riesgo recurrir a una técnica de diagnóstico prenatal invasivo(17). La aplicación de este sonograma genético fue el motivo por el cual en nuestra serie solo realizamos estudio cromosómico en 19,2% de los fetos. Así, el estudio cromosómico se realizó en fetos en que, o bien eran HNF de grado severo (UTD A3) de diagnóstico precoz o bien se obtuvo un riesgo elevado para trisomía 21, después de realizar un sonograma genético y modificar el riesgo del cribado combinado por likelihood ratio (LR)(18,19). En el resto de casos, no fue necesario realizar estudio cromosómico. La correlación entre trisomía 21 e hidronefrosis renal prenatal no se ha confirmado en nuestro trabajo, ya que no se detectaron cromosomopatías en ninguno de los fetos estudiados intraútero, ni tampoco en los recién nacidos.
La mayoría de las HNF tiene buen pronóstico, existiendo una resolución prenatal de la patología en 80% de los casos, si la HNF es leve. En la revisión sistemática y metaanálisis publicado en 2006(11) por Sidhu, este autor objetivó que más del 70% de los casos de hidronefrosis leves diagnosticadas prenatalmente permanecen estables o incluso mejoran durante la vida fetal y en el seguimiento posnatal, sugiriendo que la hidronefrosis fetal leve podría tratarse de una patología relativamente benigna. En nuestro estudio hemos obtenido resultados similares a los publicados por Sidhu; los casos de hidronefrosis leves (UTD A1) diagnosticados en el 2º trimestre han presentado buen pronóstico y solo en 20,7% la patología renal progresó, presentando el recién nacido una afectación posnatal de moderado-alto riesgo (UTD P2oP3). En esta misma publicación, Sidhu y col.(11) especificaban que no podían concluir el pronóstico de las hidronefrosis graves, dada la amplia variabilidad de los trabajos existentes en la literatura. En nuestra serie, las hidronefrosis graves (UTD A2oA3) diagnosticadas en el 2º o 3er trimestre, permanecieron estables en 87% de los casos y requirieron de estudios adicionales, con la intencionalidad de identificar aquellos casos de reflujo vesicoureteral e instaurar tratamiento antibiótico profiláctico para reducir el riesgo de infección, coincidiendo plenamente en este aspecto con lo publicado por autores como Estrada(13).
No obstante, en nuestro centro, a diferencia de lo que propone este último autor, no realizamos cistouretografía miccional, sino que practicamos urosonografía miccional seriada, por considerarla una técnica segura para el estudio de la vía urinaria en pediatría. Por este motivo, la hemos realizado en la totalidad de nuestros niños afectos de hidronefrosis posnatal persistente, y en 20,3% de los casos hemos objetivado un reflujo vesicoureteral, pudiendo así caracterizar mejor la patología de forma totalmente inocua(20). El 40,3% de los niños que presentaba hidronefrosis severa posnatal (UTD P2oP3), tuvieron también alteraciones en el renograma. Estos datos reafirman el peor pronóstico de las hidronefrosis graves y concuerdan con lo publicado por autores como Ismaili(15) y Kumar(21). Coincidimos con Perlman(22) en el hecho de que el pronóstico renal fue peor en aquellos casos en los que la HNF se asoció con otras anomalías congénitas del riñón. La hidronefrosis fetal presenta un amplio espectro clínico posnatal, que se ve influenciado por la presencia de hallazgos ecográficos asociados con otras anomalías congénitas del riñón y del tracto urinario, otras malformaciones y/o síndromes genéticos que condicionarán el pronóstico renal.
Conclusiones
Existe una buena correlación en el diagnóstico, estadificación y pronóstico de la HNF entre el estudio prenatal y el posnatal.
La HNF leve presenta un buen pronóstico, mientras que la HNF moderada-severa suele persistir posnatalmente y precisa de seguimiento posterior.
Aspectos éticos
No hay conflictos éticos. Se trata de un estudio que no identifica al individuo, garantizando la confidencialidad de los datos. Se ha realizado disociación de los datos con el fin de recoger de forma totalmente anónima.
Los investigadores declaran que no tienen conflictos de interés.
Los investigadores declaran que no ha habido prestación económica por parte del promotor o de ninguna entidad externa en relación con el estudio realizado.
Agradecimientos
A todo el servicio de Ginecología y Obstetricia, especialmente a la Unidad de Diagnóstico Prenatal, así como al servicio de Pediatría del Hospital Universitario Parc Taulí de Sabadell, por el seguimiento de los pacientes tanto de las gestantes como de los niños.
Los autores del presente trabajo manifiestan que:
El manuscrito remitido en exclusiva a la Revista Peruana de Ginecología y Obstetricia de forma que no está siendo sometido a consideración en ninguna otra publicación y no ha sido publicado previamente.
Los autores son responsables de la investigación y han participado en su concepto, diseño, análisis e interpretación de los datos, escritura y corrección del manuscrito,asícomoenelaprobadodefinitivo que ha sido enviado a la Revista Peruana de Ginecología y Obstetricia
Los autores notifican que no existe conflicto de intereses en relación a su manuscrito.
Citar como:Vilà Famada A,Pina Pérez S, Costa Pueyo J, Serra Azuara L. Correlación entre el diagnóstico ecográfico prenatal y posnatal en casos de hidronefrosis fetal. Rev Peru Ginecol Obstet. 2019;65(3):279-284. DOI: https://doi.org/10.31403/rpgo.v66i2182
Referencias Bibliográficas
1. Mallik M, Watson AR. Antenatally detected urinary tract abnormalities: More detection but less action. Pediatr Nephrol. 2008;23:897–904. DOI:10.1007/s00467-008-0746-9. [ Links ]
2. Dudley JA, Haworth JM, McGraw ME, Frank JD, Tizard EJ. Clinical relevance and implications of antenatal hydronephrosis. Arch Dis Child Fetal Neonatal Ed. 1997;76:31–4. DOI:10.1136/fn.76.1.F31. [ Links ]
3. Kim EK, Song TB. A study on fetal urinary tract anomaly: Antenatal ultrasonographic diagnosis and postnatal follow-up. J Obstet Gynaecol Res.1996;22:569–73. DOI:10.1111/j.1447-0756.1996.tb01072.x. [ Links ]
4. Ek S, Lidefeldt KJ, Varricio L. Fetal hydronephrosis; prevalence, natural history and postnatal consequences in an unselected population. Acta Obstet Gynecol Scand. 2007;86:1463–6. DOI:10.1080/00016340701714802. [ Links ]
5. Livera LN, Brookfield DS, Egginton JA, Hawnaur JM. Antenatal ultrasonography to detect fetal renal abnormalities: A prospective screening programme. BMJ. 1989;298:1421–3. DOI:https://doi.org/10.1136/bmj.298.6685.1421. [ Links ]
6. Sairam S, Al-Habib A, Sasson S, Thilaganathan B. Natural history of fetal hydronephrosis diagnosed on mid-trimester ultrasound. Ultrasound Obstet Gynecol. 2001;17:191–6. DOI:10.1046/j.1469-0705.2001.00333.x. [ Links ]
7. Fernback SK, Maizels M, Conway JJ. Ultrasound grading of hydronephrosis: introduction to the system used by the Society for Fetal Urology. Pediatric Radiology. 1993; 23: 478-80. DOI:https://doi.org/10.1007/BF02012459, [ Links ]
8. Nguyen HT, Herndon CD, Cooper C, Gatti J, Kirsch A, Kokorowski P, et al. The Society for fetal Urology consensus statement on the evaluation and management of antenatal hydronephrosis. J Ped Urol. 2010;6:212-31. DOI:10.1016/j.jpurol.2010.02.205. [ Links ]
9. Nguyen HT. Multidisciplinary consensus on the classification of prenatal and postnatal urinary tract dilation (UTD classification system). Pediatric Radiology, Multidisciplinary consensus on the classification of antenatal and postnatal urinary tract dilation (UTD classification system). J Pediatr Urol. 2014 Dec;10(6): 982-98. DOI:10.1016/j.jpurol.2014.10.002. [ Links ]
10. Morris RK, Malin GL, Khan KS, Kilby MD. Antenatal ultrasound to predict postnatal renal function in congenital lower urinary tract obstruction: systematic review of test accuracy. BJOG 2009;116:1290-9. DOI:10.1111/j.1471-0528.2009.02194.x. [ Links ]
11. Sidhu G, Beyene J, Rosenblum ND. Outcome of isolated antenatal hydronephrosis: a systematic review and metaanalysis. Pediatr Nephrol. 2006;21:218-24. DOI:10.1007/s00467-0052100-9. [ Links ]
12. Braga LH, Mijovic H, Farrokhyar F, Pemberton J, DeMaria J,Lo- renzo AJ. Antibiotic prophylaxis for urinary tract infections in antenatal hydronephrosis. Pediatrics. 2013;131:251-61. DOI:10.1542/peds.2012-1870. [ Links ]
13. Estrada CR, Peters CA, Retik AB, Nguyen HT. Vesicoureteral reflux and urinary tract infection in children with a history of prenatal hydronephrosis-should voiding cystourethrography be performed in cases of postnatally persistent grade II hydronephrosis? J Urol. 2009;181:801–6. DOI:10.1016/j.juro.2008.10.057. [ Links ]
14. Bromley B, Lieberman E, Shipp TD, Benacerraf BR. The genetic sonogram: a method of risk assessment for Down syndrome in the second trimester. J Ultrasound Med. 2002;21:108796. DOI:10.7863/jum.2002.21.10.1087. [ Links ]
15. Ismaili K, Avni FE, Hall M, Brussels Free University Perinatal Nephrology Study G. Results of systematic voiding cystourethrography in infants with antenatally diagnosed renal pelvis dilation. J Pediatr. 2002;141:21-4. DOI:10.1067/mpd.2002.125493. [ Links ]
16. Egbe A, Lee S, Ho D, Uppu S. Prevalence of congenital anomalies in newborns with congenital heart disease diagnosis. Ann Pediatr Cardiol. 2014 May;7(2):86-91. DOI:10.4103/09742069.132474. [ Links ]
17. Agathokleous M, Chaveeva P, Poon LC, Kosinski P, Nicolaides KH. Meta-analysis of second-trimester markers for trisomy 21. Ultrasound Obstet Gynecol. 2013 Mar;41(3):247-61. DOI:10.1002/uog.12364. [ Links ]
18. Shamshirsaz AA, Ravangard SF, Turner G, Borgida A, Janicki MB, Campbell WA, et al. Efficacy of the genetic sonogram in a stepwise sequential protocol for down syndrome screening. J Ultrasound Med. 2013 Sep;32(9):1607-13. DOI:10.7863/ultra.32.9.1607. [ Links ]
19. Odibo AO, Ghidini A. Role of the second-trimester 'genetic sonogram' for Down syndrome screen in the era of first-trimester screening and noninvasive prenatal testing. Prenat Diagn. 2014 Jun;34(6):511-7. DOI:10.1002/pd.4329. [ Links ]
20. Duran C, Del Riego J, Riera L. Serial voiding urosonography: a safe technique for the study of the entire urinary tract in children. Radiologia. 2013 Mar-Apr;55 (2):160-6. DOI:10.1016/j.rx.2012.03.002. [ Links ]
21. Kumar M, Gupta U, Thakur S, Aggrawal S, Meena J, Sharma S, et al. Prenatal sonographic evaluation and postnatal outcome of renal anomalies. Indian J Hum Genet. 2012;18:75–82. DOI:10.4103/0971-6866.96656. [ Links ]
22. Perlman S, Roitman L, Lotan D, Kivilevitch Z, Pode-Shakked N, Pode-Shakked B, et al. Severe fetal hydronephrosis: the added value of associated congenital anomalies of the kidneys and urinary tract (CAKUT) in the prediction of postnatal outcome. Prenat Diagn. 2018 Feb;38(3):179-83. DOI:10.1002/pd.5206. [ Links ]
Correspondencia:
Anna Vilà Famada
Calle Mallorca nº10 Alella (08328), Barcelona
669457829
Recibido: 25 febrero 2019
Aceptado: 5 abril 2019
Publicación online: 22 julio 2019