INTRODUCCIÓN
La testosterona es el andrógeno derivado del colesterol con mayor presencia en los varones, siendo del total de testosterona circulante, el 95% (6 a 7 mg / día). Es producido por las células de Leydig en los testículos1,2.
Los principales efectos de la testosterona son dos: androgénicos y anabólicos. Los efectos androgénicos están relacionados a las características sexuales masculinas, en cambio, los efectos anabólicos se encargan de la formación de proteínas, principalmente el aumento de la masa muscular3.
Un grupo de hormonas esteroideas, químicamente similares, son los esteroides androgénicos anabólicos (EAA)4, los cuales fueron creados para minimizar los efectos androgénicos y maximizar los anabólicos favoreciendo el crecimiento de músculos esqueléticos5.
Entre los usos terapéuticos de los EAA tenemos la restauración de la masa muscular en el tratamiento de la caquexia asociada con quemaduras graves, insuficiencia renal y SIDA. Además se utilizan como sustitutos hormonales en hombres con hipogonadismo o niveles bajos de testosterona circulante3,6. Sin embargo, en deportistas masculinos jóvenes es frecuente la auto-administración para mejorar sus condiciones físicas, así como también en fisicoculturistas que quieren mejorar su apariencia física aumentando su masa muscular7.
Actualmente, los estudios muestran que el uso de EEA es frecuente, y cuatro de cada cinco personas no son deportistas y los utilizan sólo con fines cosméticos8, así también existe evidencia que su uso para mejorar el rendimiento y adquirir más musculatura está incrementándose a nivel mundial. Solo en EEUU. al menos dos millones de personas utilizan o han utilizado EAA9, por otro lado la prevalencia en países como Noruega, Argentina y Polonia fueron 3,6%, 6,5% y 6,2% respectivamente10-12, es mayor.
Cuando los EAA son administrados bajo prescripción médica no presentan riesgos, pero en atletas que abusan de andrógenos, desde 1988 se han reportado estos efectos secundarios graves13. Entre los de mayor riesgo está el infarto de miocardio, especialmente en levantadores de pesas14. También se encuentran el accidente cerebrovascular, hipertrofia ventricular izquierda y muerte cardíaca súbita. A nivel hepático se ha reportado obstrucción del conducto biliar y un mayor riesgo de tumores3. Todos estos casos apoyan la idea de que los andrógenos exógenos pueden ser trombogénicos15.
Los estudios electrocardiográficos muestran que dosis muy altas de EAA modifican el funcionamiento fisiológico del sistema cardiovascular por ello que se requiere investigar la relación que existe entre la concentración de testosterona endógena y sus posibles efectos en el origen de trombosis cardiovascular16. La terapia con testosterona también se ha asociado con un aumento de la expresión del receptor de tromboxano A2 en las plaquetas, además de un aumento de la agregación plaquetaria, lo que potencialmente crea un mayor riesgo de formación de trombos15.
El objetivo de este trabajo fue determinar el efecto del metabolito de la testosterona en la cuantificación de plaquetas en ratas ORX con o sin reemplazo de DHT.
MATERIAL Y MÉTODOS
1. Animales
Este estudio se realizó en ratas Wistar macho de 200 a 300 gr obtenidas del Bioterio - Universidad Católica de Santa María. Los procedimientos experimentales y protocolos fueron aprobados por el Comité de Ética de la Universidad Católica de Santa María y están en concordancia con el manual de IASP para el estudio de dolor en animales17. Los animales fueron alojados en el Bioterio, en jaulas metálicas (cinco ratas / jaula) en una habitación con temperatura de ambiente controlada (23 ± 1 ° C) en un ciclo de luz claro-oscuro 12:12, con comida y agua disponibles ad libitum.
2. Orquidectomía (ORX)
Ratas macho wistar de 45 días de edad fueron sometidas a orquidectomización con una incisión simple escrotal. El procedimiento fue desarrollado bajo anestesia inducida por una inyección intramuscular de una mezcla de ketamina (55 mg / kg) y xilazina (5.5 mg / kg). Se usó una inyección subcutánea de ketoprofeno (5 mg / kg) para la analgesia postoperatoria18. Las ratas con orquidectomia (ORX) fueron sometidas a experimentación luego de 4 semanas después de la cirugía. Las ratas sham operadas se sometieron a un procedimiento quirúrgico similar al de las ratas ORX, excepto que las gónadas no fueron removidas.19,20
3. Administración hormonal
A los 2 meses y medio de edad, las 24 ratas fueron divididas en 4 grupos de estudio (6 ratas en cada grupo). El grupo con 12 ratas macho ORX, fue constituido por 6 animales que recibieron reemplazo hormonal con propionato de dihidrotestosterona (DHT) a dosis de 2 mg / kg a través de una inyección subcutánea durante 7 días y, por 6 animales que recibieron solución fisiológica (0.9% NaCl)21. Otro grupo paralelo con 12 machos no ORX, a los que se les denominó ratas SHAM (simuladas), siendo que 6 recibieron administración subcutánea diaria de propionato de DHT en una dosis de 2 mg / kg y la otra mitad suero fisiológico (0.9% NaCl) durante 7 días. La administración sistémica de DHT, en ratas ORX, se realizó como reemplazo para equiparar niveles fisiológicos compatibles con el observado en las sham21. Para determinar si la DHT induce un aumento en la cuantificación de plaquetas se administró en ratas ORX o sham DHT (2mg/kg) y en ratas ORX o sham NaCl (0.9%)
RESULTADOS
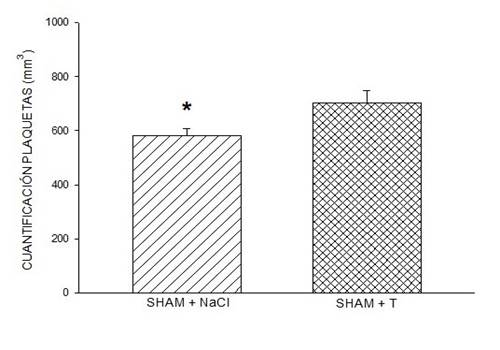
Figura 1: Efecto de la testosterona en la cuantificación de plaquetas. La administración de testosterona en ratas sham indujo una cuantificación de plaquetas significativamente mayor cuando se compara con el grupo de ratas sham con NaCl. Símbolo * (P < 0.05, Student´s t-test). En esta figura, los datos se expresan como media ± SEM de cuantificación de plaquetas, seis ratas por grupo
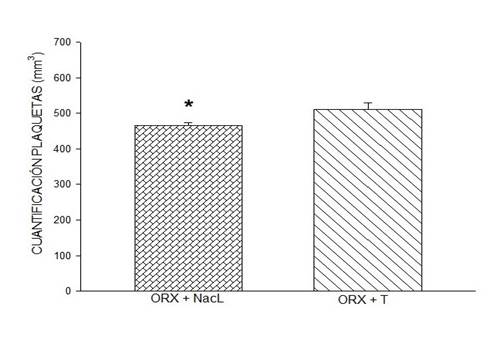
Figura 2: Efecto de la testosterona en la cuantificación de plaquetas. La administración de testosterona en ratas orquidectomizadas indujo una cuantificación de plaquetas significativamente mayor cuando se compara con el grupo de ratas orquidectomizadas con NaCl. Símbolo * (P < 0.05, Student´s t-test). En esta figura, los datos se expresan como media ± SEM de cuantificación de plaquetas, seis ratas por grupo
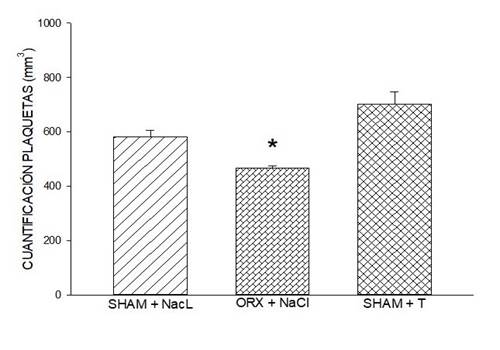
Figura 3: Efecto de la testosterona en la cuantificación de plaquetas. Ratas orquidectomizadas con NaCl presentan menor cuantificación de plaquetas cuando son comparadas con el grupo sham con NaCl, y con el grupo sham con testosterona. Símbolo * (P < 0.001, Kruskal-Wallis). En esta figura, los datos se expresan como media ± SEM de cuantificación de plaquetas, seis ratas por grupo
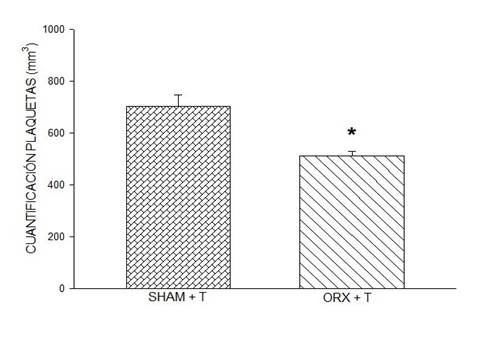
Figura 4: Efecto de la testosterona en la cuantificación de plaquetas. Ratas orquidectomizadas con testosterona presentan menor cuantificación de plaquetas cuando son comparadas con el grupo sham con testosterona. Símbolo * (P < 0.001, Student´s t-test). En esta figura, los datos se expresan como media ± SEM de cuantificación de plaquetas, seis ratas por grupo
El análisis unidireccional ANOVA se utilizó para determinar si había diferencias significativas entre los grupos en laFigura 1, el nivel de significancia estadística fue P < 0,005. La prueba post hoc del Método Dunn se empleó para determinar la base de diferencias significativas. La prueba T o la Prueba de suma de rango se usaron cuando fue apropiado, el nivel de significancia estadística fue P < 0.04. Los datos se presentan en cifras como medias ± SEM. Se utilizó el programa Sigma Stat para el análisis estadístico.
La administración de DHT en ratas macho ORX indujo una respuesta de cuantificación similar a la inducida por NaCl al 0.9% (solución salina). Sin embargo, la respuesta de cuantificación inducida por la administración de DHT en machos simulados fue significativamente mayor que la inducida por 0.9% de NaCl (Figura 1), ANOVA unidireccional, p < 0.005 y prueba para comparar dos grupos, (p < 0.04). La respuesta de cuantificación encontró resultados similares de testosterona endógena en los machos ORX y en los machos sham con NaCl al 0.9% que mostraron que la dosis de DHT fue concentración fisiológica (prueba-T fallida, p < 0.05). La diferencia estadística entre la administración endógena de DHT entre ratas sham y ratas macho ORX (Método Dunn, p < 0.05) sugiere que el impacto de la reducción prolongada en la concentración fisiológica de testosterona, a través de la ORX, en la expresión de plaquetas TXA2 afecta la regulación positiva de plaquetas, lo que sugiere la concentración controlada de testosterona endógena.
Se realizó una incisión simple escrotal bajo anestesia, se identificó el testículo, se amarró el cordón espermático y luego se procedió al corte para así evitar sangrado. Lo mismo se realizó en la otra gónada(19)
DISCUSIÓN
Este estudio muestra que hay una diferencia significativa entre el grupo con reposición de DHT y los otros grupos de comparación. Los niveles de plaquetas en sangre disminuyen en situaciones como la ORX inducida por la disminución de la testosterona endógena, además del nivel plaquetas en sangre disminuye en ratas ORX jóvenes que recibieron suero fisiológico cuando se compara con el grupo de ratas que recibió DHT exógena. Un estudio de doble ciego realizado por Ajayi, coincide con un aumento significativo de la agregación plaquetaria, siendo que los esteroides anabólico androgénicos contribuyen a un estado trombotico22.
Karolczack y colaboradores, evidenció que el efecto de esteroides sexuales in vitro, en donde la testosterona estimulada por colágeno o araquidonato, tiene un poder de inhibición de la agregación plaquetaria en personas de grupo etáreo de 60-65 años, incluyendo hombres y mujeres23, un estudio que evalúa la modulación del TXA2, a través de la administración de testosterona, mostró que el nivel de proteína sintasa TXA2 incrementa en vasos sanguíneos cerebrales24, sin embargo, se requieren más estudios para descartar que haya otro efecto indirecto que provoque esta acción. En comparación con el estudio de Campelo et al, se obtuvo como resultado que la testosterona inhibe la agregación plaquetaria en donde indican que es un efecto dependiente del óxido nítrico endotelial25. En resumen, este estudio sugiere que la administración de esteroide anabólico androgénico no demostró un efecto en la regulación de las plaquetas debido a que después de la castración la concentración de testosterona circulante se asocia con una disminución significativa de la densidad de receptor de las plaquetas TXA226.
En otro experimento se vio que la administración suprafisiológica de testosterona inhibe actividad fibrinolítica y el tiempo de sangrado es prolongado de forma significativa, sin embargo la agregación plaquetaria inducida por ADP se mostró sin cambios27. Actualmente, existen estudios en donde se sugiere que el consumo de esteroides anabólicos androgénicos está asociado a tromboembolismo y aumenta su riesgo trombótico puesto que inhiben la producción de un inhibidor de agregación plaquetaria prostaciclina, generándose estados de hipercoagulabilidad28, presentándose también cardiomiopatías, hipertrofia cardiaca entre otros29.
Algunos estudios concluyen que hay mayor cantidad de eventos perjudiciales en los hombres que tuvieron terapia de reemplazo de hormona o consumo de esteroides anabólicos androgénico30-33sin embargo, existen otros en donde encontraron efectos neutrales e incluso beneficiosos34,35.
Ante la diversidad de resultados, esto debido a distintos factores como lo son el prototipo de andrógeno utilizado, la cantidad de dosis, el tiempo del tratamiento, la forma de administración y el tipo de exámenes de laboratorio que existen para su evaluación, es que la FDA advierte de las consecuencias de usar este tipo de sustancias sin consulta o indicación médica, aprobándose solo su uso en casos tratamientos de reemplazo hormonal36. El uso indebido de esteroides anabólicos androgénicos puede ocasionar una dependencia en un contexto físico y psicológico.37
Diversos estudios que indican una mayor prevalencia en el consumo de esteroides anabólicos androgénicos en jóvenes de 15 - 24 años en un 54%11, es necesario que la población que consume dichos andrógenos no abuse con las concentraciones, en vista que a largo plazo pueden presentarse efectos adversos. Nuestra investigación sugiere ampliar y continuar con estudios para dilucidar la relación empírica entre el uso de estos esteroides anabólicos androgénicos y las consecuencias en el cuerpo del abuso de esto, ya que sigue aumentando la cantidad de personas que utilizan estas sustancias.
CONCLUSIÓN
Este estudio muestra que en ratas wistar la DHT induce un aumento en las plaquetas cuando la testosterona es administrada en niveles suprafisiológicos, sugiriendo una probable vía de TXA2. Los estudios posteriores esperan dilucidar este mecanismo probable, utilizando inhibidores de TXA2, para poder aclarar mejor a través de la regulación positiva de plaquetas.











 texto em
texto em