Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Revista de Investigaciones Altoandinas
versión On-line ISSN 2313-2957
Rev. investig. Altoandin. vol.19 no.4 Puno oct./dic 2017
http://dx.doi.org/10.18271/ria.2017.315
ARTÍCULO DEL 4TO CONGRESO INTERNACIONAL DE INGENIERÍA AGROINDUSTRIAL
Fenólicos a partir de residuos de café: Optimización del proceso de extracción
Phenolic from residues of coffee: optimization of the process of extraction
Marcelo-Diaz.R1; Luján-Gonzales V.1; Ramirez L.1; Olano M.1; Vargas A.1; Rojas M.L.2; Linares G.1*
1 School of Agroindustrial Engineering, National University of Trujillo, AV. Juan Pablo II s/n, Trujillo, Perú.
2 Department of Agri-food Industry, Food and Nutrition (LAN), Luiz de Queiroz College of Agriculture (ESALQ), University of São Paulo (USP), AV. Padua dias 11, Piracicaba, SP, Brazil.
* Autor para correspondencia (teléfono: 044 294778; email: glinares@unitru.edu.pe)
RESUMEN
La industria cafetera, cafeterías y restaurantes se encuentran en constante expansión. En consecuencia, se generan grandes cantidades de residuos sólidos de café – Spent Coffe Grounds (SCG), que son obtenidos después del proceso de lixiviación del café molido. Este residuo puede ser reutilizado debido a sus compuestos fenólicos. El objetivo del presente estudio fue evaluar el efecto del tiempo de extracción (30-90 min) asistido por ultrasonido (45 kHz y 50 W), relación líquido-sólido (10-40 ml/g) y concentración de etanol (20-93.8%) en el contenido de compuestos fenólicos totales (CFT) expresado en mg de ácido gálico/g de SCG en materia seca. Se utilizó la metodología de respuesta superficial (MSR), como una técnica eficiente que minimiza el número de experimentos, a través del diseño del rotacional central compuesto (DCCR) para determinar el efecto de estos 3 factores y para optimizar las condiciones del proceso de extracción de compuestos fenólicos totales compuestos. Las predicciones del modelo se correlacionaron con los valores experimentales en 84.04%, donde hubo una fuerte influencia (p <0,05) de las variables de tiempo de extracción asistida por ultrasonido y la relación líquido-sólido en los resultados. Las condiciones óptimas de 21.03% de etanol en una relación lıquido-sólido de 11.65 ml/g de SCG y procesamiento asistido por ultrasonidos durante 32.42 min, permitieron obtener un contenido de compuesto fenólico total de 1429.09 mg AG/g de SCG. Este contenido fué mayor al obtenido por otras técnicas de extracción descritas en la literatura.
PALABRAS CLAVES: café, fenólicos, ultrasonido, superficie de respuesta, optimización.
ABSTRACT
The coffee industry, coffee shops and restaurants are in constant expansion and growth. Consequently, large amounts of Spent Coffee Grounds (SCG) are generated, which are solid coffee residues obtained after the ground coffee leaching process. This residue can be reused because of its compounds as phenolics. The objective of the present study was to evaluate the effect of extraction time (30-90 min) assisted by ultrasound (45kHz and 50 W), liquid-solid ratio (10-40 ml/g) and ethanol concentration (20-93.8%) in the total phenolic compounds (CFT) content expressed as mg gallic acid/g SCG dry matter. Surface response methodology (MSR) was used, as an efficient technique that minimizes the number of experiments, through the central rotational compound design (DCCR) to determine the effect of these 3 factors and to perform the optimization of the extraction process conditions of total phenolic compounds. The predictions of the model were correlated with the experimental values in 84.04%, where there was a strong influence (P <0.05) of the ultrasound-assisted extraction time variables and liquid- solid ratio in the results. Optimal conditions (21.03% ethanol at a liquid-solid ratio of 11.65 ml/g SCG and ultrasonic assisted processing for 32.42 minutes) allowed a total phenolic compound content of 1429.09 mg AG/g of SCG to be obtained, a content higher than Obtained by other extraction techniques reported in the literature.
KEY WORDS: coffee, phenolics, ultrasound, surface response
I. INTRODUCCIÓN
El grano de café es el producto agrícola utilizado para producir una de las bebidas más consumidas. La cual es muy apreciada por su aroma, sabor y propiedades estimulantes debido a su contenido en cafeína (Gómez-Ruiz, Ames, & Leake, 2008). La industria cafetalera está en constante expansión, donde la producción de café instantáneo se ha convertido en uno de los más importantes. Como consecuencia, se obtienen grandes cantidades de café molido durante el procesamiento, generando en todo el mundo alrededor de 6.000.000 de toneladas de residuos (Mussatto, Ballesteros, Martins, Teixeira, 2011). Estos desechos sólidos se conocen como depósitos de café gastado ó Spent Cofe Grounds (SCG), que no tienen valor comercial y generalmente se eliminan. Para la eliminación de SCG, se debe realizar un tratamiento adecuado ya que su alto contenido y la presencia de compuestos tales como cafeína, taninos y polifenoles pueden tener efectos negativos sobre el medio ambiente (Silva, Nebra, Silva y Sánchez, 1998). Por estas razones, recientemente se ha centrado el interés en la reutilización de estos residuos (Magalhães, Machado, Segundo, Lopes & Páscoa, 2016).
Por otro lado, la actividad antioxidante en alimentos y bebidas viene generando gran interés (Gülçin, 2012). De hecho, los alimentos suelen ser fortificados con cantidades adicionales de antioxidantes, ya sean naturales o sintéticos. Sin embargo, debido a problemas de seguridad, el interés por los antioxidantes naturales se ha intensificado (Shahidi, 2000). En este contexto, los residuos de café se consideran ricos en nutrientes bioactivos (Esquivel & Jiménez, 2012). Por lo que este material representa una fuente alternativa para obtener antioxidantes naturales, considerándose completamente seguros en comparación con los sintéticos (Páscoa, Magalhães, & Lopes, 2013).
El presente estudio buscó optimizar las condiciones de extracción de compuestos fenólicos, reduciendo así el impacto ambiental generado por los residuos de café. Los compuestos fenólicos pueden utilizarse de diferentes maneras en los alimentos y en la prevención de enfermedades crónicas degenerativas, entre otros (Scalbert., Johnson & Saltmarsh, 2005) Ramalakshmi, Rao, Takano-Ishikawa y Goto, 2009).
El método utilizado para extraer compuestos fenólicos juega un papel importante en la calidad del extracto. La extracción asistida por microondas (Yang & Zhai, 2010), extracción ultrasónica (Pan, Yu, Zhu & Qiao, 2012), extracción acelerada con disolvente (Skalicka-Woźniak, Szypowski y Głowniak 2011) y extracción supercrítica (Liu, Lin, Wang, Wang, Zhang & Liu, 2011) son algunas técnicas para la recuperación de compuestos fenólicos. La empleada en esta investigación fue la técnica asistida por ultrasonido, cuyos efectos de extracción se basan en el fenómeno de la cavitación acústica. El ultrasonido induce una serie de efectos físicos, químicos y mecánicos (Wang, Sun, Cao, Tian y Li, 2008), resultando en un aumento en la tasa de recuperación de compuestos fenólicos (Ma, Ye, Fang, Chen, Xu & Liu, 2008).
El objetivo de este estudio, basado en la metodología de superficie de respuesta, fue optimizar las condiciones de extracción: tiempo (t), relación líquido-sólido (LS) y concentración de etanol (E) en el contenido total de compuestos fenólicos.
II. MATERIALES Y MÉTODOS
A. Materiales y reactivos
Los residuos de café (variedad arábica, 1 kg de muestra) fueron obtenidos en la cafetería Starbucks, Trujillo, Perú. El material se secó a 37 °C usando un sistema de aire forzado (Memmert, modelo SM 200, Alemania), hasta un 10% de contenido de humedad. Todos los reactivos utilizados fueron de grado analítico. Reactivo de Folin - Ciocalteau "HC389020", 2,2-difenil-1-picrilhidrazina (DPPH) (Sigma Aldrich, EE.UU.), Na2CO3 (EINECS, China), ácido gálico y agua destilada.
B. Proceso de extraccion asisitida por ultrasonido
Se homogeneizó un gramo de muestra seca con diferentes concentraciones de etanol (20 – 93.8%), mezclando con diferentes relaciones líquido - sólido (10-40 ml/g). Posteriormente, el homogeneizado se trató con ultrasonido a diferentes tiempos (30 - 90 min), de acuerdo con la tabla 1. Para ello, se colocó el homogeneizado en un bao ultrasónico (modelo GT SONIC VGT-1620, potencia de 45 kHz y 50 W, China). Los sobrenadantes se filtraron y vertieron en depósitos herméticamente sellados y aislados de luz para análisis posteriores.
C. Determinación de compuestos fenólicos totales (CFT)
En un tubo de ensayo se colocaron 20 μl de la solución extraída de café, 1580 μl de agua destilada, a continuación, se añadieron100 μl del reactivo Folin- ciocalteau (2 N), se agitó y se dejó en reposo durante 8 minutos a temperatura ambiente. Después se añadieron300 μl de solución de carbonato de sodio al 20%, se mezcló y se incubó durante 18 minutos a 40ºC. finalmente, se midió la absorbancia a 765 nm en espectrofotómetro (UV-VIS 6300 JENWAY, Inglaterra), usando ácido gálico para la curva estándar. Los resultados se expresaron como mg AG/g de materia seca de residuo de café.
D. Diseño experimental y análisis estadístico
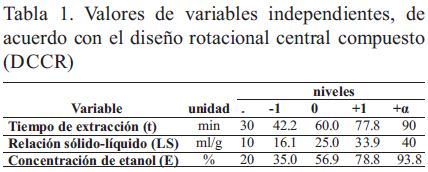
Con el fin de examinar y optimizar el proceso de extracción de compuestos fenólicos por ultrasonido, se determinó el efecto del tiempo de extracción, la relación líquido-sólido y la concentración de etanol en el contenido de compuestos fenólicos. Las variables estadísticas seleccionadas se codificaron en tres niveles (- 1, 0, +1) y dos puntos axiales (-α, +α) de acuerdo a lo descrito por Maran, (2015). Las concentraciones utilizadas en cada experimento se establecieron de acuerdo con el diseño rotacional central compuesto (DCCR), presentado en la Tabla 1
El análisis de regresión múltiple se utilizó para analizar los datos experimentales. La interacción lineal y los coeficientes cuadráticos se evaluaron mediante ANOVA (p <0.05). Se determinaron los valores de F-test y probabilidad (p) para analizar la contribución estadística significativa de todos los términos. El ajuste del modelo se verificó mediante el coeficiente de determinación (R2). Las condiciones del proceso se optimizaron a través de los gráficos de superficie de respuesta deseados. Todos los análisis se realizaron utilizando el software (Statistica 7.0.61.0, EE.UU.)
III. RESULTADOS Y DISCUSIÓN
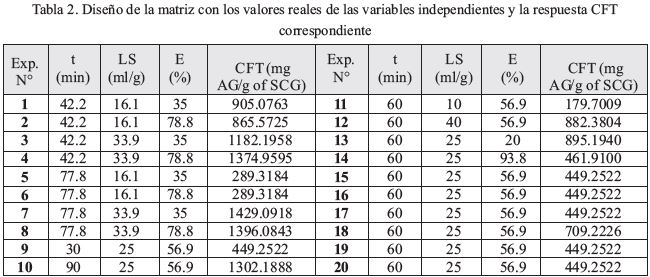
El diseño experimental y la respuesta CFT correspondiente se muestran en la Tabla 2. El modelo presentó un total de 20 experimentos, con seis repeticiones en el punto central. Los resultados del diseño experimental se procesaron mediante la aplicación de un análisis de regresión múltiple, a partir del cual se obtuvo una ecuación polinomial de segundo orden completa, obteniéndose los coeficientes de regresión del intercepto lineal, cuadrático y los términos de interacción del modelo. La relación empírica, con p < 0,05 y R2 = 84,04%, entre las variables independientes y CFT se obtuvo mediante la siguiente ecuación polinomial.
CFT = 4999.68-98.08*t+0.623*t²-
89.810*LS+0.961*LS²-
32.05*E+0.267*E²+1.152*t*LS-
0.060*t*E+0.128*LS*E
De acuerdo con las condiciones de extracción aplicadas en este trabajo, el contenido total de compuestos fenólicos estuvo en el intervalo de 179.70-1429.09 (mg AG/g SCG). El SCG tiene un contenido de fenol más alto que el del orujo de oliva, las cáscaras de papa (Makris, Boskou y Andrikopoulos, 2007), la cáscara de manzana (Sudha, Baskaran & Leelavathi, 2007), cuyos valores fueron cercanos a 10 mg AG/de uvas blancas y rojas, que eran iguales a 48,2 y 54 mg A G /g, respectivamente (Makris et al., 2007). Por lo tanto, en comparación con estos tipos de materia prima, SCG puede considerarse una buena fuente de compuestos fenólicos (Zuorro A., 2015).
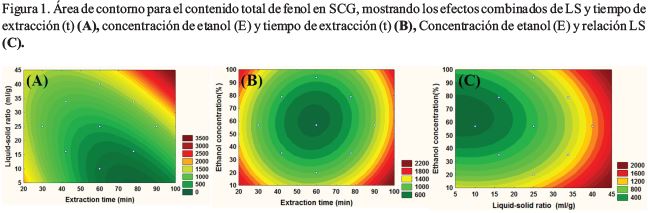
A través del gráfico de Pareto se observó que la relación líquido-sólido era la variable más importante que afectaba al contenido fenólico total del SCG, seguido por el tiempo de extracción. Las condiciones óptimas para obtener el mayor contenido de compuestos fenólicos se determinaron a través de los gráficos de contorno (Figura 1). Las condiciones óptimas fueron: tiempo de extracción de 32.42 min, relación lıquido-sólido de 11,65 ml/g y una concentración de etanol de 21,03%. Estas condiciones permitieron obtener un valor de CFT de 1429,09 mg AG/g SCG. Otros estudios reportaron que el proceso óptimo de extracción se encontró en condiciones de potencia ultrasónica de 244 W, temperatura de 40 ºC, 1:17 g/ ml de la relación de LS, procesado durante 34 min, obteniendo 33.84 ± 0.59 mg AG/ g de SCG (Al-Dhabi, Ponmurugan, & Jeganathan, 2016). Por otra parte, según Mussatto et al., (2011) la extracción de compuestos antioxidantes fenólicos de SCG con 60% de metanol en una relación solvente/sólido de 40 ml/g SCG, durante 90 min fue la condición más adecuada para producir un extracto con un alto contenido de compuestos fenólicos (16 mg AG/g SCG) por el método convencional sólido-líquido. Estos resultados son inferiores a los obtenidos en el presente estudio, debido a la influencia del tipo de disolvente, así como de las condiciones utilizadas. La relación LS aumenta la velocidad de disolución, debido a la alta concentración y diferencia de soluto entre el disolvente y la matriz material (Maran, Manikandan, Thirugnanasambandham, Nivetha y Dinesh, 2013). Este fenómeno se explica por los principios de la transferencia de masa, que establece que la tasa de difusión es directamente proporcional a la concentración (Al-Dhabi et al., 2016). Otro estudio indica que el mayor contenido de polifenoles totales de 398.95 mg AG/g de materia seca se obtuvo con una solución acuosa al 20% de etanol durante 40 s de radiación de microondas (80 W) en la extracción de CFT de residuos de café (Pavlović, Buntić, Šiler-Marinković y Dimitrijević- Branković, 2013). En comparación con la energía de microondas, la energía ultrasónica utilizada en este estudio permitió un mayor rendimiento de CFT.
IV. CONCLUSIÓN
Se determinó el efecto de las variables independientes sobre el contenido de compuestos fenólicos de los depósitos de café gastado (SCG), siendo la relación líquido-sólido y el tiempo de extracción las variables más influyentes. El contenido máximo de compuestos fenólicos (1429.09 mg AG/g SCG) puede ser extraído utilizando una relación líquido-sólido de 11.65 ml/g, con solución de etanol al 21,03%, mediante un proceso de extracción asistido por ultrasonido durante 32.42 min. Los resultados de este estudio indican que los SCG son una fuente potencial de compuestos fenólicos que pueden recuperarse fácilmente. Se demostró que el etanol era un disolvente adecuado para la extracción de compuestos fenólicos debido a su alta polaridad, además se determinó que el uso de ultrasonido mejora la extracción de compuestos fenólicos, obteniendo mayor rendimiento comparado con métodos convencionales.
REFERENCIAS BIBLIOGRÁFICAS
Al-Dhabi, N. A., Ponmurugan, K., & Jeganathan, P. M. (2017). Development and validation of ultrasound- assisted solid-liquid extraction of phenolic compounds from waste spent coffee grounds. Ultrasonicssonochemistry, 34, 206-213. [ Links ]
Esquivel, P., & Jiménez, V. M. (2012). Functional properties of coffee and coffee by-products. Food Research International, 46(2), 488-495. [ Links ]
Gómez-Ruiz, J. Á., Ames, J. M., & Leake, D. S. (2008). Antioxidant activity and protective effects of green and dark coffee components against human low density lipoprotein oxidation. European Food Research and Technology, 227(4), 1017-1024. [ Links ]
Gülçin, I. (2012). Antioxidant activity of food constituents: an overview. Archives of toxicology, 86(3), 345-391. [ Links ]
Liu, J., Lin, S., Wang, Z., Wang, C., Wang, E., Zhang, Y., & Liu, J. (2011). Supercritical fluid extraction of flavonoids from Maydis stigma and its nitrite-scavenging ability. Food and bioproducts processing, 89(4), 333-339. [ Links ]
Ma, Y. Q., Ye, X. Q., Fang, Z. X., Chen, J. C., Xu, G. H., & Liu, D. H. (2008). Phenolic compounds and antioxidant activity of extracts from ultrasonic treatment of Satsuma mandarin (Citrus unshiu Marc.) peels. Journal of Agricultural and Food Chemistry, 56(14), 5682-5690. [ Links ]
Magalhães, L. M., Machado, S., Segundo, M. A., Lopes, J. A., & Páscoa, R. N. (2016). Rapid assessment of bioactive phenolics and methylxanthines in spent coffee grounds by FT- NIR spectroscopy. Talanta, 147, 460-467. [ Links ]
Makris, D. P., Boskou, G., & Andrikopoulos, N. K. (2007). Polyphenolic content and in vitro antioxidant characteristics of wine industry and other agri-food solid waste extracts. Journal of Food Composition and Analysis, 20(2), 125-132. [ Links ]
Maran, J. P. (2015). Statistical optimization of aqueous extraction of pectin from waste durian rinds. International journal of biological macromolecules, 73, 92-98. [ Links ]
Maran, J. P., Manikandan, S., Thirugnanasambandham, K., Nivetha, C. V., & Dinesh, R. (2013). Box–Behnken design based statistical modeling for ultrasound-assisted extraction of corn silk polysaccharide. Carbohydrate Polymers, 92(1), 604-611. [ Links ]
Mussatto, S. I., Ballesteros, L. F., Martins, S., & Teixeira, J. A. (2011). Extraction of antioxidant phenolic compounds from spent coffee grounds. Separation and Purification Technology, 83, 173-179. [ Links ]
Pan, G., Yu, G., Zhu, C., & Qiao, J. (2012). Optimization of ultrasound-assisted extraction (UAE) of flavonoids compounds (FC) from hawthornseed (HS). Ultrasonics Sonochemistry, 19(3), 486-490. [ Links ]
Páscoa, R. N., Magalhães, L. M., & Lopes, J. A. (2013). FT-NIR spectroscopy as a tool for valorization of spent coffee grounds: Application to assessment of antioxidant properties. Food research international, 51(2), 579-586. [ Links ]
Pavlović, M. D., Buntić, A. V., Šiler-Marinković, S. S., & Dimitrijević-Branković, S. I. (2013). Ethanol influenced fast microwave-assisted extraction for natural antioxidants obtaining from spent filter coffee. Separation and Purification Technology, 118, 503-510.
Ramalakshmi, K., Rao, L. J. M., Takano-Ishikawa, Y., & Goto, M. (2009). Bioactivities of low-grade green coffee and spent coffee in different in vitro model systems. Food Chemistry, 115(1), 79-85. [ Links ]
Scalbert, A., Johnson, I. T., & Saltmarsh, M. (2005). Polyphenols: antioxidants and beyond. The American journal of clinical nutrition, 81(1), 215S-217S. [ Links ]
Shahidi, F. (2000). Antioxidants in food and food antioxidants. Molecular Nutrition & Food Research, 44(3), 158-163. [ Links ]
Silva, M. A., Nebra, S. A., Silva, M. M., & Sanchez, C. G. (1998). The use of biomass residues in the Brazilian soluble coffee industry. Biomass and Bioenergy, 14(5), 457-467. [ Links ]
Skalicka-Woźniak, K., Szypowski, J., & Głowniak, K. (2011). HPLC analysis of kaempherol and quercetin derivatives isolated by different extraction techniques from plant matrix. Journal of AOAC International, 94(1), 17-21. [ Links ]
Sudha, M. L., Baskaran, V., & Leelavathi, K. (2007). Apple pomace as a source of dietary fiber and polyphenols and its effect on the rheological characteristics and cake making. Food chemistry, 104(2), 686-692. [ Links ]
Wang, J., Sun, B., Cao, Y., Tian, Y., & Li, X. (2008). Optimisation of ultrasound-assisted extraction of phenolic compounds from wheat bran. Food Chemistry, 106(2), 804-810. [ Links ]
Yang, Z., & Zhai, W. (2010). Optimization of microwave-assisted extraction of anthocyanins from purple corn (Zea mays L.) cob and identification with HPLC–MS. Innovative food science & emerging technologies, 11(3), 470-476. [ Links ]
Zuorro, A. (2015). Optimization of polyphenol recovery from espresso coffee residues using factorial design and response surface methodology. Separation and Purification Technology, 152, 64-69. [ Links ]
Johns, N. (1995). Higiene de los alimentos. Zaragoza, España. Acribia. Sp. [ Links ]
Artículo recibido 22/06/2017
Artículo aceptado 18/07/2017
On line: 25/10/2017