Introducción
La contaminación del suelo por metales pesados es uno de los problemas actuales más recurrentes y de mayor importancia a nivel internacional. El empleo de estos elementos en actividades industriales, mineras, agrícolas y domésticas ha incrementado la infertilidad y degradación de los suelos, afectando la seguridad alimentaria y el desarrollo económico de muchos países a nivel mundial (Rodríguez et al., 2006).
Algunos metales como cobre y hierro son esenciales para la vida y juegan un papel importante en, por ejemplo, el funcionamiento de algunos sistemas enzimáticos. En cambio, otros metales son xenobióticos, o sea, no tienen ningún uso en los procesos fisiológicos y, como en el caso del plomo, arsénico y cadmio, los que pueden ser tóxicos en pequeñas cantidades. Aun los metales esenciales para el organismo humano, tienen el potencial de volverse dañinos si la persona es expuesta a altos concentraciones (Frazar, 2000; Alcorta et al., 2010).
El "U.S. Agency for Toxic Substances and Disease Registry" (ATSDR) enumera todos los peligros y daños presentes en desechos tóxicos de acuerdo a la severidad de su toxicidad. Según esta lista, en primer, segundo, tercer y sexto lugar se encuentran los siguientes metales pesados: plomo, mercurio, arsénico y cadmio, respectivamente (García & Dorronsoro, 2005).
La gran mayoría de los metales pesados tienen efectos tóxicos sobre las poblaciones de plantas y animales, además de acumularse y biomagnificarse en los ecosistemas a través de la cadena trófica. Por esta razón, se hace necesario el estudio de los efectos fitotóxicos de los metales pesados en cultivos agrícolas (Rubio et al., 2004). Las principales fuentes contaminantes de plomo, arsénico, cadmio y otros metales pesados son principalmente los residuos y subproductos de la industria minero-metalúrgica, química, farmacéutica y petroquímica (Prasad, 2004).
Una vez absorbido por las raíces de las plantas, el plomo, arsénico y cadmio causan efectos fitotóxicos según su concentración, naturaleza química (Bautista, 1999) y su disponibilidad en el suelo, el que a su vez depende de sus características químicas y física como el pH, humedad, salinidad, capacidad de intercambio catiónico, materia orgánica y presencia de otros componentes químicos como el fósforo (Howard & Sova, 1993).
La absorción en los vegetales se realiza principalmente a través de los pelos radiculares y la pared celular donde son almacenados debido a la carga iónica negativa que confieren los grupos carboxilo, parte estructural de glucósidos, proteínas y carbohidratos (García, 2006). Ghani et al., 2010, sostienen que la absorción de plomo, arsénico, cadmio y otros metales pesados tóxicos, generan alteraciones en la estructura celular y durante el proceso fotosintético, provocando alteraciones morfológicas y fisiológicas como reducción en el crecimiento, clorosis, necrosis y cambios en el régimen hídrico.
Asimismo, de acuerdo a Seregin & Ivanov (1997), la fitotoxicidad en las plantas depende en gran medida de su mecanismo para asimilar, acumular y translocar estos metales, y de sus mecanismos biológicos de defensa que confieren resistencia a la planta ante la presencia de metales pesados en el ambiente. Ruiz & Armienta (2012), sostienen también que dos de los cultivos con la capacidad de absorber grandes cantidades de plomo, arsénico y cadmio están representados por el “maíz” (Zea mays L.) y la “beterraga” (Beta bulgaris L.).
Por otro lado, los metales pesados como el plomo, arsénico y cadmio pueden alcanzar altos niveles de concentración en los suelos en zonas adyacentes a áreas de impacto, los que provocan efectos negativos en sus propiedades físicas, químicas y biológicas como: reducción del contenido de materia orgánica, disminución de nutrimentos, variación del pH generando suelos ácidos, amplias fluctuaciones en la temperatura, efectos adversos en el número, diversidad y actividad en los microorganismos de la rizósfera, dificultan el crecimiento de una cubierta vegetal protectora favoreciendo la aridez, erosión del suelo, y la dispersión de los contaminantes hacia zonas y acuíferos adyacentes y como consecuencia aumenta la vulnerabilidad de la planta al ataque por insectos, plagas y enfermedades, afectando su desarrollo (Zhang et al., 2000).
Actualmente existen estudios tendientes a resolver la contaminación originada por metales pesados en suelos, mediante estrategias basadas en el uso de plantas que tienen la propiedad de acumular metales pesados; proceso denominado "fitorremediación" que consiste en la remoción, transferencia, estabilización y/o degradación y neutralización de compuestos orgánicos, inorgánicos y radioactivos que resultan tóxicos en suelos y agua.
Esta novedosa tecnología tiene como objetivo degradar y/o asimilar, los metales pesados, presentes en el suelo, lo cual tiene muchas ventajas con respecto a los métodos convencionales de tratamientos de lugares contaminados; en primer lugar, es una tecnología económica, de bajo costo, en segundo lugar posee un impacto regenerativo en lugares en donde se aplica y en tercer lugar su capacidad extractiva se mantiene debido al crecimiento vegetal (Harvey et al., 2002).
Pero, la fitorremediación no es un remedio para todos los suelos contaminados, antes de que esta tecnología pueda volverse técnicamente eficiente y económicamente viable, hay algunas limitaciones que necesitan ser superadas como por ejemplo, sus mecanismos tanto moleculares, bioquímicos y fisiológicos los cuales son pocos conocidos e insuficientemente entendidos, sin embargo, a pesar de esto un gran número de plantas hiperacumuladoras todavía pueden descubrirse e identificarse (Prasad & Freitas, 2003; Alvarez, 2008; Apaclla & Peso, 2015).
No encontrándose en nuestro país investigaciones sobre fitorremediación utilizando suelos contaminados por relaves mineros con presencia de plomo, arsénico y cadmio; y siendo estos metales pesados altamente tóxicos y por estar contaminando a la mayoría de suelos de nuestro país debido a la explotación minera, por lo cual es de particular interés la realización de estudios de detoxificación de suelos, lo que nos permitiría utilizar esta técnica a futuro con la finalidad de descontaminar suelos afectados por metales pesados como el plomo, arsénico y cadmio.
Por lo que, el objetivo de la presente investigación, es cuantificar la concentración de los metales pesados plomo, arsénico y cadmio absorbidos por la raíz, tallo y hojas del “maíz” (Zea mays L.) y “beterraga” (Beta vulgaris L.) partir de suelos agrícolas contaminados por 1359,60 mg/kg de plomo, 6,10 mg/kg de arsénico y 28,80 mg/kg de Cadmio a los 65, 95 y 125 días de crecimiento vegetativo.
Material y métodos
Material de estudio
El material de estudio estuvo constituido por muestras de suelos agrícolas contaminados por 1359,60 mg/kg de plomo, 6,10 mg/kg de arsénico y 28,80 mg/kg de Cadmio en asociación con plántulas de “maíz” (Zea mays L.) y “beterraga” (Beta vulgaris L.) generadas a partir de semillas certificadas obtenidas del concesionario Hortus, La Libertad.
Procedimiento
I. Obtención de las muestras de suelo.
La muestra de suelo para el grupo control fue obtenida del campo experimental de Ecología de la Universidad Nacional de Trujillo, mientras que el suelo contaminado se obtuvo del área adyacente a las relaveras de la localidad de Samne, La Libertad, Perú. En el lugar se determinaron los parámetros físicos de temperatura, humedad relativa y pH utilizando un medidor multiparámetro. Para colectar la muestra de suelos se utilizaron palanas jardineras y bolsas plásticas dobles estériles. En el laboratorio se removieron todo tipo de material extraño, luego este se tamizó con un tamiz de 2 mm de diámetro y guardado en bolsas plásticas estériles debidamente etiquetadas.
II. Determinación de los grupos control y experimentales.
Se utilizaron como prueba control una muestra de suelo agrícola del Campo Experimental, a la cual solo se le añadió las semillas del “maíz” (Zea mays L.) y “beterraga” (Beta vulgaris L.) tres por golpe, las que fueron procesadas de la misma forma que las muestras experimentales. Se estructuraron tres grupos experimentales con tres repeticiones de suelo contaminado con 1359,60 mg/kg de Plomo; 6,10 mg/kg de Arsénico y 28,80 mg/kg de Cadmio para determinar el grado de asimilación de los metales pesados Pb, As y Cd, a nivel de raíz, tallo y hojas, a los cuales se les agregó las semillas del material biológico utilizado. Finalmente se determinaron las concentraciones de los metales pesados Pb, As y Cd presentes en raíces, tallo y hojas, a los 65, 95 y 125 días de iniciado el experimento.
III. Extracción de los metales
Para la extracción de los metales de la muestra de suelo y del tejido de raíz, tallo y hojas se siguió el protocolo de la norma EPA 2003 guía para la preparación estándar y procedimientos de operación para análisis de aguas, suelos y material vegetal, utilizando un espectrofotómetro de absorción atómica Perkin Elmer Pin AAcle 900F. Las muestras de suelos, así como de “maíz” (Zea mays L.) y “beterraga” (Beta vulgaris L.) se secaron a 110ºC. Luego se llevó a molienda, se tamizó cada muestra independientemente con tamiz de 2 mm, pesándose 1 g de muestra y luego trasladándose a una fiola de 50 ml enrasándose con ácido nítrico QP, sometiéndose a continuación a digestión en hotplate por 2 horas a 102ºC; leyéndose luego la concentración de cada elemento en ambas muestras.
Resultados
Los promedios obtenidos de los parámetros temperatura, humedad relativa y pH determinados al momento de la colección de la muestra de material de suelo contaminado por relave del área periférica a las relaveras de la zona de Samne, La Libertad-Perú, fueron los siguientes: temperatura de 24,9ºC, humedad relativa de 68,0 % y un pH 6,3.
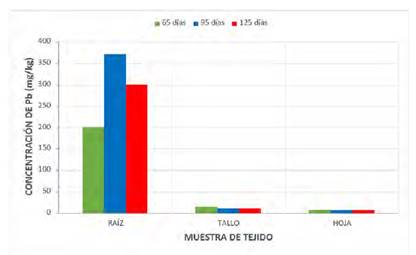
El “maíz” Zea mays L . y la “beterraga” (Beta vulgaris L.), mostraron diferentes comportamientos en relación con la absorción de plomo, arsénico y cadmio para cada una de las concentraciones experimentales. Para el plomo, en el caso del material de experimentación la concentración inicial de este metal en el suelo para ambos vegetales fue de 1359,60 mg/kg; luego al final de los 125 días de experimentación, el contenido máximo determinado de plomo en el maíz fue de 371,66 mg/kg (27,33% de absorción), mientras que para la beterraga la concentración obtenida fue de 432,95 mg/kg (31,84% de absorción), los que fueron obtenidos a los 95 días de experimentación y a nivel del órgano raíz. Mientras que la concentración mínima de este metal en el “maíz” fue de 7,01 mg/kg (0,52 % de absorción), en cambio para la “beterraga” el valor determinado fue de 13,51 mg/kg, determinados a los 125 días de iniciado el experimento y en el órgano hoja (Cuadros 2 y 5; Fig. 1, 4,7 y 10).
Cuadro 1 Concentración de los metales pesados Pb, As y Cd, en muestra de suelos contaminados por relaves mineros, provenientes de la zona de Samne, La Libertad - Perú.
| MUESTRA METAL | SUELO (mg/kg) | VALORES ECA (mg/kg) |
| Pb | 1359,60 | 70,0 |
| As | 6,10 | 2,5 |
| Cd | 28,80 | 1,4 |
ECA: Fuente D.S Nª 002-2003 MINAM
Cuadro 2 Concentración de los metales pesados Pb, As y Cd, a los 65, 95 y 125 días, en muestras de tejido de raíz, tallo y hojas del “maíz” (Zea mays L.), cultivados en suelos contaminados por relaves mineros provenientes de la zona de Samne, La Libertad - Perú.
| METAL MUESTRA | Pb 1359,60 (mg/kg) | As 6,10 (mg/kg) | Cd 28,80 (mg/kg) |
| RAÍZ (65 días) | 201,32 | 1,34 | 9,60 |
| (95 días) | 371,66 | 1,51 | 11,47 |
| (125 días) | 301,24 | 1,94 | 14,82 |
| TALLO (65 días) | 14,89 | 0,68 | 0,35 |
| (95 días) | 11,07 | 0,76 | 0,45 |
| (125 días) | 11,02 | 0,76 | 0,69 |
| HOJA (65 días) | 7,60 | 0,07 | 0,27 |
| (95 días) | 7,13 | 0,08 | 0,34 |
| (125 días) | 7,01 | 0,7 | 0.29 |
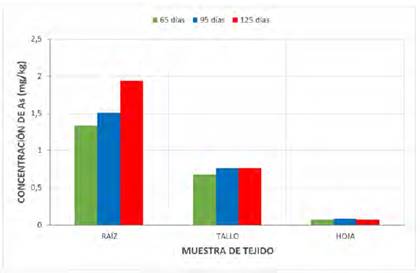
En el caso del arsénico, en el material de experimentación la concentración inicial de este metal en suelo fue de 6,10 mg/kg, luego al final de los 125 días de experimentación al evaluar el contenido máximo determinado de este metal en el “maíz”, su valor fue de 1,94 mg/kg (31,80% de absorción), mientras que en el caso de la “beterraga” la concentración fue de 3,89 mg/kg; valores determinados a los 125 y 95 días de experimentación y a nivel del órgano raíz. Mientras que la concentración mínima determinada para el arsénico en el “maíz” 0,07 mg/kg (1,15% de absorción) fue determinado a los 125 días de experimentación, en cambio para la “beterraga” este valor de 0,05 mg/kg se determinó a los 65 días del experimento y ambos en el órgano hoja (Cuadros 3 y 5; Fig. 2, 5, 8, 11).
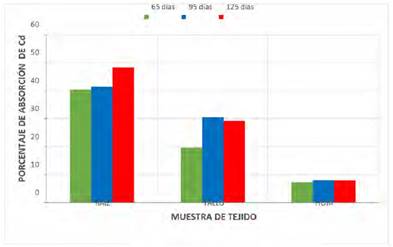
Cuadro 3 Porcentaje de absorción de los metales pesados Pb, As y Cd, a los 65, 95 y 125 días, en muestras de tejido de raíz, tallo y hojas del “maíz” (Zea mays L.), cultivados en suelos contaminados por relaves mineros provenientes de la zona de Samne, La Libertad - Perú.
| METAL MUESTRA | % Ab.Pb | % Ab.As | % Ab.Cd |
| RAÍZ (65 días) | 14,78 | 21,97 | 33,33 |
| (95 días) | 27,33 | 24,75 | 39,83 |
| (125 días) | 22,16 | 31,80 | 51,46 |
| TALLO (65 días) | 1,09 | 11,15 | 1,32 |
| (95 días) | 0,81 | 12,46 | 1,56 |
| (125 días) | 0,81 | 12,46 | 2,39 |
| HOJA (65 días) | 0,56 | 1,15 | 0,94 |
| (95 días) | 0,52 | 1,31 | 1,18 |
| (125 días) | 0,52 | 1,15 | 1,01 |
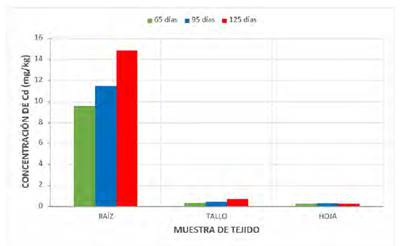
En cambio, para el caso del Cadmio, en el material de suelo de experimentación se determinó una concentración de 28,80 mg/kg de este metal; encontrándose al final de la etapa de experimentación que el contenido máximo de Cadmio en el “maíz” fue de 14,82 mg/kg (51,46% de absorción) y en la “beterraga” de 13,88 mg/kg (48,19% de absorción), los que fueron determinados a los 125 días de experimentación y a nivel del órgano raíz. Con respecto a la concentración mínima de este metal en el “maíz” esta fue de 0,27 mg/kg (0,94% de absorción) en cambio para la “beterraga” el valor determinado fue de 2,10 mg/kg (7,29% de absorción) los que se determinaron a los 65 días de iniciado el experimento en el órgano hoja (Cuadro 4 y 5; Fig. 3, 6, 9 y 12).
Cuadro 4 Concentración de los metales pesados Pb, As y Cd, a los 65, 95 y 125 días, en muestras de tejido de raíz, tallo y hojas de la “beterraga” (Beta vulgaris L.), cultivados en suelos contaminados por relaves mineros provenientes de la zona de Samne, La Libertad - Perú.
| METAL MUESTRA | Pb 1359,60 (mg/kg) | As 6,10 (mg/kg) | Cd 28,80 (mg/kg) |
| RAÍZ (65 días) | 408,33 | 3,63 | 11,62 |
| (95 días) | 432,95 | 3,89 | 11,88 |
| (125 días) | 428,17 | 3,80 | 13,88 |
| TALLO (65 días) | 114,89 | 0,82 | 5,68 |
| (95 días) | 123,07 | 0,89 | 8,76 |
| (125 días) | 115,02 | 0,81 | 8,40 |
| HOJA (65 días) | 13,61 | 0,05 | 2,10 |
| (95 días) | 13,69 | 0,07 | 2,34 |
| (125 días) | 13,51 | 0,06 | 2,30 |
Cuadro 5 Porcentaje de absorción de los metales pesados Pb, As y Cd, a los 65, 95 y 125 días, en muestras de tejido de raíz, tallo y hojas de la “beterraga” (Beta vulgaris L.), cultivados en suelos contaminados por relaves mineros, provenientes de la zona de Samne, La Libertad - Perú.
| METAL MUESTRA | % Ab.Pb | % Ab.As | % Ab.Cd |
| RAÍZ (65 días) | 30,3 | 59,51 | 40,34 |
| (95 días) | 31,84 | 63,77 | 41,25 |
| (125 días) | 31,49 | 62,29 | 48,19 |
| TALLO (65 días) | 8,45 | 13,44 | 19,72 |
| (95 días) | 9,05 | 14,59 | 30,1 |
| (125 días) | 8,46 | 13,28 | 29,17 |
| HOJA (65 días) | 1,00 | 0,82 | 7,29 |
| (95 días) | 1,01 | 1,14 | 8,12 |
| (125 días) | 0,99 | 0,98 | 7,99 |
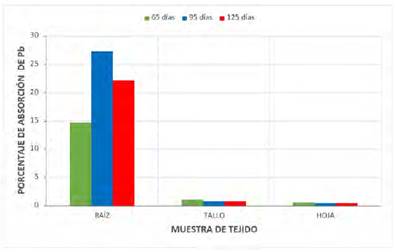
Fig. 4 Niveles de absorción comparativa de Pb en porcentaje en diversos órganos del “maíz” (Zea mays L.).
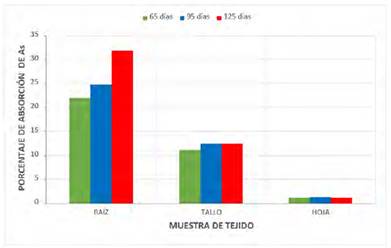
Fig. 5 Niveles de absorción comparativa de As en porcentaje en diversos órganos del “maíz” (Zea mays L.)
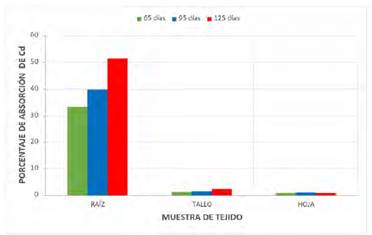
Fig. 6 Niveles de absorción comparativa de Cd en porcentaje en diversos órgano del “maíz” (Zea mays L.).
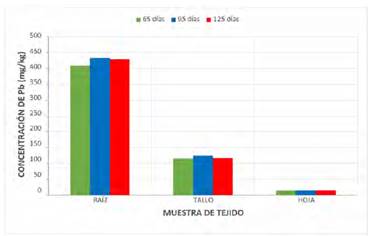
Fig. 7 Niveles de concentración comparativo de Pb en diversos órganos de la “beterraga” (Beta vulgaris L.).
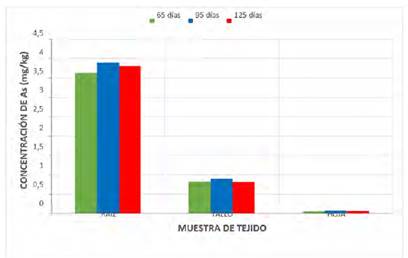
Fig. 8 Niveles de concentración comparativo de As en diversos órganos de la “beterraga” (Beta vulgaris L.)
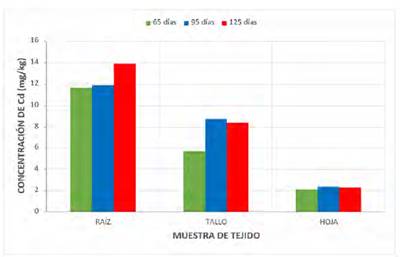
Fig. 9 Niveles de concentración comparativo de Cd en diversos órganos de la “beterraga” (Beta vulgaris L.).
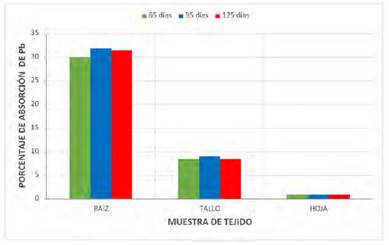
Fig. 10 Niveles de absorción comparativa de Pb en porcentaje en diversos órganos de la “beterraga” (Beta vulgaris L.).
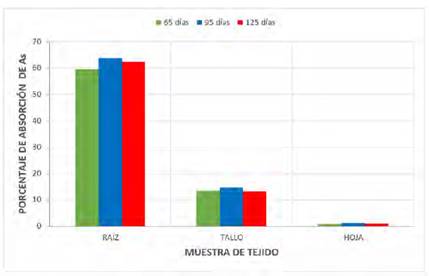
Fig. 11 Niveles de absorción comparativa de As en porcentaje en diversos órganos de la “beterraga” (Beta vulgaris L.)
Discusión
Con la finalidad de reducir la contaminación por metales pesados en los suelos de la región La Libertad, se planteó la necesidad de realizar el presente trabajo utilizando “maíz” y la “beterraga” como plantas fitorremediadoras. Para ello se emplearon suelos agrícolas contaminados por relaves mineros de la zona de Samne de la Región La Libertad, cuyos contenidos de plomo (Pb), arsénico (As) y cadmio (Cd) presentes en el suelo superan el Estándar de Calidad Ambiental (ECA) de suelos del Perú (Cuadro 1).
Según Garbisu et al., 2008, la fitorremediación se fundamenta en la capacidad de algunas plantas para tolerar, absorber, acumular, metabolizar, volatilizar o estabilizar y degradar compuestos contaminantes, tanto orgánicos como inorgánicos. Esta tecnología se está aplicando en diversos países, con la finalidad de recuperar los suelos contaminados, ya que esta fitotecnología tiene muchas ventajas con respecto a los métodos fisicoquímicos. Asimismo, Medina & Montano (2014), sostienen que un sistema eficiente de fitorremediación requiere especies de plantas que satisfagan requisitos como la tolerancia a metales pesados y capacidad de acumulación (Absorción, detoxificación y secuestro). Además, la planta ideal debería poseer la habilidad de sobrevivir a más de un metal en el medio de crecimiento, hecho que se ha comprobado en la experiencia tanto con el “maíz” como con la “beterraga”.
Asimismo, los resultados obtenidos en la presente investigación, guardan relación con los encontrados por Cubillos, 2011; Delgadillo et al., 2011 y Munive et al., 2018, sobre todo, en lo que concierne a los mecanismos fisiológicos implicados en la recuperación de los suelos contaminados por metales pesados, más aún también en lo relacionado a la absorción específica de los metales pesados por las raíces de estas plantas y su acumulación en tallos y hojas, como son los casos del Pb, As y Cd y cuyos valores se encuentran descritos en los Cuadros 2,3,4 y 5.
Por otro lado, hoy en día en investigaciones sobre mitigación de impactos ambientales fundamentalmente en áreas mineras, se están utilizando diversidad de plantas denominadas biorremediadoras, y donde se toman como marcadores referenciales la biomasa de la planta, el número de hojas y la altura máxima de la planta como indicadores de toxicidad, hecho comprobado en la experiencia y que se observan en la Figura 14 (Arienzo et al., 2004).
La alta concentración principalmente de Pb en los suelos de experimentación, generó una clara toxicidad en el “maíz” (Fig. 13), donde se observa una disminución en el crecimiento de las plantas que sobrevivieron, hecho que no sucedió con la “beterraga” si comparamos ambas especies con las del grupo control.

Fig. 13 Material colectado listo para análisis de los metales pesados plomo, arsenico y cadmio en el “maíz” (Zea mays L.)

Fig. 14 Medidas del material colectado para análisis de biomasa y medidas morfométricas del “maíz” (Zea mays L.).

Fig. 15 Material colectado para análisis de los metales pesados plomo, arsénico y cadmio en la “beterraga” (Beta vulgaris L.).
La posible respuesta diferencial encontrada es explicada por Gough & Erdman (1977), quienes afirman, que entre las respuestas fisiológicas de los plantas frente a los efectos de los contaminantes como los metales pesados estos se relacionan con cambios en los procesos respiratorios, disminución de la concentración de ATP, alteraciones en la fijación del nitrógeno, acumulación de los elementos tóxicos y perjuicio en la reproducción; en razón de que parte de estos procesos ocasionan lentamente cambios ultraestructurales y modificaciones observables al microscopio de luz, como el porcentaje de muerte o de plasmólisis celular.
Los resultados observados en las Tablas 2, 3, 4 y 5 también permiten observar que los valores de Pb frente a los de As y Cd, son los que demuestran mayor absorción por parte del “maíz” y principalmente por la “beterraga”, seguidos luego del metal pesado Cd; resultado que nos confirman que este tipo de cultivos pueden ser utilizados como bioconcentradores y biorremediadores de ambientes terrestres contaminados por metales pesados, como lo sostienen Hawksworth & Rose (1970), Duffus (1983) y Simonson (1997).
Riffo (2016), recomienda que para calcular la capacidad hiperacumuladora de una planta como son los casos del “maíz” y la “beterraga”, se debe determinar, que tanto el factor de bioacumulación en la raíz como en la parte aérea, deben ser mayores a 1, por lo cual, se debe analizar éstas 2 partes de la planta. Asimismo, los factores de bioacumulación en la raíz (RAF), al dar valores mayores a 1 confirman que ambas plantas “maíz” y “beterraga” son acumuladoras de Pb y por lo tanto este metal es translocado hacia sus raíces. En el caso de As y Cd sus valores en raíz son menores a 1 significando que estas plantas son exclusoras para estos metales y por tanto las concentraciones de estos metales se mantienen en el suelo.
En cambio, los factores de bioacumulación en la parte aérea (SAF) para concentraciones determinadas, dieron valores mayores a 1 en el caso del tallo, y en el caso de la hoja menores a 1 para Pb, salvo durante el crecimiento a los 125 días donde todos los valores fueron menores a 1, lo cual significa que la planta es bioacumuladora también para el órgano tallo, con la salvedad que se satura conforme avanza el tiempo de crecimiento del vegetal. Comparativamente en el caso del As y Cd, al ser en todos los casos los valores menores que 1, tanto en el tallo como la hoja se les puede considerar como plantas exclusoras de acumulación de estos metales, y por lo tanto las mayores concentraciones se mantienen en el suelo, acumulando así, una menor cantidad de metales en la parte aérea. Estos resultados guardan relación con los encontrados por Gutierrez, et al., 2009.
El que exista un alto grado de absorción de Pb y Cd tanto en “maíz” como en “beterraga”, a partir de las concentraciones de estos metales presentes en el material de suelo contaminado por relaves, estaría relacionado con el hecho que en una serie de especies vegetales, sus mecanismos fisiológicos particulares hacen que esta característica de absorción de estos metales sea sostenida por encima del umbral de absorción, por ejemplo hasta los 125 días (Alkorta et al., 2010).
En forma preliminar se ha podido encontrar en el caso de la “beterraga” una alta respuesta incluso a desarrollar su crecimiento vegetativo en relave puro (Pb= 3399,00 mg/kg, As = 43,80 mg/kg y 36,23 mg/kg de Cadmio).
Conclusiones
El valor promedio máximo de concentración de plomo, arsénico y cadmio para el “maíz” (Zea mayz L.) fue de 371,66 mg/kg, 1,94 mg/kg y 14,82 mg/kg, mientras que para la “beterraga” (Beta vulgaris L.) los valores fueron de 432,95 mg/kg, 3,89 mg/kg y 13,88 mg/kg, determinados a nivel de raíz respectivamente.
Se pueden seleccionar a las especies “maíz” y “beterraga”, como organismos biorremediadores de suelos contaminados por Pb, debido a su alto poder de bioconcentración de este metal a nivel de raíz.
La relación de concentración de los metales pesados plomo, arsénico y cadmio en el “maíz” (Zea mayz L.) y “beterraga” (Beta vulgaris L.) es: Pb > As > Cd.
Preliminarmente se ha determinado el desarrollo vegetativo de la “beterraga” (Beta vulgaris L.) en relave puro.












 uBio
uBio