Introducción
Todos los seres vivos sufren accidentes como quemaduras, rupturas de tejidos o intervenciones quirúrgicas que causan diversas heridas y/o cicatrices. La necesidad en atender biológicamente las heridas graves y complejas, convierte este tema en la motivación de muchos investigadores que buscan un tratamiento eficaz, rápido y económico. El estudio de sustancias inorgánicas y orgánicas completamente efectivas sigue siendo un misterio científico, principalmente porque la curación es un proceso complejo que involucra muchos eventos para lograr buenos resultados (Salazar, 2014; Asto, 2015).
En términos del sistema de salud, el cuidado de heridas implica una inversión económica importante. En Estados Unidos, cerca de 6,5 millones de personas reportan lesiones crónicas, representando un costo anual de $25 mil millones (Bauer et al., 2019; Sen et al., 2009). En Latinoamérica, Colombia reporta una tasa de lesiones en la piel de 2.213% por 5000 ciudadanos. Brasil y México reportan estadísticas ligeramente superiores, pero con costos mensuales altamente elevados. En el Perú atienden el 60% de pacientes con heridas son hospitalizados, esto equivale a 11016 pacientes con heridas crónicas no resueltas cada año que requieren tratamiento especializado (Casado, 2020).
La curación de una herida constituye un proceso complejo y ordenado. Para los traumatismos mecánicos abiertos (heridas), se debe considerar tanto la restauración del estado original, como el cierre de la misma mediante la adhesión de los bordes con tejido conectivo reparador (cicatrización) y recubrimiento epitelial (regeneración) (García, 2021; Panarbo, 2016).
Dentro de las diversas terapias para el tratamiento de las heridas, existe la terapia botánica mediante el uso medicinal de las plantas, con múltiples reportes académicos de manera positiva en diferentes partes del mundo (Quintana & Santa María, 2019). En el Perú existen muchas plantas nativas e introducidas, con conocida propiedad curativa de manera ancestral o folclórica, pero aún no han sido estudiadas a través de diseños experimentales que permitan brindar un sustento académico a dichas propiedades. Una planta en estudio es Plantago major L. “llantén” (Al-jumaly et al., 2012), que tiene estudios positivos sobre actividad antiinflamatoria (Arias, 2018) pero no se reportes estudios de actividad cicatrizante o sobre regeneración.
El alto contenido en taninos en P. major teóricamente le brinda propiedades cicatrizantes y hemostáticas; asimismo, presenta la alantoína, sustancia con propiedades que estimula el crecimiento de las células epidérmicas (Kobeasy, 2011); toda esta información nos permite tener la base para el desarrollo de diseños experimentales que puedan profundizar el beneficio que podría brindar esta planta en temas de regeneración de tejidos.
Para abordar un estudio en regeneración de tejidos la primera línea emplea modelos biológicos. Dentro de los modelos biológicos ideales para estudios de regeneración se señala a los platelmintos por su natural alta capacidad regenerativa. En el Perú se cuenta con la planaria Girardia festae donde se ha comprobado diferentes sustancias orgánicas e inorgánicas que reportan promoción de la regeneración de tejidos (Pinto, 2020; Cornejo et al., 2020).
Frente a ello, la presente investigación buscó determinar el efecto de cinco concentraciones del extracto acuoso de hojas de Plantago major L. sobre la capacidad de regeneración Girardia festae, un modelo biológico ideal en el estudio de temas de regeneración de tejidos.
Material y métodos
Se colectaron ejemplares de Girardia festae en cuerpos de agua (-8.108014, -78.939049) de la zona de Conache, Distrito Laredo, Provincia de Trujillo, libres de laceración alguna a simple vista y con una longitud entre 15 a 17mm. La identificación taxonómica estuvo a cargo de la Sección de Zoología de la Universidad Nacional de Trujillo. La crianza y evaluación de los especímenes se realizó en el Laboratorio de Citometría; la alimentación utilizó hígado de pollo, aireación 2horas/día y una renovación de agua interdiaria. Se registró una humedad relativa de 82% y una temperatura promedio 20°C.
La recolección de Plantago major L. (Plantaginaceae) “llantén” se realizó en la Estación Experimental de Bioquímica Aplicada en la Universidad Nacional de Trujillo. Las muestras obtenidas fueron herborizadas e identificadas en el Herbario Truxillense (HUT) con código de depósito 60993.
Para la obtención del extracto acuoso de Plantago major L., se pesó 30 gramos de hojas secadas previamente a estufa a 65°C por 24 horas. Se preparó el decocto, manteniendo la ebullición por 10 minutos, y luego se procedió a preparar diluciones al 25%, 50%, 75% y 100% que asumirán el papel de tratamientos (Ángulo, 2018; Herrera, 2018; León, 2016; Al-jumaly et al., 2012).
Previa aplicación de los tratamientos se procedió a obtener los diferentes fragmentos de Girardia festae seleccionándose 350 fragmentos obtenidos por corte transversal (fragmentos superior e inferior), doble transversal (fragmentos cefálico, medio y caudal) y longitudinal (fragmento derecho e izquierdo). La aplicación de las diferentes concentraciones de P. major a los diferentes tipos de fragmentos de G. festae fue por 7 minutos, pasados los cuales se procedió a individualizar cada fragmento en tubos de ensayo donde se realizó el seguimiento hasta su regeneración total a individuo completo. Empleando microscopía óptica se realizaron tomas fotográficas del proceso regenerativo utilizando el software AmScope a 10x de aumento. Con los datos obtenidos se realizó el análisis de varianza y test de comparación de medias empleando el paquete estadístico Statgraphics Plus Versión 18.0 (Herrera, 2018).
Resultados y discusión
Las planarias Girardia festae pueden sufrir cambios drásticos en el tamaño del cuerpo por diferente tipo de injuria e incluso así llegar a regenerar su organismo completo. Esta notable capacidad de regeneración las convirtió en el modelo biológico ideal para analizar fenómenos como la morfogénesis, polaridades y restauración de patrones y la homeostasis tisular. Esta capacidad reside en ellas ya que cuentan con células pluripotentes que pueden dar lugar a los diferentes tipos de células diferenciadas (Saló et al, 2009), por este motivo son utilizadas en diversos estudios para medir su capacidad de regeneración cuando se enfrentan a diferentes agentes biológicos (Urritia, 2015; Veliz, 2017; Zavala, 2017).
Cuando hay una lesión celular, se inicia dentro de Girardia festae una cascada de interacciones bioquímicas y celulares, guiadas por la actividad de múltiples agentes químicos que provocan cambios; sin embargo, la respuesta inflamatoria es el evento que químicamente determinar el inicio y la señalización del proceso de regeneración del tejido lesionado (Cornejo et al., 2020; León et al., 2015).
En la Figura 1 se muestran los tiempos en horas de lo que demandó la regeneración completa de especímenes de Girardia festae a partir de siete tipos diferentes de fragmentos y frente a la exposición de cinco concentraciones diferentes de Plantago major L., contabilizando 10 repeticiones para cada tratamiento dentro de cada bloque, con un total de 350 unidades experimentales. En la figura se logra observar dentro de cada uno de los bloques (tipo de fragmentos) un comportamiento indirectamente proporcional, donde a mayor concentración de P. major.
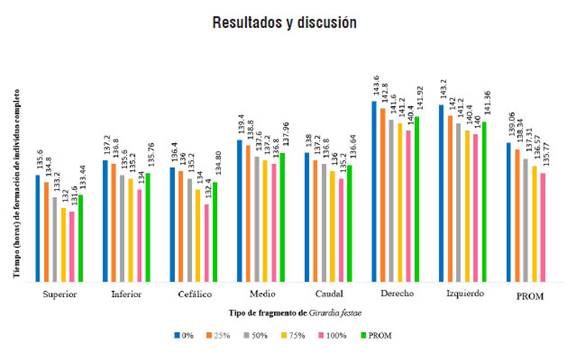
Fig. 1 Tiempo de regeneración de diferentes fragmentos de Girardia festae por efecto de diferentes concentraciones de extracto acuoso de Plantago major L. “llantén”.
En la misma Figura 1, se observa que los fragmentos que contienen los ganglios cerebrales (fragmento superior y cefálico) regeneran en menor tiempo (133.44 y 134.80 horas respectivamente) que los otros tipos de fragmentos; ello haría notorio que la capacidad de regeneración está asociada a la actividad nerviosa cerebral (Pinto, 2020). Asimismo, se logra determinar que los fragmentos obtenidos por corte longitudinal son los que demandan mayor tiempo de regeneración (141,92 y 141,36 horas); lo que coindice con diferentes investigaciones que emplearon estimulantes de la regeneración celular de tipo orgánico como inorgánico (Cornejo et al., 2020; Pinto, 2020; Ángulo, 2018).
El análisis de varianza determinó la presencia de diferencias significativas dentro de cada bloque, y el posterior test de comparación de medias determinó que cada concentración de P. major se considera un grupo homogéneo diferente; demostrándose una significativa significancia de una concentración a otra, y para cada uno de los tipos de fragmentos de G. festae.
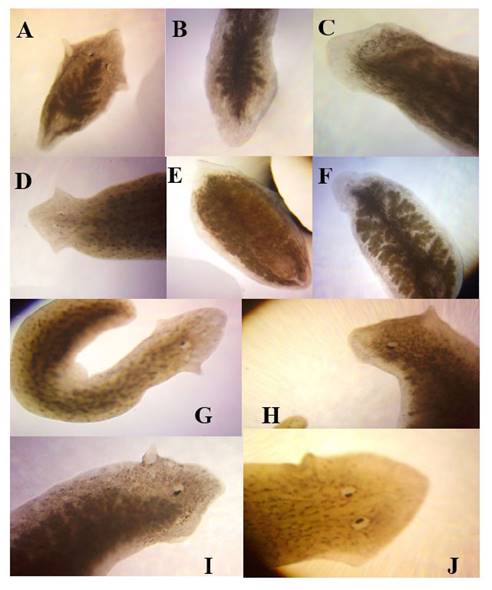
La Figura 2 nos muestra la regeneración de los diferentes fragmentos de G. festae. En la imagen A y B, se aprecia el desarrollo del fragmento inferior a partir del superior, apreciándose una pronta y mejor delimitación de bordes, en tanto las imágenes C y D señalan la regeneración del fragmento superior a partir del fragmento inferior, donde se aprecia la formación de la parte cefálica de espécimen sin pigmentación temprana, ello obedecería a lo complejo que es regenerar los nervios craneales. Los fragmentos E y F, nos muestran la regeneración de los fragmentos medios, donde de manera precisa por señalización molecular los fragmentos regeneran la parte cefálica y la parte caudal en los extremos correspondientes, regenerándose más rápido la parte cefálica.












 uBio
uBio