Introducción
La contaminación por metales pesados es una de las formas más peligrosas de contaminación de las aguas continentales y marinas, debido a que no son biodegradables, contrariamente a la gran mayoría de los contaminantes de tipo orgánico. Además, pueden ser bioacumulados en forma iónica o de compuestos orgánicos y permanecer en los organismos por largos períodos e incluso causarles la muerte (Campos, 1990; Saldaña, 2016; Acuña et al., 2021).
Desde hace varios años, muchas instituciones mundiales están promoviendo programas de evaluación y conservación de la capacidad productiva de los recursos acuáticos vivientes, para determinar fundamentalmente la interacción entre las actividades del hombre y el medio ambiente, incluyendo problemas de deposición de desechos y polución. Una de las prioridades es formular metodologías propias a fin de evaluar el estado de los ambientes acuáticos y su administración en relación a la protección de los recursos vivos, particularmente en ríos, lagos, lagunas, estuarios y áreas costeras, donde la polución ya presenta problemas urgentes (Valenzuela, 1983; Tommasi et al., 1984; Rayme, 2015; Pinto & Valbuena, 2020).
Un aspecto importante del estudio de la contaminación acuática, es lo relacionado a las pruebas ecotoxicológicas de bioensayos que deben ser conducidos para las sustancias que comúnmente son eliminadas con los productos de desecho de las actividades del hombre, particularmente los relaves mineros. De estas sustancias, los metales pesados como el cobre, zinc, plomo, mercurio, arsénico, cadmio, cromo y hierro, que se encuentran en reacción de equilibrio en el ambiente acuático, frecuentemente son acumulados en los tejidos de los recursos vivos causando efectos de inhibición enzimática y teratológicos, así como en muchos casos la muerte subsecuente (Gallardo, 1984; Sánchez & Tupayachi, 1988; Conga, 2017; Dzul, 2018; Santillán, 2020; Chujutalli & Fustamante, 2020; Gastelum et al. (2019).
Los bioensayos de toxicidad permiten evaluar el grado de afectación que una sustancia química tiene en organismos vivos y éstos pueden ser agudos o crónicos. Las pruebas agudas cuantifican las concentraciones letales de un xenobiótico a una especie en particular. El valor calculado se denomina concentración letal media (CL50) y corresponde a la concentración de un xenobiótico que causa la muerte al 50 % de la población experimental al cabo de un tiempo determinado, generalmente en 48 o 96 horas. En contraste, las pruebas crónicas estiman la concentración - efecto medio (CL50) de la sustancia de prueba que causa un efecto sobre el 50 % de la población experimental, al cabo de un tiempo determinado; dentro de las metodologías muy utilizadas para validar los bioensayos ecotoxicológicos se mencionan a las llamadas pruebas probit (Reish & Oshida, 1987; Corpus, 2010; Scotto et al., 2016; Paredes & Miglio, 2018; Vásquez et al., 2018).
Actualmente, se vienen empleando en casi todo el mundo, ensayos ecotoxicológicos como sistemas efectivos de alerta ambiental que orientan a la toma de decisiones nacionales en la protección de sus recursos naturales en busca del desarrollo sostenible de los países. El fundamento de estos ensayos ecotoxicológicos es la determinación de valores límites de las sustancias tóxicas en el ambiente, empleando a los sistemas biológicos como sensores ambientales.
Dentro de las investigaciones sobre bioensayos de toxicidad realizados en organismos acuáticos como los peces utilizando metales pesados y una serie de contaminantes podemos mencionar a: Doudoroff & Katz, 1953; Tompkins and Bridges, 1958; Anderson, 1964; Chung, 1978; Wienner, 1984; Gianotti, 1986; Corpus, 2010; Scotto et al., 2016; Dzul, 2018; Pinto & Valbuena, 2020. En el Perú, los estudios de este tipo se van consolidando por la importancia de la generación de residuos tóxicos como los metales pesados de la industria minera, destacándose las investigaciones de Bustamante (1978) en el “camarón de río” Cryphiops caementarius;Tommasi et al. (1984) en Artemia salina, Sanchez y Tupayachi (1988) en la “concha de abanico” Argopecten purpuratus;Rayme (2015) en la “trucha arco iris” Oncorhynchus mykiss; Saldaña (2016) en la “gamitana”; Scoto et al. (2016) en los “peces cebra” Danio rerio; Conga (2017) en Rhinella spinosa; Mamani (2020) en Daphnia pulex;Chujutalli & Fustamante (2020) en alevines de “paco”, “gamitana” y “trucha arco iris”; Acuña et al. (2021) en peces de la amazonía; Urviola, 2022 en Poecilia reticulata; quienes han reportado experimentos utilizando cobre, hierro, plomo, mercurio, aluminio, bario, hidrocarburos, sedimentos, insecticidas, detergentes, artículos de limpieza y aguas residuales de lagunas de oxidación. Todos estos metales pesados y contaminantes han demostrado efectos letales sobre las especies mencionadas aún cuando a diferentes concentraciones.
Por las consideraciones expuestas, se planteó investigar los niveles de toxicidad letal a diferentes concentraciones de hierro, y a distintos tiempos de exposición sobre P. reticulata; lo cual se verificó estimando el porcentaje de mortalidad en cinco concentraciones diferentes de hierro, para determinar la toxicidad letal en P. reticulata; y establecer la dosis letal media LC50-96h para el contaminante probado, en un tiempo de 96 horas como máximo.
Material y métodos
La muestra biológica estuvo constituida por 360 ejemplares adultos de P. reticulata capturados en el dren derecho de Víctor Larco, Provincia de Trujillo, Departamento de La Libertad (Fig. 1, 2 y 3). El método utilizado fue el propuesto por Reish and Oshida (1987) para bioensayos estáticos de tipo respuesta letal directa y de corto período; preparándose una solución stock de 1000 mg/L de hierro a partir de sulfato ferroso heptahidratado (FeSO4.7H2O). Posteriormente se realizó las diluciones apropiadas en agua filtrada declorada colectada del aprovisionamiento de la Ciudad Universitaria de la Universidad Nacional de Trujillo/Perú. El agua colectada tenía un pH de 7,1; una dureza de calcio de 20 a 30 mg/L; el oxígeno disuelto osciló entre valores de 5,5 y 6,5 mg/L de O2 ; temperatura con un rango entre 18ºC y 22ºC, y sin la presencia de concentración alguna del metal experimentado. Luego se determinaron cinco concentraciones experimentales en mg/L, los que se seleccionaron a través de pruebas exploratorias de bioensayos.
Basándose en los protocolos establecidos por Reish & Oshida (1987), se utilizaron baterías de peceras de 2,0 L de capacidad, con cinco (5) concentraciones además del blanco, cada concentración con tres (3) réplicas de ensayo (peceras), para un total de dieciocho (18) peceras para la prueba toxicológica. En cada pecera se introdujeron diez organismos. El total de organismos utilizados son de treinta (30) por cada concentración y ciento ochenta (180) por prueba toxicológica. Para el montaje se ubicaron las peceras en un stand acondicionado para las pruebas en el laboratorio de Ecología de la Universidad Nacional de Trujillo/Perú (Fig.4 y 5). La lectura de las pruebas se realizó a las 24, 48, 72 y 96 horas de haberse iniciado la prueba, registrando cada resultado en una tabla de datos (Tabla 1). El cese del movimiento opercular fue el criterio utilizado para considerar la muerte del pez.
Los resultados de la prueba se obtuvieron por medio del análisis estadístico Probit (Ney and Stevens, 1948; Aytac, 2013) y utilizando el software estadístico SPPS 26, con una confiabilidad del 95%, siguiendo un modelo matemático que asume una relación entre la dosis y la respuesta. Este calcula la CL50-96h con sus respectivos límites de confianza, para ello se elaboró el protocolo "Análisis de regresión y Análisis Probit".
El experimento fue planificado para utilizar un diseño completamente al azar, trabajando con cinco concentraciones, cuatro tiempos de registro y tres repeticiones para cada combinación de tratamiento (Calzada, 1970). La identificación de la especie se hizo utilizando la clave para peces teleosteos de Jordan and Evermann (1963).
Resultados
Los resultados de los bioensayos de toxicidad aguda se obtuvieron por medio del Método Probit, con una confiabilidad del 95%, siguiendo un modelo matemático que asume una relación entre la dosis y la respuesta. Este calcula la CL50-96h con sus respectivos límites de confianza, para ello se elaboró el protocolo sobre "Análisis de regresión y Análisis Probit". Luego de adquirir este resultado, se realiza el análisis de varianza, según el protocolo "Análisis de varianza - ANOVA". Se trata de una técnica para comparar si los valores de un conjunto de datos numéricos son significativamente distintos a los valores de otro o más conjuntos de datos entre las concentraciones de hierro. El procedimiento para comparar estos valores está basado en la varianza global observada en los grupos de datos numéricos a comparar.
Del análisis experimental, se puede observar que la menor mortalidad para los juveniles del “guppy” sometidos a la acción de toxicidad aguda para el Fe, se obtuvieron en el tratamiento T2 a las 24 horas de experimentación, mediante el cual se estableció que la mortalidad aumentaba con el incremento de la dosis de Fe (Tabla 1). En los experimentos la mortalidad en el grupo control fue de 0,00 %, por lo tanto la prueba puede ser referenciada como válida.
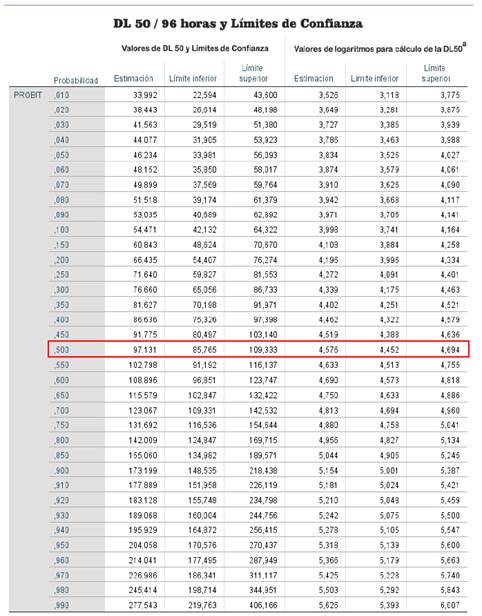
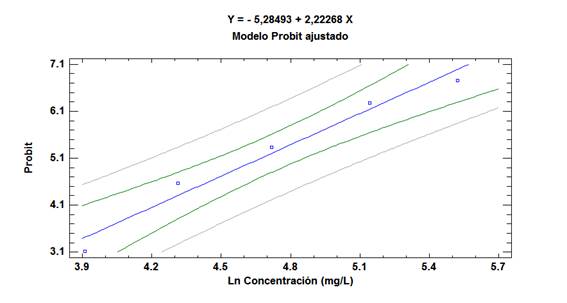
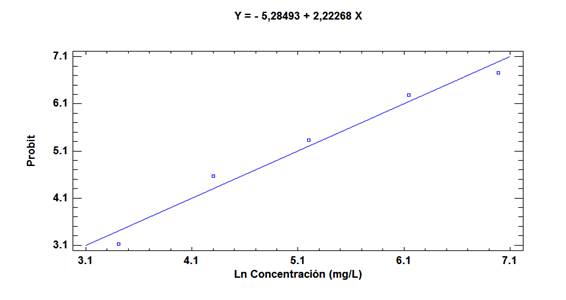
Para corroborar gráficamente esta información (Fig. 4) y con base en las Tablas 2 y 3, se realizó un gráfico de dosis-respuesta, porque tanto el análisis Probit como el gráfico de dosis-respuesta permiten utilizar una curva de respuesta sigmoidal como es el caso de la investigación presente, o transformarla mediante regresión lineal (Fig. 5). La ventaja del gráfico de dosis-respuesta es que no solo proporciona el valor de la DL50, sino que también por ejemplo los correspondientes a la DL20 o DL80 (Tabla 4). En las Figs. 4 y 5; puede observarse la regresión Probit obtenida a partir de valores de mortalidad frente a las dosis de hierro.
La DL50-96h de 97,131 mg/L determinada para el hierro en los cuales hubo el 50% de mortalidad de P.reticulata, se complementa con los límites superior e inferior con el 95% de probabilidad, los cuales están en el rango de 85,765 a 109,333 mg/L respectivamente (Anexo 3), con un R2 de 97,09% que prueba la bondad de ajuste significativa del modelo Probit utilizado en la determinación experimental del DL50-96h trabajando en las condiciones experimentales de laboratorio establecidas (Tabla 5).
Discusión
Las investigaciones sobre el particular, han confirmado que las especies presentan distintas sensibilidades a la toxicidad de los diversos metales, las cuales se deben en primer lugar a las variaciones biológicas naturales de la composición genética de las poblaciones y condiciones individuales de los peces. Es usual que la variación sea menor dentro de una especie, considerando los estadios, la condición de salud, condiciones del medio natural de origen; y mayor entre especies (Zakaria et al., 2016). Asimismo, los resultados obtenidos en los ensayos de toxicidad podrían estar influenciados por la historia de vida de los peces empleados, de donde provienen (OECD, 2014).
Asimismo, el efecto letal de los metales como es el caso del hierro, ha sido relacionado con la coagulación del mucus de la superficie de las agallas, daño al tejido de las agallas y consecuentemente falla en la respiración (Authman et al., 2015). Características como el incremento del movimiento opercular han sido observados en peces expuestos a algunos metales pesados, como es el caso de la presente investigación (Wang et al., 2013). Los síntomas por intoxicación aguda de metales pesados en peces comprenden, rigidez del cuerpo, disminución de la motilidad y suspensión en la zona superficial con la parte posterior del cuerpo dirigida hacia el fondo; estos síntomas son seguidos por la pérdida de balance y finalmente por el hundimiento del individuo en el fondo antes de la muerte (Sehgal & Saxena, 1987). Todos estos síntomas fueron observados durante los ensayos experimentales de laboratorio.
La diferencia del nivel de toxicidad del metal pesado hierro del presente estudio y otras investigaciones, podrían estar relacionadas con los siguientes factores: características del agua de dilución (dureza, pH, temperatura, entre otros), características químicas del metal experimentado, especies y estadíos (larva, alevín, juvenil, adulto) de los organismos de prueba, y aclimatación, entre otros, los cuales pueden modificar la toxicidad de los metales (Sprague, 1985, Spehar & Fiandt, 1986). En agua blanda, el efecto tóxico de los metales puede llegar a ser de 5 a 30 veces más potente que en agua dura (Canton & Slooff, 1982). En los diversos estudios, se ha registrado que a mayor tiempo de exposición la CL50 disminuye, es decir que, el contaminante se vuelve más tóxico, y la tasa de individuos afectados, de manera letal y subletal, se incrementa (Zakaria et al., 2016).
Particularmente, en el caso de los estadios de los organismos vivos, algunos investigadores indican que las larvas generalmente son el estadio más sensible de los peces para contaminantes, tales como los metales (Alsop & Wood, 2011). Sin embargo, muchos estudios, han demostrado tener resultados opuestos, como el de Buhl & Hamilton (1991) quienes identificaron que los juveniles fueron más sensibles a los tóxicos (entre ellos arsénico, cadmio y mercurio) que los alevines.
Con los valores de mortalidad de los organismos a cada concentración de hierro ensayados (Tabla 1), se observa que la sensibilidad de P. reticulata está relacionado con el efecto combinado de las formas inorgánicas del hierro, mayormente Fe2+ y FeCO3, de acuerdo a Sprague (1964), Rehwoldt et al. (1971) y Romano et al. (2021). La calidad de las aguas, especialmente de las aguas blandas, fue corroborada también por Scotto et al. (2016) y Scotto et al. (2019) en su estudio de 10 especies de peces dulceacuícolas, dentro de las cuales se encuentra P. reticulata. Este mismo fenómeno se observa en la experiencia realizada por Bustamante (1978) en el camarón de río C. caementarius, en donde no obstante haber utilizado agua potable dura, los LC50-96h para metales como el cobre, zinc y hierro tuvieron este mismo comportamiento.
Asimismo, Alabaster and Lloyd (1980), manifiestan que las concentraciones mayores a 10 mg/L de hierro son letales para los organismos acuáticos, la diferencia puede ser atribuida mayormente a las diferentes durezas del agua, especies de organismos, duración de la prueba y fase del ciclo de vida.
En relación con el hierro, Doudoroff & Katz (1953) en aguas blandas, encontraron que para el C. auratus, un LC50 de 37 mg/L a 96 horas, que difiere significativamente del valor obtenido para P. reticulata cuyo LC50 fue de 97,131 mg/L (Tabla 3 y Anexo 3). En crustáceos, Anderson (1964) determinó una LC50 para Daphnia magna del lago Erie de 30,62 mg/l, en cambio Bustamante (1978) reporta para el “camarón de río” C. caementarius una LC50 de 102,74 mg/l de hierro en agua dulce dura.
Conociéndose que la respuesta de los organismos acuáticos a la toxicidad de los metales pesados está determinada por una serie de variables, Wienner (1984) y Gianotti (1986), afirman que la respuesta más sobresaliente se da a nivel de las diferentes durezas del agua de experimentación, de aquí que la variación de los valores LC50 a diferentes durezas pueden ser debidas a variaciones en la sensibilidad de las branquias de estos organismos, frente a distintas durezas y metales o que las tasas en las cuales se dañan las branquias son diferentes y dependen de la combinación de dureza y metales.
En la Fig. 1, se observa que conforme avanza el tiempo de exposición la LC50 disminuye, tal como sucede en otras especies experimentadas (Chung, 1978; Bustamante, 1978; Ahsanullah & Arnott, 1978), sugiriendo que una relativa prolongada exposición es necesaria para permitir una adecuada concentración de estos contaminantes a fin de penetrar en los tejidos de los organismos sometidos a las pruebas de bioensayo.
Conclusiones
De los resultados obtenidos en el presente trabajo se concluye lo siguiente:
La concentración letal de hierro de 250 mg/l causó el 96,66 % de mortalidad en P. reticulata en un tiempo de 24 horas, siendo su LC50-96h de 97,131 mg/L a las 96 horas de exposición.
P. reticulata, por ser una especie resistente al contaminante probado, puede servir de indicador biológico del grado de contaminación de peces de agua dulce.












 uBio
uBio