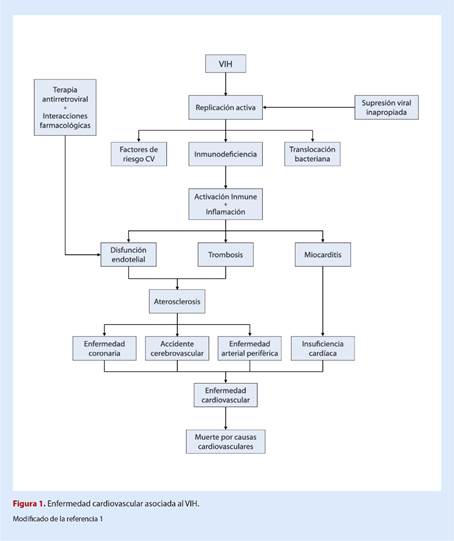
Introducción
Las personas infectadas por el Virus de Inmunodeficiencia Humana (VIH) tienen un riesgo incrementado de enfermedad cardiovascular al compararse con las personas sin esta condición. Los mecanismos asociados son: factores dependientes de la infección viral, de la terapia antiretroviral que reciben, así como relacionados con factores tradicionales y no tradicionales de enfermedad cardiovascular 1.
Se conoce que esta infección puede generar un estado profundo de inmunosupresión, la cual predispone a los pacientes a una serie de infecciones por agentes no convencionales, neoplasias malignas y a un mal funcionamiento progresivo de diferentes órganos y sistemas 2.
El compromiso cardíaco en pacientes con Síndrome de Inmunodeficiencia Adquirida (SIDA), el cual es el estadío más avanzado de la infección, fue descrito en el año 1983 por Austran, quien reportó sarcoma de Kaposi miocárdico en una necropsia. Después de ello, se han realizado una serie de estudios epidemiológicos en pacientes en diferentes estadíos de enfermedad, hospitalizados y manejados ambulatoriamente, recibiendo o no terapia antiretroviral. También se han establecido diferentes perfiles de seguridad con el empleo de agentes antiretrovirales, los cuales son excelentes estrategias para mejorar la función del sistema inmune y reducir la carga viral, pero que pueden tener algunos eventos adversos sobre el corazón o los vasos sanguíneos, o que pueden asociarse a un incremento de los clásicos factores de riesgo cardiovasculares, como son hipertensión, diabetes, dislipidemia, entre otros 2.
Desde 1983, año en que se reportó el primer caso de SIDA en el Perú, a Setiembre del 2021 se han notificado un total de 143,732 casos de infección por VIH, de los cuales 46,641 han sido diagnosticados en estadío SIDA. La relación hombre/mujer es de aproximadamente 3:1 estando el 50% de casos de infección por VIH y en estadío SIDA, entre 20 y 34 años 3.
A continuación, haremos una descripción del compromiso cardiovascular asociado a la infección por VIH, con una mención inicial a algunos estudios locales.
Entre los años 2001 y 2003 se realizó un estudio prospectivo comparativo en los hospitales Guillermo Almenara (EsSalud) y Cayetano Heredia (Ministerio de Salud, MINSA), evaluándose a 164 pacientes en estadío SIDA. Los resultados no encontraron diferencias en el compromiso cardiovascular evaluado por ecocardiografía. Se encontró disfunción diastólica del ventrículo izquierdo en el 26.82% de casos, derrame pericárdico en el 9.75%, disfunción sistólica del ventrículo izquierdo en el 1.82% y signos compatibles con hipertensión pulmonar en el 2.43% de casos 4.
Adicionalmente, entre los años 1996 y 2012 se realizó un estudio retrospectivo en el Hospital Edgardo Rebagliati (EsSalud). Se revisaron 510 historias clínicas de pacientes hospitalizados en el servicio de infectología con diagnóstico de infección por VIH en cualquier estadío de enfermedad. Se registró compromiso cardiovascular en 26 pacientes. Once de ellos tuvieron compromiso cardíaco (42.3%) y 15 (57.7%) compromiso no cardíaco. Las causas de compromiso cardíaco fueron derrame pericárdico (4 casos), infarto de miocardio (3 casos), miocarditis (2 casos), endocarditis bacteriana (1 caso) e insuficiencia cardíaca (1 caso). De las causas vasculares no cardíacas se encontraron trombosis venosa profunda (6 casos), desórdenes cerebrovasculares (5 casos), hipertensión pulmonar (3 casos) y embolia pulmonar (1 caso) 5.
1.1. Compromiso cardíaco
El compromiso cardíaco incluye a diferentes síndromes clínicos, cuya prevalencia puede variar en función al uso de terapia antiretroviral (Tablas 1 y 2)
Tabla 1 Compromiso cardiovascular en la infección por VIH
| Compromiso cardiovascular | Síndromes clínicos asociados |
|---|---|
| Cardíacas | |
| Miocárdicas -Cardiomiopatía dilatada -Miocarditis -Infarto de miocardio -Hipertensión pulmonar -Enfermedad arterial coronaria -Neoplasias | Insuficiencia cardíaca, arritmias Insuficiencia cardíaca, arritmias Insuficiencia cardíaca, arritmias Insuficiencia cardíaca, embolia pulmonar, infarto pulmonar Angina inestable, infarto de miocardio, arritmias Arritmias, taponamiento cardíaco |
| Endocárdicas -Endocarditis infecciosa -Endocarditis trombótica no bacteriana | Choque séptico, insuficiencia cardíaca, embolia séptica Embolización sistémica, coagulación intravascular diseminada |
| Pericárdicas -Derrame pericárdico -Pericarditis | Taponamiento cardíaco, arritmias, insuficiencia cardíaca Insuficiencia cardíaca |
| Extracardíacas | |
| -Ateroscleróticas -Tromboembólicas | Accidentes cerebrovasculares Trombosis venosa profunda, tromboembolia pulmonar |
| Eventos adversos de la medicación o interacciones farmacológicas | Arritmias, incremento de aterosclerosis |
| Enfermedad arterial periférica | Isquemia arterial, isquemia crítica |
| Arritmias | Accidentes cerebrovasculares, muerte súbita cardíaca, insuficiencia cardíaca |
Construido con datos de 2,35-37
Tabla 2 Efecto de la terapia antirretroviral de gran eficacia (TARGA) sobre la frecuencia de manifestaciones cardíacas
| Manifestación cardiovascular | Antes de la TARGA | Después de la TARGA |
|---|---|---|
| Derrame pericárdico | 40% de prevalencia en pacientes con estadio SIDA. Taponamiento cardíaco en 5-30% de pacientes | Muy rara |
| Miocarditis | Más del 40% en autopsias | Muy rara |
| Cardiomiopatía dilatada | 17,7% | Muy rara |
| Hipertensión pulmonar | 0,5% | 0.5% |
| Enfermedad arterial periférica | Datos no concluyentes | Principal causa de muerte y discapacidad actualmente |
construido con datos de 2,35-37
1.1. Compromiso miocárdico
1.1.1.Cardiomiopatía dilatada
La infección por el VIH ha sido reconocida como una causa significativa de miocardiopatía adquirida, la cual tiene una prevalencia menor en la época posterior al empleo de terapia antiretroviral, probablemente por la reducción de las infecciones por gérmenes oportunistas. En la época previa a la terapia antiretroviral, su prevalencia era de 3.6% entre todos los pacientes con cardiomiopatía, y con características diferentes en cuanto a pronóstico, pues su probabilidad de muerte es cuatro veces mayor en comparación con los pacientes con cardiomiopatía dilatada sin infección por VIH 2,6. Las características histopatológicas son similares a los pacientes no infectados, con evidencia de hipertrofia y degeneración de miocitos, con incremento del colágeno intersticial y fibrilar endocárdico, y evidencia de miocarditis, mientras que las características macroscópicas incluyen la dilatación de las cámaras cardíacas con fibrosis endocárdica y trombos murales 2-6. Además de la contribución etiológica de la infección por el VIH, se han propuesto otras causas como las deficiencias de vitamina B12, selenio, carnitina, hormona de crecimiento, hormonas tiroideas, en presencia o no, de síndromes de malabsorción. También se ha descrito la cardiotoxicidad farmacológica (descrita para la zidovudina), la cual genera una destrucción difusa de las ultraestructuras celulares y la inhibición en la replicación del ADN, lo cual generaría un estado de acidosis capaz de amplificar este fenómeno patológico 2,6.
La ecocardiografía es la primera opción durante el proceso diagnóstico y permitirá la evaluación de la función sistólica del ventrículo izquierdo, las anormalidades en la motilidad segmentaria, así como la función diastólica, para el diagnóstico diferencial. La resonancia magnética cardíaca debe considerarse como un método complementario pues permitirá valorar la morfología y función ventricular, la fibrosis miocárdica, el edema miocárdico, el realce tardío de gadolinio y el pronóstico, así como datos para el diagnóstico diferencial. Sin embargo, el estudio histopatológico es la “prueba de oro” (7,8.
1.1.2. Miocarditis
La afectación miocárdica es en parche, sin una asociación entre la carga viral y la disfunción de los cardiomiocitos. Ello ocurriría por otros mecanismos, como la presencia de agentes como Mycobacterium tuberculosis, Mycobacterium avium, Toxoplasma gondii, Cryptococcus neoformans, Histoplasma capsulatum, Herpes simplex, Parvovirus, cocksackievirus B3 y Citomegalovirus2,7,8.
En los estudios de autopsias, en la época anterior a la terapia antiretroviral fue documentada entre 40 a 52% en pacientes fallecidos en estadío SIDA, sin una etiología definida en el 80% de los casos 2,8.
Shaboodien et al, en el año 2013 compararon la prevalencia de miocarditis y los genomas cardiotrópicos virales en pacientes con miocardiopatía asociada al VIH, cardiomiopatía dilatada idiopática y pacientes receptores de trasplante cardíaco, encontrando miocarditis presente en 44%, 25% y 36% de los grupos, respectivamente. Adicionalmente, la miocarditis fue aguda en el 50% de los pacientes con miocardiopatía asociada al VIH y asociada al trasplante, y crónica en todos los pacientes con miocardiopatía dilatada idiopática, encontrándose también infecciones cardiotrópicas virales en todos los casos de cardiomiopatía asociada al VIH y miocardiopatía dilatada, y en el 90% de los pacientes receptores de trasplante cardíaco 7.
1.1.3. Disfunción ventricular derecha e hipertensión pulmonar
Los síntomas y el pronóstico de los pacientes con hipertensión pulmonar son diferentes de acuerdo a la severidad de la infección, encontrándose desde pacientes asintomáticos u oligosintomáticos, hasta otro grupo con insuficiencia cardíaca avanzada y cor pulmonale. Se ha descrito que en general, los pacientes con esta condición tienen un tiempo de supervivencia menor en comparación con aquellos que no la presentan (1,3 años versus 2,6 años) 2,9-11.
La prevalencia aceptada de hipertensión pulmonar en pacientes infectados es de 0.5%, considerando los datos de una cohorte suiza de 1200 pacientes evaluados con ecografía transtorácica por síntomas respiratorios. Esta prevalencia se confirmó en un estudio francés de 7648 pacientes, evaluados también por ecocardiografía, postulándose que la terapia antiretroviral no modificaría la prevalencia de esta condición 12.
El mecanismo por el cual ocurre esta condición no está completamente entendido, pues no hay datos que avalen que el VIH infecte las células endoteliales de la arteria pulmonar y que los ácidos nucleicos se encuentren en los vasos pulmonares. Sin embargo, las proteínas virales pueden generar remodelamiento vascular, proliferación de las células vasculares endoteliales, inducción de inflamación, estrés oxidativo y disregulación de la apoptosis (12.
Su presentación es indistinguible de la forma idiopática, siendo los síntomas más importantes la disnea progresiva (86%), edema en pies (30%), tos no productiva (19%), fatiga (13%), síncope o pre-síncope (12%) y dolor torácico (7%), pudiendo ayudar el ecocardiograma como un método de tamizaje sobre todo en la subpoblación con factores de riesgo (género femenino, uso de cocaína, uso de drogas endovenosas, infección por hepatitis C) 12.
Cuando la hipertensión pulmonar se presenta, es un predictor independiente de muerte y se asocia con una supervivencia pobre, empleándose como terapia la medicación convencional, pudiendo considerarse inhibidores de fosfodiesterasa, antagonistas de receptores de endotelina y análogos de prostaciclina 12.
1.1.4. Infarto de miocardio.
El proceso de aterosclerosis en personas con VIH no debería diferir significativamente del resto de la población siendo los procesos más importantes la disfunción endotelial de causas inmunes y no inmunes, la inflamación, la transformación de macrófagos en células espumosas y la apoptosis de las células espumosas. Debemos resaltar el rol pivotal que cumplen la activación de los monocitos (aún después del tratamiento antiretroviral), asociándose a inflamación persistente y activación inmune 13-15.
Se conocen también las propiedades aterogénicas de algunos antiretrovirales, el efecto de las proteínas virales Tat, Nef y gp120, la disminución de la proliferación muscular lisa en el medio inflamatorio, la coinfección con el citomegalovirus y hasta la contribución de los procesos de traslocación bacteriana a nivel intestinal (14.
De esta forma el mecanismo asociado en los síndromes coronarios en pacientes con infección por VIH parecería ser la ruptura y no tanto la erosión de la placa aterosclerótica, siendo dos factores asociados la trombosis y la disfunción microvascular 14.
Los pacientes con VIH generalmente presentan menor inflamación de placa, más probabilidad de compromiso de un solo vaso, una menor puntuación de TIMI (Thrombolysis in Myocardial Infarction risk), y una mayor probabilidad de lesiones proximales en comparación con individuos sin infección 16.
Un metaanálisis con datos de estudios entre el 2003 y el 2015, sugirió que después de la intervención coronaria percutánea, los pacientes con infección por VIH tienen similar mortalidad, muerte por causas cardiovasculares e infarto de miocardio recurrente, en un seguimiento a 3 años. Esta tendencia se mantiene en individuos con enfermedad coronaria avanzada, en quienes se requiere cirugía de revascularización miocárdica, observándose una mortalidad similar a corto plazo, pero una leve tendencia a requerir una mayor proporción de transfusiones postoperatorias y una mayor proporción de eventos cardiovasculares a largo plazo 16.
1.1.5 Neoplasias cardíacas
Los linfomas no Hodgkin (LNH) cardíacos son infrecuentes en el SIDA, apareciendo de manera importante o restringida de forma nodular, o inclusive de aspecto polipoideo. El compromiso puede afectar al pericardio y más raramente al miocardio y casi no se acompaña de inflamación o de necrosis, siendo la mayoría de ellos los de células B de grado alto o los de tipo Burkitt 17-22.
Por otro lado, el sarcoma de Kaposi (SK) cardíaco en estadio SIDA, tiene una prevalencia entre 12 a 28% en necropsias de la era anterior al uso de antiretrovirales, y asociados a un compromiso visceral sistémico 2,17,18. Las lesiones son menores de 1 cm de diámetro, pueden ser pericárdicas o miocárdicas y, en casos muy raros, pueden generar obstrucciones al tracto de salida sanguíneo, disfunción miocárdica, y morbimortalidad elevadas (2, 20-22).
La introducción de la terapia antiretroviral ha reducido de manera importante la incidencia del compromiso cardíaco por estas neoplasias, probablemente por la mejoría del estado inmunológico o por la supresión de las infecciones por agentes oportunistas como el virus herpes tipo 8 y el virus Epstein Barr 20-22.
1.2. Compromiso endocárdico
1.2.1. Endocarditis infecciosa
La prevalencia de endocarditis infecciosa es similar a otros grupos de pacientes como por ejemplo a los usuarios de drogas endovenosas. Sin embargo, los individuos con recuentos celulares de CD4 menores a 50 células /mm3 y altas cargas virales (> 100,000 copias /ml), tienen un riesgo cuatro veces mayor para desarrollar esta condición 17-21.
En los países desarrollados, un factor de riesgo importante es el uso de drogas endovenosas con endocarditis del lado derecho del corazón, mientras que los pacientes que viven en países en vías de desarrollo, presentan como factor de riesgo el antecedente de enfermedad cardíaca reumática 23.
Los datos clínicos dependen del tipo y la localización del compromiso valvular. El germen más común es el Staphylococcus aureus, principalmente sensible a la meticilina. Por otro lado, se ha descrito que la tasa de hemocultivos negativos varía de 3.7% a 54%, especulándose que este hallazgo estaría asociado con el empleo de cotrimoxazol u otros antibióticos usados en la profilaxis de infecciones 17,23.
El pronóstico de esta condición es similar a la de los pacientes sin infección. Sin embargo, los pacientes con mayores grados de inmunosupresión (menores recuentos de linfocitos CD4), y aquellos que tienen un compromiso valvular izquierdo o mixto, tienen una mayor mortalidad 17,23.
El manejo médico y quirúrgico debe ser guiado por los hallazgos bacteriológicos y el estado clínico de los pacientes, siguiendo las recomendaciones de las guías 23.
1.2.2. Endocarditis trombótica no bacteriana
Los pacientes en estadío SIDA pueden presentar otra forma de endocarditis llamada marántica: trombótica, no bacteriana, la cual está presente entre el 3 y 5% de este subgrupo de pacientes, predominantemente con síndrome de consumo. Estas vegetaciones son friables, de tamaño menor a 0.5 cm y afectan más el lado izquierdo del corazón, a pesar de esto la embolización sistémica es poco frecuente 17-22.
1.3. Compromiso pericárdico
El compromiso pericárdico es otra de las formas de compromiso cardiovascular en la infección por el VIH, incluyendo una gran variedad de manifestaciones clínicas desde el derrame pericárdico asintomático, pericarditis, taponamiento cardíaco y pericarditis constrictiva 17,24.
Antes de la terapia antiretroviral, la prevalencia de derrame pericárdico oscilaba entre 11 hasta 40%. En la cohorte del estudio realizado en Soweto, Sud Africa, entre los años 2006 y 2008, los derrames pericárdicos y pericardtis fueron la segunda manifestación cardíaca más común (25%). Sin embargo, en países desarrollados, la prevalencia es baja 17,24.
1.3.1. Derrame pericárdico
El derrame pericárdico podría servir como una señal de un estado inmune reducido, probablemente por la presencia de infecciones oportunistas como infecciones bacterianas (por ejemplo Tuberculosis, especialmente en países con alta prevalencia de esta enfermedad), por Citomegalovirus, Nocardia, Cryptococcus, o neoplasias malignas como linfomas o Sarcoma de Kaposi. También se ha sugerido asociación con hipoalbuminemia, por activación de citoquinas generando “un síndrome de fuga capilar”, o por la invasión directa del pericardio o miocardio. Por otro lado, en un 8% de los casos no se identifica una causa específica 17,23,24.
Con pequeños derrames pericárdicos, los pacientes pueden presentarse sin síntomas. Con grandes derrames pericárdicos, los pacientes pueden presentar disnea, agrandamiento de la silueta cardíaca en la radiografía de tórax, cambios electrocardiográficos e inestabilidad hemodinámica en el caso del taponamiento cardíaco 23,24.
El proceso diagnóstico deberá considerar la epidemiología de la región y la presentación clínica. La pericardiocentesis con el análisis del fluído pericárdico, incluyendo citología, bioquímica, y cultivos para bacterias (especialmente para Tuberculosis) puede ser útil. A ello se suma la pericardioscopía y el estudio anátomo-patológico, incluyendo estudios de biología molecular 23,24.
El diagnóstico de derrame pericárdico se asocia a una reducida supervivencia. En personas con infección por VIH en estadío SIDA, la mortalidad a 6 meses fue 9 veces mayor que aquellos que no presentaban derrame pericárdico 23,24.
El tratamiento es dependiente de la severidad y de la etiología. Los derrames pequeños no requieren tratamiento pero sí seguimiento. En pacientes con inestabilidad hemodinámica y características de taponamiento cardíaco, la pericardiocentesis de emergencia está indicada. Se ha estudiado el efecto combinado de la prednisolona oral y Mycobacterium indicus pranii, no encontrándose una asociación con una menor mortalidad. En este estudio, se encontró que la prednisolona oral, se asoció con un riesgo reducido de pericarditis constrictiva, pero con un riesgo 3 veces mayor de cáncer 24.
2. Compromiso vascular extracardíaco
2.1. Compromiso aterosclerótico vascular
2.1.1. Desórdenes cerebrovasculares
La epidemiología del compromiso cerebrovascular puede estar alterada considerando la mayor supervivencia de los pacientes, el incremento de los factores de riesgo cardiovasculares, el uso extensivo de la terapia antiretroviral y la disminución de las infecciones por gérmenes oportunistas 25.
Si bien es cierto, en la época anterior a la terapia antiretroviral, las personas afectadas por esta condición eran jóvenes quienes se encontraban en estadío SIDA (16,19,20, estudios actuales han demostrado una mayor incidencia del riesgo de enfermedad vascular cerebral en la población infectada, en comparación con los no infectados. Según el estudio de Rasmussen L y colaboradores, desarrollado en Dinamarca, la tasa de incidencia es de 1.6 (IC 95% de 1.32-1.94), y el meta-análisis de Gutiérrez J, encontró intervalos de Hazard ratio de 1.53-2.16 25.
Al parecer, existiría un mayor predominio en mujeres de edad no avanzada, en comparación con varones, y sobre todo en personas que viven en países de bajos recursos económicos. Se describen como factores de riesgo: estadíos avanzados de inmunosupresión, uso de inhibidores de proteasa (se ha identificado al darunavir), y los factores de riesgo tradicionales (hipertensión, diabetes, dislipidemia, tabaquismo, fibrilación auricular, edad). Un apunte importante es considerar la presencia de infecciones por agentes oportunistas como meningitis tuberculosa, neurosífilis, vasculitis por el virus de Varicela-Zoster, o incluso lesiones que ocupan espacio como toxoplasmosis del sistema nervioso central, tuberculomas o abscesos cerebrales (16,19,20,25.
La presentación clínica sería el comienzo súbito de un déficit neurológico focal, aún cuando pueden presentarse síntomas de alteración del estado mental, pérdida aguda de conciencia, fiebre, comienzo subagudo de los síntomas en horas o días, o inclusive presentaciones subclínicas. Los infartos cerebrales son más frecuentes que las hemorragias (algunas series refieren proporciones de 90 a 95% de casos para infartos cerebrales y de 5 a 10% de hemorragias cerebrales) (25 -27).
Cuando se sospecha de cardioembolismo, debemos recordar que estos pacientes tienen un riesgo incrementado para hacer fibrilación auricular, y que pueden desarrollar cardiomiopatía en el contexto de una infección no controlada, o pueden tener enfermedad valvular, incluso con enfermedad infecciosa agregada. El manejo es similar que el de la población general, con buenas respuestas con el empleo del activador de plasminógeno tisular (tPA), y el control de los factores de riesgo en prevención secundaria 25.
2.2. Compromiso tromboembólico
2.2.1. Trombosis venosa profunda
La enfermedad tromboembólica venosa puede presentarse como una trombosis venosa profunda o embolismo pulmonar. Los trombos venosos son consecuencia del estrés de rozamiento y son ricos en fibrina y células rojas, con bajos niveles de plaquetas. La triada de Virchow incluye tres factores presentes en este grupo de pacientes como: hipercoagulabilidad sanguínea, disfunción de las células endoteliales y éstasis sanguíneo 22.
En la población general, la enfermedad tromboembólica venosa, ocurrió con una frecuencia anual de 1 a 2 eventos por 100,000 personas-año (0.1%-0.2%), que se incrementa con la edad. La incidencia varía dependiendo de la población de estudio (0.19%-7.63%) (16,22.
Las causas de este síndrome son complejas, y pueden estar relacionadas con desórdenes de la coagulación, como incremento de los niveles de fibrinógeno, IL-6, PCR, dímero D, inhibidor del plasminógeno tisular tipo 1, antígeno activador del plasminógeno, o una deficiencia de proteína S16-21.
2.3. Enfermedad arterial periférica
La prevalencia de enfermedad arterial periférica en pacientes con infección por VIH oscila entre un 2 a 27%, dependiendo de la técnica empleada para su diagnóstico, predominantemente a través del índice tobillo brazo, considerando diferentes puntos de corte, inclusive después del ejercicio físico. Las variables asociadas en algunos estudios son: género masculino, dislipidemia, edad avanzada, tabaquismo, recuento de CD4 menor a 200 copias/mL, o enfermedad activa 28.
2.4. Arritmias
Los pacientes con infección por el VIH pueden presentar fibrilación auricular, la cual se asociaría a una mayor frecuencia de eventos cardiovasculares. También es frecuente la presentación de disfunción autonómica con reducción de la variabilidad cardíaca, asociada a un predominio simpático, en relación con la progresión de la infección (29.
Por otro lado, la muerte súbita cardíaca es la tercera causa de muerte en la población con VIH, siendo 4.5 veces más frecuente que en la población general. Los pacientes pueden presentar también síndrome de QT prolongado y torcida de puntas, asociadas a disturbios hidroelectrolíticos o al empleo de algunos medicamentos antiretrovirales (mejor descritos los inhibidores de proteasa como atazanavir, lopinavir y saquinavir), o sus interacciones con otros fármacos como macrólidos, pentamidina, antifúngicos, fluoroquinolonas o metadona 29.
3. Medicación antiretroviral y riesgo cardiovascular
Algunos antiretrovirales y clases de antiretrovirales se han asociado con un incremento del riesgo cardiovascular. (Tabla 3)
Tabla 3 Efectos adversos más frecuentes de los medicamentos antirretrovirales
| Fármacos | Eventos adversos |
|---|---|
| Inhibidores nucleósidos de la transcriptasa reversa | |
| Abacavir Didanosina Emtricitabina Lamivudina Estavudina Tenofovir Zidovudina | -Potencial incremento de eventos cardiovasculares -Hipertensión, infarto de miocardio -Hipertrigliceridemia -Posible cardiotoxicidad en fetos -Redistribución de grasas, dislipidemia -Reducción modesta en colesterol total y LDL -Potencial disfunción mitocondrial / miopatía |
| Inhibidores no nucleósidos de la transcriptasa reversa | |
| Delavirdina Efavirenz Etravirina Nevirapina | -Interacciones farmacológicas con bloqueadores de calcio, warfarina, betabloqueadores, quinidina, corticoesteroides, teofilina -Arritmias fatales -Dislipidemia, dislipidemia aterogénica -Hipertensión |
| Inhibidores de proteasa | |
| Amprenavir Atazanavir Darunabir Fosamprenavir Indinavir Lopinavir/ritonavir Nelfinavir Ritonavir Saquinavir Tipranavir | Hipercolesterolemia, hipertrigliceridemia Hipotensión Bloqueo aurículoventricular Prolongación del intervalo QT Incremento del riesgo de infarto de miocardio |
| Inhibidores de integrasa | |
| Raltegravir Elvitegravir Dolutegravir Bictegravir | Incremento de peso, predominantemente dolutegravir y bictegravir (hasta 6 kg en 4 años de seguimiento) Efecto neutral sobre los lípidos |
| Inhibidores de entrada y de fusión | |
| Enfuvirtida Maraviroc | Casos esporádicos de hipotensión postural, angina, insuficiencia cardíaca, infarto de miocardio |
Construido con datos de 2,35-37
Aún no puede determinarse si el inicio inmediato de la terapia antiretroviral reduce el riesgo cardiovascular. Sin embargo, se tienen datos del estudio DAD (Data Collection on Adverse Events of Anti-HIV Drugs), en el que se encontró que cada año acumulado de uso de inhibidores de proteasa se asoció a un incremento de 10% de infarto de miocardio, a pesar de ajustarse por valores del colesterol16,30.
También se ha reportado que el darunavir (pero no el atazanavir), potenciado con ritonavir-todos ellos pertenecientes a la clase de inhibidores de proteasa, se asoció con un riesgo cardiovascular incrementado y con un grosor carotídeo íntima-media alterado. De la clase terapéutica de los inhibidores de transcriptasa reversa, el empleo de abacavir se ha asociado a un mayor número de eventos cardiovasculares16,31,32.
La evaluación del riesgo cardiovascular en la población de pacientes con infección por el VIH está recomendada, considerándose los factores de riesgo tradicionales: edad, diabetes mellitus, tabaquismo, hipertensión, dislipidemia, y el efecto de la infección por sí misma, así como el de la medicación. Se puede usar cualquier escala como en la población general (US-based cohort equations, PCE; Framingham Risk Score; Europe-based SCORE; o la específica para esta población, D:A:D, basada en el estudio Data Collection on Adverse Events of Anti-HIV Drugs, con la consideración de que todas ellas tienden a subestimar el riesgo cardiovascular en esta población33,34.
Recientemente se ha desarrollado una segunda escala validada para la población de los pacientes con VIH, empleando el análisis de una cohorte retrospectiva de 1,914 pacientes entre Marzo del 2012 y Enero del 2017. Esta escala incluye las siguientes variables: género, etnicidad, edad cronológica, edad en que se hizo el diagnóstico de infección, pico de carga viral, recuento más bajo de linfocitos CD4, hipertensión, hiperlipidemia, diabetes, enfermedad renal crónica y tabaquismo. Con estas once variables, el modelo de regresión logística tuvo un área bajo la curva de 0.957 (IC 0.938-0.975), para la predicción de eventos cardiovasculares a 10 años 35.
Una enorme oportunidad es la educación médica, para quienes atienden a pacientes con infección por VIH, quienes sólo reconocen a algunos antiretrovirales como posibles causas de un mayor riesgo cardiovascular, e identifican sólo algunos factores de riesgo cardiovascular. Adicionalmente evalúan el riesgo cardiovascular de sus pacientes “siempre” en un 7% y “algunas veces” en el 21%. También evalúan de manera inapropiada los factores de riesgo cardiovasculares, pues la medición de lípidos en sangre es muy esporádica: una vez al año (39%), dos veces al año (46%), tres veces al año (7%), cuatro veces al año (4%) y nunca (4%) 36.
En el Perú, se conoce la prevalencia de algunos factores de riesgo cardiovasculares en esta población, siendo el reporte más reciente la evaluación de 305 pacientes, quienes recibían terapia antiretroviral por más de 6 meses, en cinco hospitales de Lima y Callao. Se encontró dislipidemia en el 51.5%, sobrepeso en 41.6%, obesidad en 11.1%, Diabetes Mellitus en 7.2%, hipertensión en 8.9%. Los médicos tratantes prescribían tratamiento farmacológico en el 91.3% de pacientes con diabetes e hipertensión, pero sólo al 29.3% de pacientes con dislipidemia 37.
A la fecha, se cuentan con pocas estrategias efectivas para prevenir la enfermedad cardiovascular en los pacientes con infección por VIH, pero parecería que la terapia con estatinas sería efectiva, quedando pendiente la publicación oficial de los resultados del estudio REPRIEVE. También se ha estudiado la modulación del proceso inflamatorio empleando metrotexate y colchicina, pero sin mejoría en la función endotelial, y el anticuerpo monoclonal canakinumab con disminución de los marcadores sistémicos de inflamación e inflamación aórtica, medidos a través de tomografías de emisión de positrones. Por otro lado, se cuenta con los datos positivos de evolocumab, un inhibidor de PCSK9, el cual mejoró la función endotelial coronaria en solo 6 semanas de tratamiento, existiendo más de 70 estudios clínicos en marcha, enfocados en la prevención y el tratamiento de la enfermedad cardiovascular en esta población de riesgo 38.