Introducción
La cardiomiopatía hipertrófica (CMH) es una afección primaria del músculo cardiaco la cual consiste en un aumento del grosor de la pared del ventrículo izquierdo ≥15 mm en cualquier segmento miocárdico que no se explica únicamente por condiciones de sobrecarga 1. La CMH puede presentarse con diferentes espectros clínicos, entre ellos la obstrucción del tracto de salida del ventrículo izquierdo (OTSVI) 2. Comúnmente, involucra al septum en la porción basal; pueden encontrarse diferentes fenotipos, entre ellos la variante apical que varía en frecuencia dependiendo de la población estudiada, se ha documentado desde un 3 a 11% de las CMH en Estados Unidos. Es más frecuente en hombres que en mujeres 3, con una proporción de casos con diagnóstico genético y transmisión mendeliana que puede ser positivo hasta en hasta un 60% de los pacientes 4, y se encuentra principalmente en individuos con variantes sarcoméricas o sarcoméricas negativas que generan diferentes espectros de presentación clínica 5.
La variante de la filamina C (FLNC) es poco frecuente en la CMH y se ha asociado a presentaciones sindrómicas y elevado riesgo de muerte súbita, es más frecuente esta variante en la cardiomiopatía restrictiva y no dilatada 1. Por tal motivo, se presenta el siguiente caso de un paciente con diagnóstico de CMH variante septal asimétrica con importante gradiente intracavitario y variante de la FLNC en quién se realizó un abordaje quirúrgico transapical con mejoría posterior de su sintomatología.
Reporte de caso
Paciente de sexo masculino de 23 años, natural de Itagüí - Colombia, antecedente familiar de muerte súbita de etiología no clara en abuelo a los 50 años, sin otros antecedentes familiares o personales de importancia. Venía en seguimiento externo por episodios sincopales a repetición con diagnóstico desde la infancia de disfunción del nodo sinusal sintomática por lo que se le implantó un marcapaso.
Durante controles posteriores no hay reporte de deterioro de clase funcional hasta el año 2012 en Guayaquil-Ecuador. Durante su hospitalización se realiza el cambio de generador; en el primer mes postoperatorio presenta como complicación temprana una infección de bolsillo de marcapaso por lo que requirió el explante de la unidad generadora con posterior abandono de electrodo ventricular previamente implantado. Se realiza un nuevo implante de marcapaso en el lado contralateral sin complicaciones ni registro de nuevos eventos sincopales en los siguientes 10 años de seguimiento.
Seis meses antes del ingreso presentaba deterioro de clase funcional NYHA III, sin otros síntomas y sin reportes de evaluaciones por servicio de electrofisiología desde el último implante de generador de marcapaso en 2012. Durante controles ambulatorios se reportó la suspensión del tratamiento con beta bloqueador debido a la pobre tolerancia.
Al examen físico se encontró soplo sistólico en foco aórtico II/VI sin irradiación, no presentó signos de congestión central o periférica. Dentro de los laboratorios no se evidenció alteración en función renal, electrolítica ni del perfil hematológico. Se programó el marcapaso con evidencia de agotamiento de la batería de generador. Se realizó un ecocardiograma transtorácico donde se encontró hipertrofia concéntrica severa del septum interventricular a nivel medio ventricular, de 26 mm con gradiente intracavitario pico de 117 mmHg (Figura 1) y movimiento sistólico anterior del velo mitral (SAM) el cual generaba una regurgitación mitral leve.
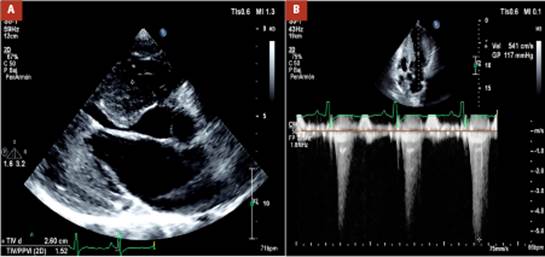
Figura 1 (A) Ecocardiograma transtorácico proyección paraesternal eje largo con documentación de septum de 2,6 cm y documentación de engrosamiento medioventricular. (B) Doppler continuo en TSVI con gradiente intracavitario pico de 117 mmHg.
Fue evaluado por Heart Team, debido al score de riesgo de muerte súbita (16,8%) además de tener antecedentes familiares de muerte súbita considerando EUROSCORE II 0,67%; en cuanto a los electrodos abandonados previamente y la contraindicación de realización de resonancia magnética cardiaca, dado a la incompatibilidad del marcapaso, se realiza un estudio tomográfico y se consideró la realización de miectomía por sintomatología y variante documentada.
Fue programado para realización de miectomía medio ventricular por abordaje transapical con retiro de electrodos; se realizó la ventriculotomía izquierda en el ápex, con posterior resección del septum desde el parte medio ventricular hasta la base, con posterior retiro de electrodos adheridos a velo septal tricúspideo. No hubo complicaciones intraoperatorias y posteriormente se presentó disminución del gradiente intracavitario sin presencia del fenómeno SAM (Figura 2). Durante su estancia en Unidad de Cuidados Intensivos el paciente cursó con dos episodios documentados de taquicardia ventricular con inestabilidad hemodinámica por lo cual se le colocó un cardiodesfibrilador implantable (CDI) compatible con resonancia magnética (MRI) ST Jude sin presentar nuevos episodios de TV. El paciente cursó sin nuevas intercurrencias y se iniciaron los estudios ambulatorios de estudio genético debido a sus antecedente familiares.
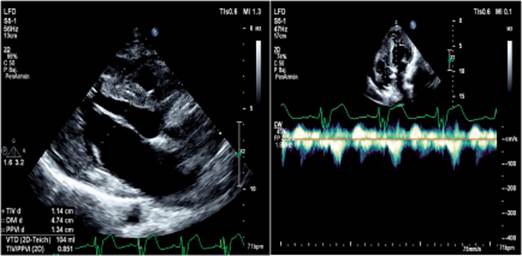
Figura 2 (A) Proyección paraesternal eje largo con documentación de septum de 1,1 cm. (B) Doppler continuo en TSVI sin evidencia de gradiente intracavitario.
El paciente presentó una evolución posoperatoria favorable luego del implante de CDI. En los estudios genéticos se encontró una variante, probablemente patogénica, en heterocigosis del FLNC, c 4636G>A consistente con miocardiopatía familiar hipertrófica tipo 26 autosómica dominante.
Actualmente, el paciente se encuentra en clase funcional I, sin arritmias evidenciadas en la telemetría y en tratamiento regular con Bisoprolol 5 mg. Se inició ampliación de estudio genético a familiares directos, sin embargo, debido al difícil acceso a servicios de salud su ejecución fue limitada.
Discusión
La CMH es una de las cardiomiopatías más frecuentes a nivel mundial, se estima una prevalencia de 0,2%1. La mayoría de los casos de CMH se asocian con ocho variantes sarcoméricas establecidas; esto conlleva a una alteración en la codificación de proteínas implicadas en la homeostasis del calcio o genes que codifican para proteínas del disco Z, como la FLNC, se presentan con menor frecuencia en la CMH 6.
La FLNC es una proteína dimérica de gran tamaño que se une a la actina y se localiza en las premiofibrillas, los discos Z y discos intercalados donde interviene en la estabilización mecánica y la señalización intracelular de los miocitos 6,7. Variantes de la FLNC se han asociado más con el desarrollo de cardiomiopatías restrictivas y arritmogénicas. Sin embargo, mutaciones en esta proteína pueden alterar la estructura del sarcómero generando una organización alterada de las miofibrillas. Esta alteración estructural genera agregados proteicos que conducen finalmente a la desorganización sarcomérica y al probable desarrollo de CMH 8. Las mutaciones no sarcoméricas, como la FLNC, se han asociado más al desarrollo de hipertrofia septal basal aislada, con menor realce tardío de gadolinio, pero más OTSVI5, como lo presentó en el paciente del caso actual.
Es de vital importancia el hallazgo genético implicado debido a la estrecha relación entre la FLNC y muerte súbita, los cuales han sido estudiados en pacientes con miocardiopatía dilatada, arritmogénica e hipertrófica. Esta variante se asocia a una prevalencia de falla cardiaca avanzada a los 5 años, y desarrollo de arritmias ventriculares entre el 22 al 27%, siendo el primer caso reportado en Colombia.
Respecto a la miectomía, la técnica septal transaórtica extendida es la mejor opción de tratamiento para los pacientes con OTSVI cuyos síntomas son refractarios al tratamiento médico. Por otra parte, este abordaje es útil para pacientes con obstrucción subaórtica 9. Para los pacientes con compromiso obstructivo medio ventricular (OMV) como causa subyacente del gradiente residual es eficaz un abordaje transapical 10. En una cohorte de 115 pacientes llevados a esta técnica entre 1993 y 2012, de los cuales 55 pacientes tenían un fenotipo OMV (n=55), en su totalidad presentaron disminución del gradiente y sin complicaciones posteriores como defectos ventriculares septales, pseudoaneurisma del VI o arritmias ventriculares, siendo el abordaje transapical seguro y eficaz para el alivio de la OMV, con resultados hemodinámicos similares al abordaje transaórtico 11,12. Este mismo abordaje fue realizado en nuestro paciente, con posterior éxito clínico, disminución del gradiente y mejoría de la sintomatología clínica.
En conclusión, la variante de la FLNC se ha asociado en gran medida a cardiomiopatías restrictivas y no dilatadas, con presentación poco frecuente en pacientes con CMH. Es crucial el estudio genético en el diagnóstico y pronóstico de estos pacientes debido al elevado riesgo de muerte súbita en poblaciones con variante de FLNC, donde esta última es de vital importancia para guiar nuestra actitud terapéutica por la progresión de enfermedad y requerimientos de dispositivos avanzados. No hay casos reportados en nuestro medio acerca de la miectomía con abordaje transapical en estos pacientes; sin embargo, es una alternativa más a estos pacientes con OMV, con una importante mejoría y seguridad en los resultados clínicos del paciente.















