Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Peruana de Medicina Experimental y Salud Publica
versión impresa ISSN 1726-4634
Rev. perú. med. exp. salud publica v.16 n.1-2 Lima 1999
ARTÍCULOS ORIGINALES
Evaluación de la Intradermorreacción con Antígenos de Leishmania (Viannia) peruviana y Leishmania (Viannia) braziliensis en Áreas endémicas de Leishmaniasis en el Perú
Minaya G1; Torres Y2; Farfán M1; Mendizabal L1; Colchado M3; Arroyo E3.
1 División de Parasitología, Centro Nacional de Laboratorios en Salud Pública, Instituto Nacional de Salud.
2 División de Virología, Centro Nacional de Laboratorios en Salud Pública, Instituto Nacional de Salud.
3 Centro de Salud Pucará, Sub-Región Jaén.
RESUMEN
Se elaboró extractos de antígenos solubles de Leishmania (leishmanina), a partir de formas promastigotes de Leishmania (Viannia) peruviana y Leishmania (Viannia) braziliensis. Los antígenos fueron evaluados respecto a su sensibilidad, especificidad y efectos colaterales. Los ensayos se llevaron a cabo en una área de transmisión de la uta (leishmaniasis andina), en un área de transmisión de la espundia(leishmaniasis selvática), y en pacientes atendidos en Lima. El antígeno de Leishmania (Viannia) peruviana, 25 µg/ml, resultó adecuado para la detección de la reacción de hipersensibilidad cutánea tardía en pacientes con lesiones cutáneas y/o cutáneo-mucosas activas, encontrando una sensibilidad promedio de 95,9%. La misma sensibilidad, pero con reacciones más intensas (potentes) fue observada con el antígeno homólogo de 30 µg/ml. Los antígenos de Leishmania (Viannia) braziliensis de 25 y 30 µg/ml mostraron similar sensibilidad y potencia a las dosis equivalentes de Leishmania (Viannia) peruviana.La sensibilidad y la potencia de la reacción se incrementaron mínimamente con el incremento en la concentración de proteínas. No se observaron efectos colaterales como vesiculación y ulceración en el sitio de inoculación. Los antígenos demostraron ser altamente específicos. La especificidad en el grupo control alcanzó el 100,0%, mientras que en el grupo control endémico fue 95,7%.
Palabras clave: Leishmaniasis, Leishmania, antígeno, Perú.
ABSTRACT
Extracts of Leishmania soluble antigens (leishmanina) were made from Leishmania (Viannia) peruviana and Leishmania (Viannia) braziliensis promastigotes.Antigens were evaluated for sensitivity, specificity and side effects. Assays were perfomed in transmission areas for uta (andean leishmaniasis), espundia (sylvatic leishmaniasis), and also in patients seen in Lima. Leishmania (Viannia) peruviana antigen, 25 µg/ml, was adequate to detect late skin hypersensitivity reaction among patients with active cutaneous and/or mucocutaneous lesions, with an average sensitivity of 95,9%. The same sensitivity, but with more intense (potency) reactions were observed with the homologous 30 µg/ml antigen. Antigens of Leishmania (Viannia) braziliensis, 25 and 30 µg/ml, showed similar sensitivity and potency to the equivalent doses of Leishmania (Viannia) peruviana. The reactions sensitivity and potency increase minimally with increased protein concentration. No side effects, such as vesiculation and ulceration on the site of the innoculation, were observed. Antigens showed high specificity. Specificity in the control group reached 100,0% whereas in the endemic control group, it was 95,7%.
Key words: Leishmaniasis, Leishmania, antigen, Peru.
INTRODUCCIÓN
La prueba intradérmica (IDR) de Montenegro, que mide la reacción de hipersensibilidad cutánea (RHC) de tipo retardada a antígenos homólogos o heterólogos de promastigotes de Leishmania, es una prueba útil en el estudio clínico y epidemiológico de la leishmaniasis tegumentaria de las Américas1-4.
Desde que Montenegro5, en 1926, empleara por primera vez la IDR en el diagnóstico de la leishmaniasis cutáneo-mucosa (LCM), diversos autores han encontrado altos índices de positividad en personas con leishmaniasis cutánea (LC), leishmaniasis cutáneo-mucosa (LCM) y leishmaniasis visceral (LV)4,6-11. Hay datos para considerar que la IDR es altamente específica. Se ha obtenido reacciones negativas en pacientes con paludismo, tuberculosis pulmonar, lepra, blastomicosis, así como en diversas dermatosis4,11,13. Aún cuando regionalmente no se disponga de antígenos estandarizados, la sensibilidad y especificidad de antígenos elaborados en algunos laboratorios es utilizada como prueba auxiliar en el diagnóstico clínico de las leishmaniasis cutánea13,14. En áreas endémicas de Ecuador2, se evaluó la prueba cutánea frente a la prueba de ELISA, reportando una sensibilidad del 82,4% y recomendándola como herramienta diagnóstica para las leishmaniasis cutáneo-mucosas. En 1991, los mismos autores concluyen que el extracto crudo soluble de L. braziliensis panamensis, a una concentración de 10 µg/mL es altamente sensible, 100% en pacientes con LC de 3-6 meses de evolución8.
Sin embargo, la IDR no puede distinguir infecciones actuales de infecciones leishmaniásticas previas, una característica muy común en áreas donde la prevalencia de leishmaniasis es alta15. Con la finalidad de reforzar el conocimiento derivado de los estudios transversales de las leishmaniasis, se han llevado a cabo estudios longitudinales, los que permitieron una mejor comprensión de la historia natural de la enfermedad y sus factores de riesgo16,17. Similar a estudios longitudinales efectuados en la tuberculosis empleando el PPD12, la conversión de no reactivos a reactivos a la leishmanina, en estudios prospectivos, podría ser utilizado como un marcador de infecciones recientemente adquiridas.
La ausencia de un antígeno (leishmanina) estandarizado apropiadamente4 limita la utilidad epidemiológica de esta prueba. Adicionalmente, interrogantes sobre la sensibilidad y especificidad de la IDR, así como la duración de la RHC a la leishmanina, dificultan la interpretación de la prueba en el estudio de las diferentes formas clínicas de las leishmaniasis.
Resultados de estudios longitudinales no sustentan el concepto generalizado de que la respuesta RHC a la leishmaniasis tegumentaria sea permanente16, 17.
En el Perú, se ha llevado a cabo algunos estudios epidemiológicos de tipo transversal empleando la IDR con leishmanina; en ellos, factores de riesgo tales como edad, sexo, ocupación y tiempo de residencia han sido asociados a la reactividad a la leishmanina6,7,19-21, sin embargo no se dan mayores referencias sobre las características del antígeno empleado.
Con el objetivo de disponer de un antígeno de Leishmania para la IDR, aplicable al diagnóstico de las leishmaniasis en el Perú, se evaluó desde el punto de vista de su sensibilidad, especificidad y efectos colaterales diferentes antígenos (leishmanina) utilizando cepas de Leishmania (V.) peruviana y L.(V.) braziliensis, especies consideradas responsables de las dos formas clínicas de mayor importancia en la salud pública de nuestro país.
MATERIALES Y MÉTODOS DE ESTUDIO
PREPARACIÓN DE LA LEISHMANINA
La leishmanina, extracto soluble del parásito, fue preparada siguiendo la metodología de Reed y col10. Se utilizó formas promastigotes de las cepas L. (V.) peruviana MHOM/PE/84/LC 26 y L. (V.) braziliensis MHOM/PE/84/LC 53, identificadas por análisis de zimodemas e hibridación del kDNA, procedentes del Instituto de Medicina Tropical Alexander von Humboldt-Universidad Peruana Cayetano Heredia.
Los promastigotes fueron cultivados en forma sucesiva en los medios de agar sangre bifásico suplementado con 15% de sangre desfibrinada de conejo (USAMRU) y el medio líquido LIT suplementado con 10% de suero fetal bovino, cosechados en la fase logarítmica de crecimiento, centrifugados a 3 500 rpm por 15 minutos a 4°C y lavados 3 veces con solución salina 0,89 %. Subsecuentemente, se lisaron por ultrasonido (tres ciclos de 1 minuto a 25,000 Kc/s en baño de hielo). El lisado, diluido en solución salina, fue centrifugado a 10 000 rpm por 30 minutos a 4°C.
El sobrenadante obtenido, solución antigénica, fue esterilizada mediante filtros Millipore de 0,22 µm y almacenados a –80°C hasta su uso. Previamente, se separó una alícuota de esta solución, para la medición de proteínas por el método de Lowry. La concentración final de proteínas fue ajustada en lotes a 25 y 30 µg/mL, adicionando 0,5 % de fenol como conservador.
Se elaboró los siguientes tipos de leishmanina:
- antígeno de L. (V.) peruviana, 25 ug/mL
- antígeno de L. (V.) peruviana, 30 ug/mL
- antígeno de L. (V.) braziliensis, 25 ug/mL
- antígeno de L. (V.) braziliensis, 30 ug/mL
Tres lotes de leishmanina fueron preparados en fechas diferentes y almacenados en refrigeración, previos al trabajo de campo.
Para garantizar la esterilidad e inocuidad del antígeno, se realizó el estudio microbiológico en placas de agar sangre y saboraud, e incubados a 37°C por 30 días.
EVALUACIÓN DE LAS LEISHMANINAS
Para el enrolamiento de las personas que conformaron el grupo de estudio, se tomaron en cuenta las siguientes consideraciones:
Para el estudio de sensibilidad:
Criterios de inclusión:
- personas portadoras de lesiones activas y/o cicatriciales de etiología leishmaniásica confirmada por demostración del parásito mediante las técnicas de frotis y/o cultivo.
- personas portadoras de lesiones activas y/o cicatriciales adquiridas en áreas endémicas de transmisión, compatibles con etiología leishmaniásica, demostrables por la detección de inmunoglobulinas antileishmania mediante la prueba de Inmunofluorescencia Indirecta (IFI).
Para el estudio de especificidad:
Criterios de inclusión:
- residentes de la ciudad de Lima, área no endémica, sin antecedentes clínicos, ni de visita a zonas de transmisión de leishmaniasis.
- residentes de áreas endémicas sin antecedentes clínicos de leishmaniasis.
- personas portadoras de lesiones activas con diagnóstico clínico de otras patologías.
POBLACIÓN DE ESTUDIO
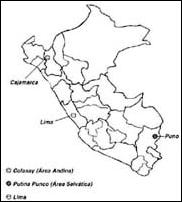
El estudio se llevó a cabo en pobladores de la localidad de Colasay (dpto. Cajamarca), área de transmisión andina, donde L. (V.) peruviana ha sido identificada, así como en residentes de Putina Punco, área selvática del dpto. de Puno, en el cual L. (V.) braziliensis es el agente causal de la enfermedad. Integraron también este grupo los individuos que acudieron al Instituto Nacional de Salud (INS) solicitando el servicio de diagnóstico de leishmaniasis (Figura 1).
Figura 1. Áreas geográficas en las que se realizó la evaluación
de la leishmanina
I. ÁREA DE TRANSMISIÓN CUTÁNEA ANDINA
- Lugar de estudio
La evaluación del antígeno en el área de transmisión de la forma andina se realizó en el caserío de Colasay, distrito del mismo nombre (provincia de Jaén, dpto. Cajamarca) ubicado a 1790 msnm, distante 60 Km de la carretera Panamericana norte.
- Población en estudio
Para el estudio de sensibilidad, el grupo estuvo constituido por 22 pobladores portadores de lesiones activas y/o cicatriciales, quince (68,2%) de ellos fueron confirmados por demostración de amastigotes en frotis coloreados con Giemsa.
Los siete restantes fueron cicatriciales, tres de ellos no acudieron nunca a un centro de salud por el diagnóstico respectivo, y cuatro tenían antecedentes de un examen anterior de frotis con resultado negativo; sin embargo, integrantes de su familia tenían o habían tenido leishmaniasis confirmada; cinco respondieron al tratamiento con glucantime y dos aparentemente curaron con métodos caseros.
Para el estudio de especificidad, el grupo control endémico estuvo conformado por siete residentes sin antecedentes clínicos de leishmaniasis.
La presencia de dos individuos portadores de lesiones, diagnosticados clínicamente como poco compatibles con etiología leishmaniásica, permitió investigar reacciones cruzadas con otras patologías.
II. ÁREA DE TRANSMISIÓN SELVÁTICA
- Lugar de estudio
Para la evaluación de la leishmanina en área de transmisión selvática, se eligió la localidad de San Juan del Oro (Putina Punco), situada en la provincia de Sandia, dpto. de Puno. Comprende áreas boscosas de la vertiente oriental de los Andes y es de relieve accidentado; el clima es tropical húmedo, típico de selva alta.
- Población en estudio
La población estuvo constituida por comunidades nativas y mestizas asentadas en las márgenes del río Putina; los pobladores se dedican a labores agrícolas, principalmente cultivos de panllevar, frutales y actividades extractivas temporales, especialmente madera y oro, razón por la cual muchos se trasladan al dpto. de Madre de Dios.
Se realizó la prueba de IDR a 42 personas con lesiones activas y/o cicatriciales sospechosas de patología leishmaniásica y a 16 residentes sin antecedentes clínicos de leishmaniasis.
Con la finalidad de investigar la existencia de reacción cruzada con infecciones micóticas, se incluyó a dos niños con lesiones dérmicas diagnosticadas clínicamente como micosis, en el centro de salud de Putina Punco.
Además de considerar los criterios clínico- epidemiológicos, se comparó los resultados de la reacción de hipersensibilidad tardía con los obtenidos en la prueba de IFI, la cual es altamente sensible y específica en el diagnóstico de las leishmaniasis.
III. PACIENTES ATENDIDOS EN EL INS (Lima)
De los diecinueve individuos que fueron derivados al INS para descarte de leishmaniasis, 13 de éstos presentaban lesiones cutáneas, mientras que los seis restantes presentaban, además, lesiones mucosas compatibles con etiología leishmaniásica.
PROCEDIMIENTOS
Datos relativos al nombre, edad, sexo, ocupación, procedencia, tiempo de residencia en la localidad, número, descripción y tiempo de evolución de las lesiones, etc., de cada participante, fueron consignados en una ficha clínico epidemiológica.
Muestras de tejido y exudado para la investigación parasitológica, mediante las técnicas de frotis y cultivo, fueron obtenidas de todas las personas que presentaron lesiones activas compatibles con leishmaniasis. Previa información de los fines del estudio, fue requerido el consentimiento oral en cada caso; de los menores de edad, se requirió autorización de sus padres.
Adicionalmente, a fin de determinar la inmunidad de tipo humoral, se colectó una muestra de sangre por punción venosa; el suero obtenido fue conservado en condiciones de refrigeración hasta su procesamiento mediante la prueba de Inmunofluorescencia Indirecta (IFI). Según estandarización de la técnica en nuestro laboratorio, las muestras de suero, en las cuales se detectó inmunoglobulinas IgG a la dilución mínima de 1/40, fueron consideradas positivas.
El antígeno para la prueba de IFI fue elaborado con promastigotes de L. (V.) braziliensis, siguiendo la metodología de Guimaraes y col 23.
Los antígenos de leishmanina e IFI fueron preparados en el Laboratorio de Leishmaniasis y Chagas de la División de Parasitología del Centro Nacional de Laboratorios en Salud Pública, Instituto Nacional de Salud (INS).
APLICACIÓN DEL ANTÍGENO (PRUEBA DE MONTENEGRO)
Se aplicó vía intraepidérmica, 0,1 mL de la leishmanina preparada, en la cara anterior de los antebrazos (Figura 4) de los siguientes grupos de individuos (Tabla 1):
- 49 individuos con lesiones activas de etiología compatible con leishmaniasis: 30 con lesiones cutáneas y 19 con lesiones cutáneo-mucosas.
- 33 individuos con lesiones cutáneas curadas (cicatricial): 15 de zona andina y 18 de zona selvática.
- 23 residentes de áreas endémicas sin antecedentes clínicos (control negativo endémico).
- 20 residentes de la ciudad de Lima (área no endémica) sin antecedentes clínico epidemiológicos de leishmaniasis (grupo control).
- 8 individuos afectados con otras patologías.
La lectura de la reacción de hipersensibilidad se verificó, según patrón establecido, entre las 48 y 72 horas posteriores a la aplicación24-25.
La prueba fue considerada positiva si el diámetro promedio de induración (pápula) era > 5 mm en el sitio de inoculación (Figura 4). Para ello, tanto el diámetro mayor como su perpendicular fueron medidos y promediados; utilizando un bolígrafo, la pápula fue delimitada y estos bordes transferidos a un papel humedecido en alcohol al 70%, para su registro permanente.
Tabla 1. Grupos Clínicos evaluados

RESULTADOS
ESTERILIDAD E INOCUIDAD
En los tres lotes de leishmanina preparados, no se detectó contaminación bacteriana ni micótica. Asimismo, la ausencia de reacción en ratones inoculados con estos antígenos demostró la inocuidad de los mismos.
SENSIBILIDAD
Para el estudio de sensibilidad, la condición de enfermos de leishmaniasis fue determinada a través de pruebas que permitieron confirmar la naturaleza de la enfermedad, mediante la demostración directa o indirecta del agente etiológico causal, denominadas pruebas o patrón de oro.
Los Patrones de confirmación considerados en el presente estudio fueron:
1. Observación del amastigote de leishmania mediante la técnica del frotis.
2. Aislamiento del promastigote de leishmania mediante la técnica de cultivo.
3. Detección de inmunoglobulinas circulantes antileishmania mediante la técnica de IFI.
La sensibilidad, porcentaje de reacciones positivas en una población de enfermos, fue determinada mediante la aplicación de la leishmanina en personas portadoras de lesiones cutáneas y/o cutáneo-mucosas activas y cicatriciales (grupos 1, 2 y 3).
Grupos 1 y 2. Lesiones activas cutáneas y/o cutáneo-mucosas
Cuarenta y nueve personas, incluyendo los consultantes al INS, con lesiones activas, 30 cutáneas (Figura 2), 19 cutáneo-mucosas (Figura 3), mostraron una sensibilidad promedio de 95,9%. Estos porcentajes son comparables con hallazgos de otros autores en países vecinos 4,5,13.
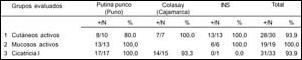
En la tabla 2, se consolida la reactividad mostrada, cuando menos a uno de los antígenos evaluados.
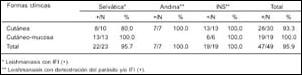
En personas con enfermedad cutánea activa, 28/30 (93,3%) fueron sensibles a la leishmanina. En relación a la reactividad demostrada por pacientes afectados con LCM activa, 19/19 (100,0%) fueron sensibles a todos los antígenos (Tabla 3).
Grupo 3 Cicatricial
La sensibilidad promedio en el grupo cicatricial fue 86,4%. Una niña de 3 años de edad, con diagnóstico parasitológico confirmatorio previo al tratamiento con glucantime, reaccionó a la leishmanina L. (V.) peruviana 30 µg/mL, pero no a su homólogo de 25 µg/mL. Situación similar ocurrió con un niño de 11 años que dio reacción positiva a los antígenos de L. (V) peruviana, 30 µg/mL y L. (V) braziliensis, 25 µg/mL, pero reacciónó negativamente a L. (V) peruviana, 25 µg/mL.
En el grupo evaluado en la localidad de Putina Punco (Puno), área de transmisión selvática de la enfermedad, 17/17 (100,0%) respondieron a los antígenos de L. (V.) braziliensis (Tabla 2).
Los resultados de los conformantes de este grupo, evaluados en la localidad andina de Colasay, indican que 14/15 (93,3%) fueron sensibles a la prueba intradérmica. Un individuo con leishmaniasis curada de procedencia selvática, que acudió al INS para control serológico, no respondió a ningún antígeno (Tabla 4).
ESPECIFICIDAD
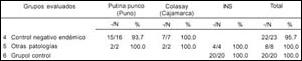
La especificidad, número de reacciones negativas en una población de sanos, fue determinada con los grupos 4, 5 y 6 evaluados (Tabla 5).
Grupo 4. Control negativo endémico
En los residentes de área endémica sin antecedentes clínicos de leishmaniasis, la especificidad promedio fue 95,7%.
Grupo 5. Otras patologías
Con relación a la reactividad frente a otras patologías, ninguno de los ocho individuos que presentaron lesiones cutáneas de origen no leishmaniásico respondieron a los diferentes antígenos evaluados. Su procedencia y conformación fue la siguiente:
* Putina Punco: dos personas con diágnostico clínico de micosis.
* Colasay:
a) Varón de 21 años con lesión cutánea protuberante, sin diagnóstico establecido.
b) Escolar de 12 años con lesión punzocortante originada por accidente.
* Pacientes examinados en el INS:
a) Mujer de 21 años con aislamiento de Mycobacterium tuberculosis en cultivo de lesión cutánea.
b) Mujer de 85 años, con lesión nasal cutánea de origen neoplásico.
c) Escolar de 14 años, sexo femenino.
d) Escolar de 9 años, sexo masculino.
Estos dos últimos presentaron lesiones cutáneas superficiales, diagnosticadas clínicamente para otras patologías.
Grupo 6. Control
Todos los antígenos evaluados en este grupo, individuos sanos residentes de Lima, área no endémica, demostraron alta especificidad, no reaccionando a ningún tipo de antígeno.
RESULTADO GENERAL DE SENSIBILIDAD Y ESPECIFICIDAD
La sensibilidad, porcentaje de reacciones positivas en una población de enfermos, fue determinada mediante la aplicación de la leishmanina en 82 personas portadoras de lesiones cutáneas y/o cutáneo-mucosas activas y cicatriciales, correspondientes a los grupos 1, 2 y 3 de la población estudiada. En tanto, la especificidad, porcentaje de reacciones negativas en una población de sanos, fue determinada por aplicación de la leishmanina en 51 individuos pertenecientes a los grupos 4, 5 y 6 evaluados (Tabla 6).
REACCIONES COLATERALES
En general, reacciones normales como eritema y prurito fueron observadas en los casos activos de leishmaniasis. Excepcionalmente, un individuo conformante del grupo control negativo endémico, exhibió reacción similar a las 24 horas con la leishmanina de Leishmania (Viannia) peruviana 30 µg/mL, persistiendo una reacción mínima a las 48 horas. Durante su juventud, este individuo había sido intervenido quirúrgicamente por estar afectado de tuberculosis ósea.
Reacciones colaterales como vesiculación y reacción necrótica no fueron observadas en los grupos presentados, pero sí con el lote 2: Leishmania (Viannia) peruviana, L.(V.) braziliensis a 30ug/mL, aplicados en individuos con LC y/o LCM activos, en el Hospital de Quillabamba, provincia La Convención, departamento Cusco, los que serán objeto de una comunicación posterior.
El incremento en la dosis de antígenos de Leishmania (V.) braziliensis ha sido asociado con un incremento en la presentación de efectos colaterales no deseables 6,9. Por consiguiente, es preciso ser cautos al seleccionar la dosis del antígeno a ser empleado, en especial, cuando las infecciones son causadas por miembros del complejo braziliensis, como ocurre en nuestro país.
Figura 2. Lesiones cutáneas
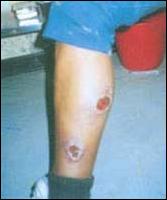
Figura 3. Lesión cutáneo-mucosa
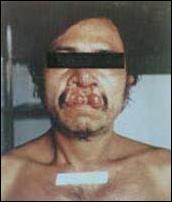
Tabla 2. Resultado general de reactividad a los antígenos (V.)
peruviana y L. (V.) braziliensis (25 y 30 μg proteínas/mL)
Tabla 3. Reactividad a los Antígenos de Leishmania (V.)peruviana y
L. (V) braziliensis (25 y 30 30 μg proteínas/mL) en pacientes
con enfermedad activa
Figura 4. Aplicación de Leishmanina
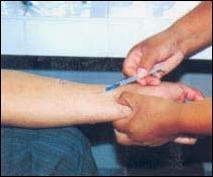
Figura 5. Reacción a las 48 horas post-aplicación
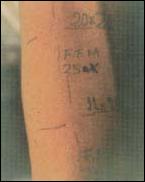
Tabla 4. Evaluación de Leishmanina 25 y 30 μg proteínas/mL:
Resultado de Reactividad (Leishmaniasis Cicatricial)
Tabla 5. Resultado de reactividad negativa a las leishmanias (25 y 30 μg
proteínas/mL)
Tabla 6. Resultado general de sensibilidad y especificidad a los antígenos
de Leishmania (V.) peruviana y Leishmania (V) braziliensis
(25 y 30 μg proteínas/mL).
DISCUSIÓN
La leishmanina no representó dificultad en su preparación y aplicación para las pruebas de intradermorreacción.
La sensibilidad promedio 95,9% (47/49) que informamos, en pacientes cutáneos y cutáneo-mucosos activos es similar a los hallazgos de otros autores en países vecinos (Tabla 7). Reed y col 4, evaluando extracto soluble de L. donovani donovani a la dosis de 25 µg proteínas/mL, encontraron 97% de sensibilidad en individuos con LV curada; su sensibilidad disminuyó a 82%, cuando, a estos mismos individuos, se les aplicó extracto de L. mexicana amazonensis, 25 µg/mL. En Colombia, Weigle y col 14, empleando parásitos fenolados de L. (Viannia) braziliensis refieren una sensibilidad de 98,5%.
En 1997, en el Estado de Campeche-México, Monroy y col 9, aplicando parásitos fenolados de L. mexicana en pacientes leishmaniásicos, obtuvieron una sensibilidad del 100%. Por su parte, Furuya y col 8, utilizando extracto soluble de L. (Viannia) panamensis 10 µg/m, informaron reacción positiva en 25/25 pacientes ecuatorianos, casos confirmados por demostración del parásito.
Porcentajes menores de positividad como el 82,7% han sido reportados por Weigle y col 14, mientras que Furuya y col 2, empleando extracto soluble L. (Viannia) braziliensis de 25 µg/mL, hallaron una sensibilidad de 93,3% en pacientes con LC activa confirmada.
En nuestro estudio, 28/30 personas con LC activa fueron sensibles a los antígenos evaluados. Uno de los dos casos con leishmanina negativa correspondió a un joven de 17 años de edad, de la localidad de Putina Punco, con lesión cutánea única de 17 días de evolución, de la cual se obtuvo formas de promastigote en cultivo. Es conocido que la reacción intradérmica se hace positiva de 4 a 6 semanas después de iniciada la infección 5, lo cual explicaría este resultado. El otro caso, también de Putina Punco, correspondió a un niño de 11 años, con serología positiva (1/40) a leishmaniasis.
En Colasay, área de transmisión de leishmaniasis andina, un niño de 9 años fue sensible a los antígenos de L. (V.) peruviana 25 y 30 µg/ mL, más no a la leishmanina L. (V.) braziliensis 25 µg/mL. En este caso, hubo mejor respuesta frente al antígeno homólogo. En el Perú, se han efectuado algunos estudios epidemiológicos con aplicación de leishmanina. En pacientes cutáneos y cutáneo-mucosos activos del valle del Apurímac (San Francisco, dpto. de Ayacucho). Castro y col 21 encontraron una reacción del 87,1%, mientras que Canario y col 20 refieren un 100% en pacientes cutáneos del caserío de Tambora (San Miguel, dpto. de Cajamarca); por otro lado, en la provincia de la Convención, dpto. de Cusco. Cjuno y col 22 evaluaron, con fines diagnósticos, a 210 personas con diagnóstico clínico de leishmaniasis, encontrando una positividad del 71,2% para la prueba intradérmica. No se tiene evidencia, en ninguno de estos estudios, que la leishmanina haya sido aplicada en pacientes con leishmaniasis confirmada.
En cuanto al 86,4% de sensibilidad demostrada en el grupo cicatricial participante de este estudio, resultados similares han sido informados; en el Ecuador, 25/29 personas con leishmaniasis cicatricial demostraron reacción de hipersensibilidad tardía al antígeno de L. Braziliensis panamensis 8.
En el grupo control de individuos sanos residentes de Lima, área no endémica, la especificidad fue del 100,0%. Estos resultados concuerdan con el 98,5% informado por Weigle y col13 utilizando promastigotes de L. (V.) panamensis, y el 96,6% obtenido por Reed y col 10 con extracto soluble de L. donovani donovani, a la concentración de 25 µg/mL de proteínas. En el Brasil, resultados semejantes fueron obtenidos por Navarrete y Biagi 26, con promastigotes fenolados de L. (V.) braziliensis y, Mayrink y col 3 utilizando un extracto soluble preparado con una mezcla de cepas de L. (V.) braziliensis, L. (V.) guyanensis, L. (L.) mexicana y L. (L.) amazonensis.
En nuestro grupo control negativo endémico, sólo 1/23 con antecedente de tuberculosis ósea reaccionó a la aplicación del antígeno de L. (V) peruviana, 30 µg/mL. Estos resultados difieren del 26%, reportado por Arzubiaga y col19 en Perú, en el cual, utilizando promastigotes de L. (V) braziliensis a una concentración proteínica equivalente a 35 µg/mL, se obtuvo 21% de respuesta positiva, la cual estaría en relación a la mayor concentración proteínica del antígeno empleado. La determinación de anticuerpos IgG mediante la prueba de IFI, en los sueros de estos individuos, dieron resultados positivos sólo a la dilución de 1/16, no obteniéndose, en ningún caso, el título positivo (1/40) a infecciones por leishmania, que consideramos en nuestro grupo de estudio.
En relación a la reactividad cruzada frente a otras patologías, los ocho individuos afectados por otras patologías no reaccionaron a ningún tipo de los antígenos evaluados.
Las diferencias en cuanto a la intensidad de la reacción, potencia, tamaño de la pápula en milímetros no guardaron relación con el tipo de antígeno utilizado, habiendo sido el eritema y el área de induración en unos casos, algo mayor para el antígeno homólogo, mientras que en otros la situación fue inversa.
Debido a la estrecha relación taxonómica que muestran los parásitos de Leishmania y Trypanosoma, diversos autores han evaluado antígenos de Leishmania en pacientes con xenodiagnóstico y serología positivos a T. cruzi; unos, no encontraron reacciones positivas 3,11 en tanto que Reed y col 10 informaron menos del 5% de reacciones con diámetros mínimos de induración entre 5-6 mm.
Fuller y col 7 informaron que antígenos hechos con cultivos de T. cruzi pueden dar reacciones positivas en casos activos de LC en las Américas, pero en magnitud menor a los producidos por antígenos de Leishmania.
La dificultad en detectar pacientes con la Enfermedad de Chagas en las áreas estudiadas no permitió su inclusión en la presente evaluación.
Tabla 7. Antecedentes de evaluación de Lesihmanina
CONCLUSIONES
* El antígeno de Leishmania (Viannia) peruviana, 25 µg/mL, resultó adecuado para la detección de la reacción de hipersensibilidad cutánea tardía, en pacientes con lesiones cutáneas y/o cutáneo-mucosas activas, encontrando una sensibilidad promedio de 95,9%. La misma sensibilidad, pero con reacciones más intensas (potencia) fue observada con el antígeno homólogo de 30 µg/mL.
* Los antígenos de Leishmania (Viannia) braziliensis, 25 y 30 µg/mL, mostraron similar sensibilidad y potencia a dosis equivalentes de Leishmania (Viannia) peruviana.
* Los antígenos demostraron ser altamente específicos. La especificidad en el grupo control alcanzó el 100%, mientras que en el grupo control endémico, fue 95,7%.
RECOMENDACIONES
La prueba de IDR, empleando el antígeno de Leishmania (Viannia) peruviana 25 µg/mL, podría ser usado como prueba auxiliar en el diagnóstico de las leishmaniasis a nivel nacional.
AGRADECIMIENTOS
Los autores desean dejar constancia de su agradecimiento al Dr. César Náquira Velarde, por la revisión y crítica del manuscrito; a los Drs. Eduardo Falconí Rosadio y Ángel Garay, por la evaluación clínica de los pacientes que acudieron al INS y los de Colasay respectivamente. Así mismo a la Blga. Silvia Vega Ch. por la asistencia técnica prestada.
REFERENCIAS BIBLIOGRÁFICAS
1. Furuya M, Eshita Y, Martini L, Gómez EA, Hashiguchi Y. Un análisis del antígeno de Leishmania para el skin test. Jpn J Trop Med Hyg 1989; 17: 325-328. [ Links ]
2. Furuya M, Mimori T, Gómez EAL, De Coronel VV, Kawabata M, Hashiguchi Y. Epidemiological survey of leishmaniasis using skin test and ELISA in Ecuador. Jpn J Trop Med Hyg 1989; 17: 331–338. [ Links ]
3. Mayrink W, Williams P, Cohelo MB, Dias M, Martins AV, Magalhaes PA, et al. Epidemiology of dermal leishmaniasis in the Rio Doce Valley, State of Minas Gerais, Brazil. Ann Trop Med Parasitol 1979; 73: 123-137. [ Links ]
4. Pellegrino M, Pereira LH, Furtado TA. Mucocutaneous leishmaniasis: intradermal test with a promastigote suspension and a crude extract from Leishmania braziliensis. Rev Inst Med Trop Sao Paulo 1977; 19: 393-396. [ Links ]
5. Melo MN, Mayrink W, De Costa CA, Magalhaes PA, Dias M, Williams P, et al. Padronizacao do antigeno de Montenegro. Rev Inst Med Trop Sao Paulo 1977; 19: 161-164. [ Links ]
6. Cuba CA, Marsden PD, Barreto AC, Jones TC, Richards F. The use of different concentrations of leishmania antigen in skin testing to evaluate delayed hypersensitivity in American cutaneous leishmaniasis. Rev Soc Brazil Med Trop 1985; 18: 231-236. [ Links ]
7. Fuller GK, Lemma A, Haile T. A comparison of skin test responses using antigen from Leishmania donovani and a lizard trypanosome. Trans Roy Soc Trop Med Hyg 1980; 74: 205-208. [ Links ]
8. Furuya M, Nonaka S, Comez EA, Hashiguchi Y. Evaluation and characterization of parcially purified skin test antigens prepared from Leishmania panamensis promastigotes. Jpn J Trop Med Hyg 1991; 19: 209–217. [ Links ]
9. Monroy A, Sosa T, Rivas B, Ruiz R, Mendoza A, Favila L. Seropidemiological studies of cutaneous leishmaniasis in the Campeche State of Mexico. Mem Inst Oswaldo Cruz 1997; 92: 21- 26. [ Links ]
10. Reed SG, Badaro R, Masur N, Carvalho EM, Lorenco R, Lisboa A, et al. Selection of a skin test antigen for American visceral leishmaniasis. Am J Trop Med Hyg 1986; 35: 79-85. [ Links ]
11. Zeledón R, Hidalgo W, De Hidalgo H. Intradermoreacción de Montenegro con antígeno de Strigomonas oncopelti. Nota previa. Rev Biol Trop 1960; 8: 145-146. [ Links ]
12. Naiff RD, Barrett TV, Arias JR, Naiff MF. Encuesta epidemiológica de histoplasmosis, paracoccidiodimicosis y leishmaniasis mediante pruebas cutáneas. Bol Of Sanit Panam 1988; 104: 35-49. [ Links ]
13. Weigle KA, Valderrama L, Arias AL, Santrich C, Saravia N. Leishmanin skin test standardization and evaluation of safety, dose, storage, longevity of reaction and sensitization. Am J Trop Med Hyg 1991; 44: 260-271. [ Links ]
14. Weigle KA, Davalos M, Heredia P, Molineros R, Saravia N, DAlessandro A. Diagnosis of cutaneous and mucocutaneous leishmaniasis in Colombia: A comparison of seven methods. Am J Trop Med Hyg 1987; 36: 489-496. [ Links ]
15. Kerdell-Vegas F. American leishmaniasis. Inter J Dermat 1982; 21: 291-303. [ Links ]
16. Davies CR, Llanos-Cuentas A, Pyke SDM, Dye C. Cutaneous leishmaniasis in the Peruvian Andes: an epidemiological study of infection and immunity. Epidemiol Infect 1995; 114: 297-318. [ Links ]
17. Weigle KA, Santrich C, Martinez F, Valderrama L, Saravia NG. Epidemiology of Cutaneous Leishmaniasis in Colombia: A longitudinal study of the natural history, prevalence and incidence of infection and clinical manifestations. J Inf Dis 1993; 168: 699-708. [ Links ]
18. Stead WW, Senner JW, Reddick WT, Lofgren JP, 1990. Racial differences in susceptibility to infection by Mycobacterium tuberculosis. The New Engl J Med 1990; 322: 422-427. [ Links ]
19. Arzubiaga C, Huayanay J, Biaggioni I, 1984. An epidemiologic study of American cutaneous leishmaniasis in Maipuco, Perú. Bull Pan Am Health Organ 1984; 18: 19-25. [ Links ]
20. Canario W, Zuñiga I, Silva T. Leishmaniasis en el caserío «La Tambora» en Bolívar, San Miguel - Cajamarca. Bol Per Paras 1995; 11:16-18. [ Links ]
21. Castro J, Maraví A, Ango H, Tejada A. Aspectos epidemiológicos de la leishmaniasis tegumentaria americana. San Francisco, Ayacucho. 1992. Libro de resúmenes del I Congreso Peruano de Parasitología. Lima, Perú. 1993, p. 10. [ Links ]
22. Cjuno M, Olivera R, Pacheco R, Quispe M, Yanacaya F. Leishmaniasis en pacientes migrantes del departamento del Cusco a zonas endémicas. Bol Per Paras 1995; 11: 13-15. [ Links ]
23. Guimaraes MCS, Giovannini VL, Camargo ME. Antigenic standarization for mucocutaneous leishmaniasis inmunofluorescence test. Rev Inst Med Trop Sao Paulo 1974; 16: 145-148. [ Links ]
24. De Ferreira LC, Laender JF. A intradermo-reacao de Montenegro no diagnóstico de leishmaniose tegumentar americana. Brasil Méd 1945; 59: 3-17. [ Links ]
25. De Pessoa SB, Barreto MP. Leishmaniose tegumentar americana. Imp Nac Río de Janeiro, 1948: 527. [ Links ]
26. Navarrete F, Biagi F. Especificidad de la reacción intradérmica de Montenegro. Pren Méd Mex 1960; 25: 321-23. [ Links ]
Correspondencia: Gloria Minaya. Instituto Nacional de Salud.
Calle Cápac Yupanqui 1400, Lima 11, Perú. Apartado postal 471.
Telf.: (0511) 4719920 - Fax: (0511) 4710179.
Email: gminaya@ins.sld.pe