Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Revista Peruana de Biología
versión On-line ISSN 1727-9933
Rev. peru biol. vol.24 no.1 Lima ene./abr. 2017
http://dx.doi.org/10.15381/rpb.v24i1.13109
doi: http://dx.doi.org/10.15381/rpb.v24i1.13109
TRABAJOS ORIGINALES
Plantas alimenticias de 19 especies de mariposas diurnas (Lepidoptera) en Loreto, Perú
Food Plants of 19 butterflies species (Lepidoptera) from Loreto, Peru
Joel Vásquez Bardales *1,2, Ricardo Zárate Gómez 1,3, Percy Huiñapi Canaquiri 1,2, Julio Pinedo Jiménez 4, Juan José Ramírez Hernández 5, Gerardo Lamas 5, Pedro Vela García 1,2
1 Instituto de Investigaciones de la Amazonía Peruana (IIAP). Av. A. Quiñones km 2.5, Iquitos, Loreto, Perú
2 Programa de Investigación en Biodiversidad Amazónica (PIBA).
3 Programa de Investigación en Cambio Climático, Desarrollo Territorial y Ambiente (PROTERRA).
4 Universidad Nacional de la Amazonia Peruana, Facultad de Agronomía. Calle Pevas s/n, Iquitos Perú
5 Universidad Nacional Mayor de San Marcos, Museo de Historia Natural. Av. Arenales 1256, Jesús María, Lima, Perú.
*Autor para correspondencia
Email Joel Vásquez Bardales: jvasquez@iiap.org.pe
Email Ricardo Zárate Gómez: rzarate@iiap.org.pe
Email Percy Huiñapi Canaquiri: pasadolinathus@yahoo.es
Email Julio Pinedo Jiménez: jupiji_61@hotmail.com
Email Juan José Ramírez Hernández: macrodontia@hotmail.com
Email Gerardo Lamas: glamasm@unmsm.edu.pe
Email Pedro Vela García: pvelacaligo@gmail.com
Resumen
El presente trabajo informa sobre las plantas alimenticias utilizadas por 19 especies de mariposas diurnas (Lepidoptera) que ocurren en el Centro de Investigaciones Allpahuayo-Mishana y la Comunidad Campesina de San Rafael, Loreto, Perú. Se reportan 23 especies y 1 híbrido de angiospermas empleadas por las mariposas investigadas. Veintiún plantas eran hospedadoras de las larvas y 5 nectaríferas de los adultos; Passiflora coccinea Aubl. y Passiflora edulis Sims eran a la vez hospederas y nectaríferas. Las familias de plantas más utilizadas por las mariposas en estado larval fueron Solanaceae, Passifloraceae, Fabaceae y Aristolochiaceae.
Palabras clave: Biocomercio; plantas hospederas; plantas nectaríferas; relaciones planta-animal; sustentabilidad.
Abstract
This work reports the food plants utilized by 19 species of butterflies from Allpahuayo-Mishana Research Center and the Community of San Rafael, Loreto, Peru. We report 23 plant species and one hybrid of angiosperms used by the butter flies. Larval host plants were 21 species and five were adult nectar sources. Two species were both host plant and nectar source: Passiflora coccinea Aubl. and Passiflora edulis Sims. The most frequently used plant families were Solanaceae, Passifloraceae, Fabaceae and Aristolochiaceae.
Keywords: Biotrade; host plants; nectar sources; plant-animal relationships; sustainability.
Introducción
Las mariposas diurnas son los insectos mejor conocidos taxonómicamente y mejor descritos (Lamas 2000); además, por su estrecha relación con las plantas, su abundancia, diversidad, y facilidad de observación son excelentes indicadores biológicos (Brown 1991, Beccaloni & Gaston 1994). Son de gran importancia agrícola, ya que sus larvas, usualmente herbívoras, pueden constituir ocasionalmente plagas de cultivos (Triplehorn & Johnson 2005, Vásquez et al. 2012). También, tienen relevancia en la industria y ecoturismo por su extraordinaria belleza, colores y formas; siendo reproducidas en cautiverio para su avistamiento (mariposarios) y la obtención de pupas con fines de exportación (New et al. 1995). Aunque, la crianza comercial de mariposas tropicales es una potencial actividad para bionegocios por sus resultados en el manejo y uso sustentable de bosques tropicales (Salazar et al. 2010), la mayoría de mariposas que se comercializan en el Perú son capturadas del medio natural para artesanías y cuadros, sin criterios sustentables (Mulanovich 2007). La mejor alternativa para remediar esta situación es llevar a cabo la crianza de dichas especies en condiciones de cautiverio o semi-cautiverio. Para realizar estas actividades de crianza, es esencial conocer las relaciones de las mariposas con las plantas hospederas de sus larvas y nectaríferas de los adultos. Tales conocimientos son fundamentales para desarrollar estudios bioecológicos (comportamiento de cortejo, cópula, oviposición, capacidad reproductiva y alimentación) que permitan efectuar ensayos de adaptación reproductiva y alimentaria en condiciones controladas.
Para el Perú existen pocas publicaciones dedicadas a la relación de las plantas con las mariposas, si bien existe una extensa compilación de las mariposas y sus plantas hospederas en el neotropico (Beccaloni et al. 2008) donde se encuentra valiosa información. Específicamente para el Perú, Lamas (1985) publicó una lista de mariposas de las familias Papilionidae, Pieridae y Nymphalidae de la Reserva Tambopata, en Madre de Dios, Perú, y enumeró diversas plantas hospederas que se presume puedan servir de alimento a las larvas de tales especies, muchas de ellas reportadas a nivel de género. Racheli y Callegari (1988), para Satipo (Junín), reportaron una especie de Aristolochia (Aristolochiaceae) como planta hospedera del papiliónido Parides neophilus. Tákács y Tello (1993a, 1993b, 1994) registraron Erythroxylum sp. como planta hospedera de Agrias amydon boliviensis, y dos especies de plantas hospederas para dos especies de Morpho. Mulanovich (2007) presentó una lista de 35 especies comerciales de mariposas y sus plantas hospederas, de los más de 4300 lepidópteros registrados hasta ahora para Perú (Lamas 2000 y datos inéditos). Vásquez et al. (2007, 2010, 2012) enumeraron las plantas hospederas de seis especies de mariposas del departamento de Loreto. Finalmente, Gallusser et al. (2010) y Ramírez et al. (2014) presentaron estudios detallados sobre el ciclo de vida y ecología de dos especies de Morpho del departamento de San Martín (Perú).
En este estudio damos a conocer las especies de plantas hospederas y nectaríferas utilizadas por 19 especies comerciales de mariposas del departamento de Loreto, con miras a efectuar futuros ensayos de adaptación reproductiva y alimentaria en condiciones de cautiverio y semicautiverio.
Material y métodos
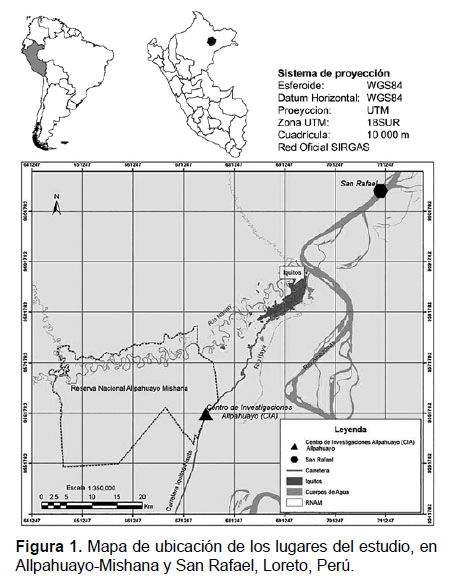
Área de estudio.- El presente estudio se realizó de febrero del 2010 a diciembre del 2014 en dos localidades: (1) Comunidad Campesina San Rafael, río Amazonas, distrito de Indiana (3°33’40.21"S; 73°07’07.17"W, 110 m); y (2) Centro de Investigaciones Allpahuayo (CIA, en la Reserva Nacional Allpahuayo Mishana), distrito de San Juan (3°38’01.99"S; 73°25’08.86"W, 160 m), ambas localizadas en la provincia de Maynas, Región Loreto (Fig. 1).
San Rafael presenta una temperatura anual media de 26 °C, con una precipitación promedio anual de 2900 mm, siendo los meses de mayor pluviosidad enero y febrero. La zona tiene características de bosque húmedo tropical, sus suelos son de baja fertilidad, y el terreno es relativamente llano.
El Centro de Investigaciones Allpahuayo presenta temperatura media anual mayores a 24 °C y precipitaciones promedio anuales mayores a 2400 mm, distribuidas sin una estación seca definida; no obstante, la estación más lluviosa se presenta de noviembre a mayo.
Especies consideradas.- Los 19 taxa de mariposas estudiadas fueron: Archaeoprepona demophon muson (Fruhstorfer, 1905); Caligo idomeneus idomenides Fruhstorfer, 1903; Dione juno (Cramer, 1779); Dryadula phaetusa (Linnaeus, 1758); Dryas iulia alcionea (Cramer, 1779); Heliconius erato (Linnaeus, 1758); Heliconius numata Cramer, 1780; Heliconius sara sara (Fabricius, 1793); Heraclides anchisiades (Esper, 1788); Heraclides thoas cinyras (Ménétriés, 1857); Mechanitis polymnia (Linnaeus, 1758); Memphis acidalia acidalia (Hubner, 1819); Methona confusa psamathe (Godman & Salvin,1898); Morpho helenor theodorus Fruhstorfer, 1907; Morpho marcus intermedia Kaye, 1917; Morpho menelaus occidentalis (C. Felder & R. Felder, 1862); Parides aeneas (Linnaeus, 1758); Parides pizarro pizarro (Staudinger, 1884); y Philaethria dido (Linnaeus, 1763).
Mariposas relacionadas a las plantas hospederas y nectaríferas.- Para reconocer las plantas nectaríferas asociadas a las mariposas, en el medio natural se observaron a los adultos que visitaban las flores, estos fueron capturados con una red entomológica cuando estaban alimentándose, y colocados en sobres entomológicos para su transporte al laboratorio, donde fueron montadas para su posterior identificación. Para el caso de las plantas hospederas, se observó el comportamiento de oviposición de las hembras, en el hábitat natural, después de producida, se recolectó los huevos. También se realizó búsquedas de huevos y larvas de mariposas en plantas hospederas potenciales, que luego se llevaron al laboratorio para confinarlas en envases de crianza. Las larvas recolectadas y las emergidas de los huevos fueron alimentadas con su planta de origen hasta la obtención de los adultos.
Solamente en el caso específico de las mariposas Morpho menelaus occidentalis, M. helenor theodorus y Archaeoprepona demophon muson se registraron algunas plantas hospederas en condiciones de cautiverio; para ello se utilizó un mariposario de 250 m2 con 6 m de altura cubierta con una malla "raschell" de 65% de sombra que contenía diversas plantas, luego se recolectaron hembras del bosque y se colocaron en el interior del mariposario, las que fueron alimentadas con frutos maduros de plátano (Musa x paradisiaca L.) fermentado en jugo del tallo de caña (Saccharum officinarum L.) debido al habito frugívoro que presentan estos géneros (De Vries,1988; Takacs & Tello, 1993, Mulanovich, 2007; Guerra-Serrudo y Ledezma-Arias 2008, Ruiz et. al. 2015). Los huevos y las larvas encontrados fueron recolectados y se criaron en el laboratorio hasta la obtención de los adultos. Las muestras botánicas detectadas fueron colectadas y transportadas al laboratorio para su respectiva herborización de acuerdo a Judd et al. (1999).
Muestreo de las plantas.- Las especies de plantas fueron herborizadas siguiendo lo recomendado por Judd et al. (1999). Para su identificación se empleó las publicaciones de Spichiger et al. (1989, 1990), Gentry (1993), Vásquez (1997), Ribeiro et al. (1999), Vásquez y Rojas (2004), y Zárate et al. (2015). También fueron consultadas fotografías de exsiccata del Missouri Botanical Garden, St. Louis, Missouri, EE.UU. y del Field Museum of Natural History, Chicago, EE.UU. El sistema de clasificación utilizado fue el propuesto por APG III (2009).
Tratamiento de las especies de mariposas.- Los ejemplares de mariposas fueron preparados siguiendo las técnicas usuales (v.g. Andrade et al. 2013). La identificación de las especies se efectuó utilizando claves especializadas y comparación directa con muestras depositadas en el Museo de Historia Natural, Universidad Nacional Mayor de San Marcos, Lima (Perú).
Resultados y discusión
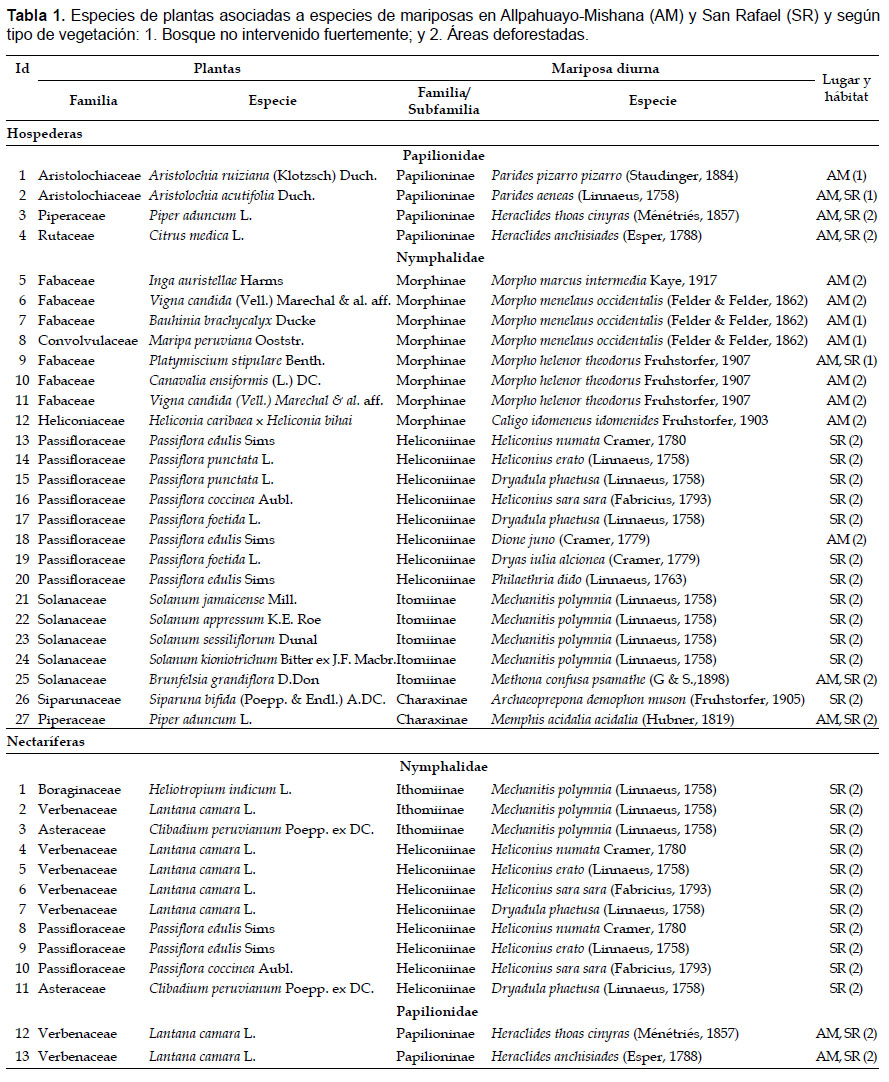
Reportamos 23 especies (más 1 híbrido) de angiospermas (incluidas en 12 familias y 17 géneros), asociadas a 19 especies (algunas subespecies) de mariposas diurnas (Tabla 1). Las familias Fabaceae, Solanaceae, Passifloraceae y Aristolochiaceae presentaron la mayor cantidad de especies utilizadas, tanto en el estado de larva como en adulto. Las especies de plantas asociadas al mayor número de especies de mariposas adultas son: Lantana camara (7 especies), Passiflora edulis (2), Clibadium peruvianum (2), Heliotropium indicum (1), y otras.
Las plantas nectaríferas cumplen un rol fundamental en la reproducción de las mariposas, atraen principalmente a los machos (Boggs & Gilbert 1979), debido a que en ella se encuentran nutrientes (alcaloides) como la pyrrolizidina precursores de feromonas sexuales que se encuentra en el néctar de las flores como la de Heliotropium indicum y varias especies de Asteraceae (Boppré 1978, Edgar 1982, Masters 1968, Lamas & Pérez 1981, Stegelmeier 2011). Estos alcaloides son trasferidos por los machos a las hembras a través de su esperma para la producción de sus huevos principalmente en Ithomiinae (Boggs & Gilbert 1979). Las mariposas del género Heliconius combinan su alimentación con polen y néctar (Boggs & Gilbert 1979) ya que sin estos nutrientes su tasa de reproducción y su longevidad disminuyen drásticamente (Mulanovich 2007). Para su reproducción es importante la utilización de flores de Passiflora edulis por que poseen abundante néctar y liberan polen (Peña 2003). La propagación de P. edulis es través de semillas mientras que Passiflora coccinea es muy difícil encontrarlas en fructificación. Lantana camara contiene abundante néctar, posee flores adaptadas para lepidópteros, los mismos que son sus polinizadores (Aguilar 1965), su presencia es necesario para la crianza de mariposas, su mejor propagación es por estacas y su enraizamiento en agua se da entre una y dos semanas.
Las especies de plantas asociadas al mayor número de especies de mariposas en estado larval fueron: Passiflora foetida (2), Passiflora edulis (2), Piper aduncum (2), y Vigna candida aff. (2).
El 69.6% de plantas (16 spp.) provinieron de áreas deforestadas, donde la vegetación se encuentra en proceso de recuperación; el 21.7% (5 spp.) provino del bosque no intervenido fuertemente (ver Tabla 1).
Nuestros resultados muestran una relación entre grupos discretos de lepidópteros con grupos discretos de plantas, como el enfatizado en el trabajo clásico de Ehrlich y Raven (1965). Así, las especies Parides aeneas y P. pizarro pizarro tienen como hospederos a Aristolochia acutifolia y A. ruiziana respectivamente, lo que corrobora la estrecha dependencia de especies de Parides con Aristolochia mencionada por Lamas (1985) y DeVries (1987), quienes indican que las larvas de Parides están relacionadas a las Aristolochiaceae, constituyéndose en especies oligófagas. Adicionalmente, Tyler et al. (1994) y Beccaloni et al. (2008) registran a A. acutifolia como hospedero de P. aeneas, P. anchises, P. echemon, P. lysander, P. neophilus, P. panthonus, P. sesostris y P. vertumnus en Brasil. Sin embargo, Racheli y Callegari (1988) indican que A. ruiziana es utilizada por P. neophilus en Satipo (Perú). Por lo tanto, P. pizarro y P. neophilus pueden alimentarse, en su fase larval, del mismo hospedero en diferentes lugares (una en Brasil y otra en Perú).
De las tres especies de Morpho investigadas, la mayor cantidad de hospederos pertenecen a Fabaceae. Sin embargo también se encontró a Morpho menelaus occidentalis ovipositando en hojas de Maripa peruviana (Convolvulaceae); así como Gallusser et al. (2010) y Ramírez et al. (2014) quienes reportaron a las larvas de Morpho telemachus martini y M. cisseis phanodemus alimentándose de Abuta grandifolia (Menispermaceae); lo que indica que las larvas de Morpho pueden ser polífagas; estos datos son confirmados por Lamas (1985), Tákács y Tello (1993a, 1994), Constantino (1997), Constantino y Corredor (2004), Guerra-Serrudo y Ledezma-Arias (2008), Beccaloni et al. (2008), Montero y Ortiz (2010), Gallusser et al. (2010).
El mejor hospedero en cautiverio para Morpho helenor theodorus fue Platymiscium stipulare y para Morpho menelaus occidentalis Vigna candida aff.; el primero se reproduce por semilla y por estacas en cambio la segunda su mejor propagación se da por semilla.
Reportamos aquí a Passiflora edulis como hospedero de tres especies: Heliconius numata, Dione juno y Philaethria dido; resultados similares fueron reportados por Beccaloni et al. (2008) para Brasil, Belize, Colombia, Costa Rica, El Salvador y Venezuela. Mientras que a Passiflora punctata lo encontramos como hospedero de Heliconius erato y Dryadula phaetusa. Resultados similares encontraron Beccaloni et al. (2008) en Colombia y Panama, y para Heliconius erato cyrbia en Ecuador. Sin embargo Becaloni et al. (2008) reportan a P. punctata como hospedero de Dryadula phaetusa en cautiverio, en cambio nosotros lo encontramos como hospedero natural.
Estos resultados concuerdan con lo publicado por Beccaloni et al. (2008) para varios países neotropicales como Trinidad y Tobago, Venezuela, Costa Rica y El Salvador. Todas estas especies de Heliconiinae en estado larval tiene habito alimenticio de tipo oligófago, sin embargo existe especificidad con las especies de mariposa que utilizan como hospedero a Passiflora para su reproducción en cautiverio, como es el caso de Dryas iulia alcionea que utiliza solo Passiflora foetida; y Dryadula phaetusa, que en el medio natural se reproduce en Passiflora foetida y Passiflora punctata, mientras que en cautiverio solo tuvimos éxito reproductivo utilizando P. punctata. Sin embargo, en condiciones de cautiverio, Dryadula phaetusa puede utilizar P. biflora como hospedero en Colombia (Acosta Guio & Blanco Martínez 2009) en cambio las Heliconius erato, Heliconius numata y Dione juno se pueden reproducir en cautiverio sobre P. edulis. Todas las especies de Passiflora se propagan con éxito a partir de semilla, la única plaga encontrada que retarda el crecimiento de P. punctata es un Lepidóptero nocturno de la familia Pyralidae que barrena el tallo y mata la parte aérea de la planta.
Entre los Ithomiinae, Mechanitis polymnia y Methona confusa psamathe en estado larval utilizan como hospederos a especies de Solanaceae, tales como Solanum jamaicense, S. appressum, S. sessiliflorum, y S. kioniotrichum para Mechanitis polymnia, y Brunfelsia grandiflora para Methona constituyéndose en especies oligófagas, siendo M. polymnia la especie con mayor número de hospederas y Methona confusa psamathe con un solo hospedero y no usa las especies que utiliza M. polymnia, siendo las especies de Solanum jamaicense y S. sessiliflorum las mejores hospederas para M. polymnia en condiciones de cautiverio. Resultados similares fueron reportados por Lamas (1975) para Mechanitis polymnia dorissides en Perú, Beccaloni et al. (2008) para M. p. isthmia en Costa Rica, M. p. dorissides y M. p. casabranca en Brasil, M. p. dorissides en Ecuador, M. p. veritabilis en Venezuela, y Methona confusa psamathe en Ecuador y Venezuela. La propagación de estas especies hospederas es por semilla.
Las especies de mariposas, al menos las del presente estudio, tienden claramente a asociarse a la misma especie o grupos de especies del mismo género o familia de plantas en diferentes lugares del neotrópico, tal como lo expresan Beccaloni et al. (2008).
Siete especies de mariposas están asociadas a cinco especies de plantas nectaríferas (Tabla 1), lo que está indicando que hay especies de plantas que son nectaríferas de más de una especie de mariposa. Las especies más importantes de plantas, por la cantidad de especies de mariposas que las utilizan, corresponden a Lantana camara (7 especies), Clibadium peruvianum (2) y Passiflora edulis (2). Lantana camara se relaciona con siete especies de mariposas, entonces posiblemente todas estas mariposas sean sus polinizadores tal como indica Aguilar (1965) quien precisando que el 95% de sus polinizadores está constituido por lepidópteros, y además las especies de Heliconius están utilizando el néctar y el polen para su proceso reproductivo (Mulanovich 2007).
La ocurrencia de especies de mariposas depende de sus plantas alimenticias, en Allpahuayo Mishana se ha observado la mayor presencia de mariposas indicadoras de bosque de baja intervención (bosque primario) como es el caso de los Morphinae. En cambio San Rafael es una zona deforestada con fines agrícolas en proceso de recuperación (purmas) donde ocurre la mayoría de mariposas de la sub familia Heliconinae cuyas plantas alimenticias se desarrollan en estos tipos de hábitat.
Adicionalmente podemos mencionar que, los clados filogenéticamente más basales de las mariposas diurnas, de acuerdo a la clasificación de Jong et al. (1996) están asociados a los clados más basales de las angiospermas, de acuerdo al sistema de clasificación del APG III (2009). Así, Heraclides thoas cinyras, Parides pizarro pizarro y P. aeneas (Papilioninae), formando un grupo basal de las mariposas diurnas, están asociadas a Piper aduncum, Aristolochia ruiziana y A. acutifolia, plantas consideradas en el grupo basal de las angiospermas. En el otro extremo evolutivo sucede lo mismo: Mechanitis polymnia, ubicada entre los clados más recientes de las mariposas diurnas, está relacionada a Solanum jamaicense, S. appressum, S. sessiliflorum, S. kioniotrichum, Heliotropium indicum, Lantana camara y Clibadium peruvianum, que corresponden a grupos recientes de angiospermas, como también ocurre con Methona confusa psamathe y Brunfelsia grandiflora. Esta información ayuda a comprender que las mariposas están coevolucionando con las plantas.
Agradecimientos
Este trabajo fue financiado por el "Programa Nacional de Innovación para la Competitividad y Productividad, Innóvate-Perú" a través del sub-proyecto "Modelos tecnológicos de crianza de 10 especies de mariposas diurnas para su aprovechamiento en bionegocios en la Región Loreto", conducido por el Programa de Investigación en Biodiversidad Amazónica, Instituto de Investigaciones de la Amazonía Peruana, Iquitos. Los autores agradecen a Juan José Bellido Collahuacho y un revisor anónimo por la revisión y comentarios que enriquecieron los resultados. A George P. Gallardo Gonzales por la ayuda en el sistema de información geográfica.
Información sobre los autores:
JVB, RZG, diseño de la presente investigación. JVB, evaluación de plantas y crianza en cautiverio. RZG y PVG colecta e identificación de las muestras botánicas. PHC, realizó observaciones y muestreo en campo. JJRH y GLM realizaron la identificación taxonómica de las mariposas. JVB, RZG, JPJ la redacción de gran parte del presente manuscrito. Todos los autores revisaron y aprobaron el manuscrito.
Los autores no incurren en conflictos de intereses.
Fuentes de financiamiento: El presente trabajo se realizó gracias al financiamiento del Programa Nacional de Innovación para la Competitividad y Productividad, Innóvate-Perú.
Literatura citada
Acosta Guio M.A. & M.A. Blanco Martínez. 2009. Establecimiento y adaptación de dos especies de lepidópteros de trópico bajo y medio, a condiciones controladas en la sabana de Bogotá. Tesis (Zootecnista). Universidad de La Salle. Facultad de Ciencias Agropecuarias. Programa de Zootecnia. 104pp.URI: http://hdl.handle.net/10185/6173 (Acceso 18/10/15). [ Links ]
Andrade M.G., E.R. Henao & P. Triviño. 2013. Técnicas y procesamiento para la recolección, preservación y montaje de mariposas en estudios de biodiversidad y conservación.(Lepidoptera: Hesperioidea – Papilionoidea). Revista de la Academia Colombiana de Ciencias Exactas Físicas y Naturales 37(144): 311-325. [ Links ]
Aguilar P.G. 1965. Algunas Consideraciones Sobre los Insectos Polinizadores en los Alrededores de Lima. Revista Peruana de Entomología 8 (1): 138-145. [ Links ]
APG III (Angiosperm Phylogeny Group). 2009. An update of the Angiosperm Phylogeny Group classification for the orders and families of flowering plants. Botanical Journalof the Linnean Society 161 (2): 105-121. http://dx.doi.org/10.1111/j.1095-8339.2009.00996.x [ Links ]
Beccaloni G.W. & K.J. Gaston 1994. Predicting the species richness of Neotropical forest butterflies: Ithomiinae (Lepidoptera: Nymphalidae) as indicators. Biological Conservation 71(1):77-86. http://dx.doi.org/10.1016/0006-3207(94)00023-J [ Links ]
Beccaloni G., A. Viloria, S. Hall & G. Robinson. 2008. Catálogo de las plantas huésped de las mariposas neotropicales. Zaragoza,Sociedad Entomológica Aragonesa. (m3m-MonografíasTercer Milenio, Volumen 8). 536pp. [ Links ]
Boggs C.L. & L.E. Gilbert. 1979. Male contribution to egg production: first evidence for transfer of nutrients at mating inbutterflies. Science 206: 83-84. http://dx.doi.org/10.1126/science.206.4414.83 [ Links ]
Boppré M. 1978. Chemical communication, plant relationships, and mimicry in the evolution of danaid butterflies. EntomologiaExperimentalis et Applicata 24: 264-277. http://dx.doi.org/10.1111/j.1570-7458.1978.tb02782.x [ Links ]
Brown K.S. 1991. Conservation of Neotropical environments: Insectsas indicators, pp. 349-404. In: Collins N.M. & J. A. Thomas(Eds.), The Conservation of Insects and their Habitats.London, Academic Press. [ Links ]
Brown K.S. & F. Fernández. 1985. Los Heliconiini (Lepidoptera,Nymphalidae) de Venezuela. Boletín de EntomologíaVenezolana 3(4):29-73. [ Links ]
Constantino L.M. 1997. Natural history, immature stages andhostplants of Morpho amathonte from western Colombia (Lepidoptera: Nymphalidae: Morphinae). Tropical Lepidoptera, 8(2): 75-80. [ Links ]
Constantino L.M. & Corredor G. 2004. The biology, and morphologyof the early stages of Morpho macrophthalmus and Morphopeleides telamon (Nymphalidae: Morphinae) from WesternColombia. Boletín Científico. Museo de Historia Natural. Universidad de Caldas 8: 201-209. [ Links ]
DeVries P.J. 1987. The butterflies of Costa Rica and their natural history. Papilionidae, Pieridae, Nymphalidae. Princeton,Princeton University Press. 327pp. [ Links ]
Edgar J.A. 1982. Pyrrolizidines alkaloids sequestered by Solomon IslandDanaine butterflies. The feeding preferences of the Danainaeand Ithomiinae. Journal of Zoology (London) 196: 385-399.http://dx.doi.org/10.1111/j.1469-7998.1982.tb03510.x [ Links ]
Ehrlich P.R. & P.H. Raven. 1965. Butterflies and plants: a study in coevolution. Evolution 18(4):586-608. Stable URL: http://www.jstor.org/stable/2406212 [ Links ]
Gallusser S., C. Ramírez & P. Blandin. 2010. Observaciones sobre el desarrollo y polimorfismo de Morpho (Iphimedeia)telemachus (Linnaeus, 1758) en el noreste Peruano (Lepidoptera, Nymphalidae, Morphinae). Bulletin de la Société entomologique de France 115(1):5-15. [ Links ]
Gentry A. 1993. A Field Guide to the families and genera of woody plants of Northwest South America (Colombia, Ecuador, Peru) with supplementary notes on herbaceous taxa. Washington, DC, Conservation International. 895pp. [ Links ]
Guerra-Serrudo J. & J. Ledezma-Arias. 2008. Biología y morfología de Morpho menelaus godartii (Lepidoptera: Nymphalidae: Morphinae) en el Parque Nacional Cotapata (Bolivia).Ecología en Bolivia 43(1):40-52. [ Links ]
Jong R., R.I. Vane-Wright, P.R. Ackery. 1996. The higher classification of butterflies (Lepidoptera): problems and prospects. Insect Systematics & Evolution 27(1):65-101. https://doi.org/10.1163/187631296X00205 [ Links ]
Judd W.S., C.S. Campbell, E.A. Kellogg, P.F. Stevens. 1999. Plant Systematics. A phylogenetic approach. Sunderland, Sinauer Associates. 464pp. [ Links ]
Lamas G. 1975. Mariposas diurnas (Lepidoptera, Rhopalocera) que atacan plantas de interés agrícola en el Perú. Revista Peruanade Entomología 18(1):2-5. [ Links ]
Lamas G. 1985. Los Papilionoidea (Lepidoptera) de la Zona de Reservada de Tambopata, Madre de Dios, Perú. I. Papilionidae, Pieridae y Nymphalidae (en parte). Revista Peruana deEntomología 27:59-73. [ Links ]
Lamas G. 2000. Estado actual del conocimiento de la sistemática de los lepidópteros, con especial referencia a la Región Neotropical,pp. 253-260. In: Martín-Piera, F., J. J. Morrone & A. Melic (Eds.), Hacia un Proyecto CYTED para el Inventario y Estimación de la Diversidad Entomológica en Iberoamérica: PrIBES 2000. Zaragoza, Sociedad Entomológica Aragonesa. [ Links ]
Lamas G., J.E. Pérez. 1981. Danainae e Ithomiinae (Lepidoptera: Nymphalidae) atraidos por Heliotropium (Boraginaceae) en Madrede Dios, Peru. Revista Peruana Entomologica 24: 59-62. [ Links ]
Masters J. H. 1968. Collecting Ithomidae with Heliotrope. Journal of the Lepidopterists' society 22 (2): 108-110. [ Links ]
Montero F. & M. Ortiz. 2010. Descripción de los estados inmaduros deMorpho rhodopteron nevadensis (Lepidoptera: Nymphalidae:Morphinae). Tropical Lepidoptera Research 20(2):71-76. [ Links ]
Mulanovich A.J. 2007. Mariposas. Guía para el manejo sustentable delas mariposas del Perú. Lima, Comisión para la Promociónde Exportaciones-PROMPEX, Instituto de Investigaciones dela Amazonía Peruana-IIAP, Cooperación Técnica Alemana-GTZ. 98pp. [ Links ]
New T.R., R.M. Pyle, J.A. Thomas et al. 1995. Butterfly conservation management. Annual Review of Entomology 40: 57-83. [ Links ]
Peña J. E. 2003. Insectos polinizadores de frutales tropicales: no solo lasabejas llevan la miel al panal. Manejo Integrado de Plagas y Agroecología (Costa Rica) 69: 6-20. URI http://hdl.handle.net/11554/6417 [ Links ]
Racheli T. & M.C. Callegari. 1988. Notes of the life history of Parides neophilus (Geyer, 1837) in Peru (Lepidoptera, Papilionidae).Fragmenta entomologica 21(1): 67-74. [ Links ]
Ramírez C., S. Gallusser, G. Lachaume et al. 2014. The ecology and life cycle of the Amazonian Morpho cisseis phanodemus Hewitson, 1869, with a comparative review of early stages inthe genus Morpho (Lepidoptera: Nymphalidae: Morphinae).Tropical Lepidoptera Research 24(2): 67-80. [ Links ]
Ribeiro J.E., M.J. Hopkins, A. Vicentini et al. 1999. Flora da Reserva Ducke. Guia de identificação das plantas vasculares deuma floresta de terra-firme na Amazônia Central. Manaus, INPA. 799pp. [ Links ]
Ruíz E., J. Vásquez, R. Zárate et al. 2015. Aspectos biológicos de Morpho helenor theodorus (Fruhstorfer) (Lepidoptera: Nymphalidae; Morphinae) y Mechanitis polymnia (Linnaeus), (Lepidoptera: Nymphalidae; Ithomiinae), en la Amazonia baja de Perú. Folia Amazónica 24 (1):45-54. [ Links ]
Salazar J.A., J.I. Vargas, A.M. Mora et al. 2010. Identificación preliminar de los Rhopalocera que habitan el Centro Experimental Amazónico (C.E.A.) Mocoa-Putumayo – y algunas especies aptas para criar en cautiverio (Insecta: Lepidoptera). Boletíncientífico. Museo de Historia natural. Universidad de Caldas 14(1):150-188. [ Links ]
Spichiger R., J. Méroz, P. Loizeau et al. 1989. Contribución a la Flora dela Amazonia Peruana. Los Árboles del Arborétum Jenaro Herrera. Volumen I. Moraceae a Leguminosae. Boissiera, 43:1-359. [ Links ]
Spichiger R., J. Méroz, P. Loizeau et al. 1990. Contribución a la Flora de la Amazonia Peruana. Los Árboles del Arborétum Jenaro Herrera. Volumen II. Linaceae a Palmae. Boissiera, 44:1-565. [ Links ]
Stegelmeier B.L. 2011. Pyrrolizidine Alkaloid– Containing ToxicPlants (Senecio, Crotalaria, Cynoglossum, Amsinckia, Heliotropium, and Echium spp.). Veterinary Clinics of North America: Food Animal Practice 27 (2): 419-428. http://dx.doi.org/10.1016/j.cvfa.2011.02.013 [ Links ]
Tákács M. & C. Tello. 1993a. Notas sobre la biología de Morpho deidamia Hubner, 1819 (Lepidoptera: Nymphalidae). Revista Peruana de Entomología 35: 37-40. [ Links ]
Tákács M. & C. Tello. 1993b. Notas sobre la biología de Agrias amydonboliviensis Fruhstorfer, 1915 (Lepidoptera: Nymphalidae). Revista Peruana de Entomología 35: 41-44. [ Links ]
Tákács M. & C. Tello. 1994. Notas sobre la biología de Morphorhetenor f. cacica Staudinger, 1875 (Lepidoptera; Nymphalidae). Revista Peruana de Entomología 36: 31-34. [ Links ]
Triplehorn C.A. & N.F. Johnson. 2005. Borror and DeLong's Introduction to the Study of Insects. Ed. 7. Belmot, Thomson Brooks/Cole. 864pp. [ Links ]
Tyler H.A., K.S. Brown & K.H. Wilson. 1994. Swallowtail butterflies of the Americas. A study in biological dynamics, ecological diversity, biosystematics, and conservation. Gainesville,Scientific Publishers. 376pp. [ Links ]
Vásquez J., G. Lamas, G. Couturier et al. 2012. Aspectos biológicos de Panacea prola amazonica (Fruhstorfer) (Lepidoptera:Nymphalidae), en la Amazonia peruana. Folia Amazónica 21(1/2): 71-76. [ Links ]
Vásquez J., K. Mejía, A. Gonzales et al. 2010. Sistema de crianza comunal de 06 especies de mariposas diurnas con alto potencialde exportación, en la Región Loreto. Informe técnico final IIAP – INCAGRO. 55pp. [ Links ]
Vásquez J., E. Rengifo & G. Couturier. 2007. Ciclo biológico de Battuspolydamas (Linnaeus) (Lepidoptera: Papilionidae) en la Amazonía de Perú. Revista Peruana de Entomología 45: 101-103. [ Links ]
Vásquez R. 1997. Flórula de las Reservas Biológicas de Iquitos, Perú. St. Louis, Missouri Botanical Garden Press. 1046pp. [ Links ]
Vásquez R. & R. Rojas. 2004. Plantas de la Amazonía peruana. Clave para identificar las familias de Gymnospermae y Angiospermae. Arnaldoa (Edición especial). 261pp. [ Links ]
Zárate R., T. J. Mori, F. F. Ramírez et al. 2015. Lista actualizada y clavepara la identificación de 219 especies arbóreas de los bosquessobre arena blanca de la Reserva Nacional AllpahuayoMishana, Perú. Revista Acta Amazonica 45 (2): 133 – 156. [ Links ]
Apéndice 1. A) Larva de Parides pizarro pizarro sobre hojas de Aristolochia ruiziana; B) Larva Morpho menelaus occidentalis sobre hoja de Bauhinia brachycalyx; C) Larva de Morpho helenor theodorus sobre hoja de Platymiscium stipulare; D) Larva de Archaeoprepona demophon muson sobre hoja de Siparuna bifida; E) Larva de Caligo idomeneus idomenides sobre hoja de Heliconia caribaea x Heliconia bihai; F) Larva de Mechanitis polymnia sobre hoja de Solanum appressum.
Apéndice 3. A) Larva de Heliconius numata sobre hojas de Passiflora edulis; B) Larva Philaethria dido sobre hoja de P. edulis; C) Larva de Dryas iulia alcionea sobre hoja de P. foetida; D) Larva de Dryadula phaetusa sobre hoja de P. foetida; E) Larva de Heraclides anchisiades sobre hoja de Citrus medica; F) Larva de Methona confusa psamathe sobre hoja de Brunfelsia grandiflora.
Presentado: 30/11/2015
Aceptado: 25/01/2017
Publicado online: 20/03/2017